GPSYCH:瑞金医院团队报告全球首个间充质干细胞衍生外泌体喷鼻治疗阿尔茨海默病临床试验结果,患者认知功能有所改善!
来源:奇点糕 2023-11-02 17:09
最近,由于2023年阿尔茨海默病临床试验(CTAD)会议的举行,不同机制的AD新药早期临床试验结果一个接一个地报告,前有针对淀粉样蛋白前体蛋白(APP)基因的短干扰RNA(siRNA)药物ALN-AP
最近,由于2023年阿尔茨海默病临床试验(CTAD)会议的举行,不同机制的AD新药早期临床试验结果一个接一个地报告,前有针对淀粉样蛋白前体蛋白(APP)基因的短干扰RNA(siRNA)药物ALN-APP,后有靶向微管相关蛋白tau(MAPT)mRNA的反义寡核苷酸(ASO)药物BIIB080。
就在奇点糕以为CTAD已经结束,应该暂时没有新药消息了的时候,今天突然在General Psychiatry期刊上又看到了一个使用间充质干细胞(MSC)来源的外泌体喷鼻治疗AD的新临床试验结果[1]!
这项I/II期临床试验(NCT04388982)由上海交通大学医学院附属瑞金医院王刚教授团队开展,共同通讯作者还包括上海交通大学医学院高晓玲研究员和瑞金医院任汝静副主任医师。
研究团队使用低中高三种剂量的MSC外泌体对AD患者进行治疗,中等剂量组受试者阿尔茨海默病评估量表-认知部分(ADAS-cog)评分在第12周下降了2.33,蒙特利尔认知评估基础量表(MoCA-B)评分增加了2.38,表明认知功能有所改善。此外,中等剂量组受试者ADAS-cog评分至第36周持续下降3.98分。没有报告不良事件,安全性指标无明显异常。

这是首个使用MSC外泌体治疗AD的临床试验,证实了经鼻给药的安全性,并且为下一阶段的试验提供了剂量标准。
近年来,外泌体被发现在AD中发挥重要作用,调节β淀粉样蛋白(Aβ)的聚集和清除[2],MSC衍生的外泌体相比MSC自身,具有低免疫原性、容易获得、在收集或分化过程中无需侵入性操作,以及储存简单等优势[3]。
此前研究团队在AD小鼠(APP/PS1模型)中开展的研究显示,健康人类来源的脂肪衍生MSC外泌体(ahaMSCs-Exos)经鼻给药后,可以通过嗅觉系统快速扩散到多个脑区,主要被神经元吸收,显示出神经保护作用,小鼠的神经发生增加,Aβ沉积减少,小胶质细胞激活得到抑制,空间记忆能力改善[4]。
本次开展的临床试验是一项三臂、开放标签、单中心、药物干预I/II期临床试验,在2020年4月至2022年4月间进行,分为3个阶段:筛选阶段(21天)、干预阶段(12周)和随访阶段(48周),给药剂量分为高(8×108)、中(4×108)、低剂量(2×108),在1mL生理盐水中稀释,经鼻给药,每周2次。
试验采取“3+3”设计,按照剂量由低到高划分,例如,如低剂量组的3例受试者中没有出现剂量限制性毒性(DLT),则试验转移至中等剂量组进行,如出现1例DLT,则增加额外的3例受试者,所有受试者均接受医学观察。理论上来讲,试验需要3-18例受试者。
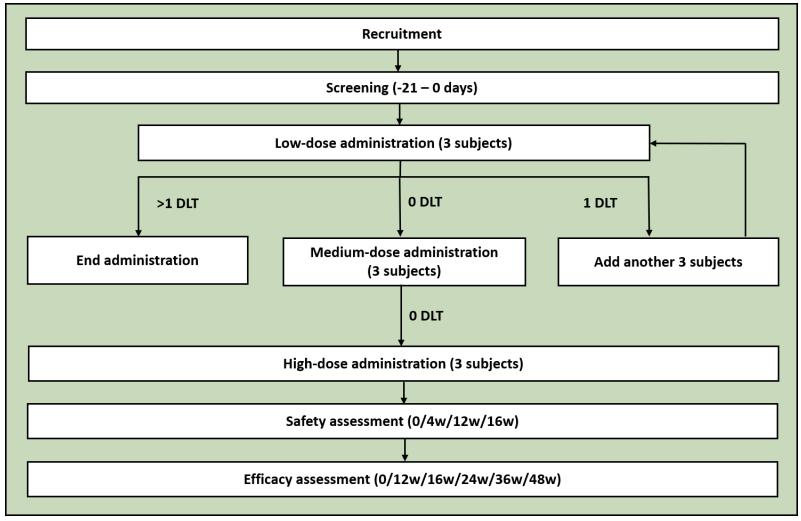
试验设计示意
受试者入组要求为≥50岁,诊断结果为轻度或中度AD,暂停使用认知增强药物和其他获批上市的AD治疗药物。
共9例受试者入组,其中4例为女性,所有受试者均完成了治疗,1例受试者因个人原因退出了随访。
治疗期间,没有受试者报告不良事件(AE)或严重不良事件(SAE),也没有鼻部不适,血压和心率波动无明显异常,1例报告有偶尔发生的心动过缓,没有过敏事件,没有治疗相关肝肾功能损伤,谷丙转氨酶、谷草转氨酶、血尿素氮和血清肌酐在正常范围内保持稳定。
尽管总体受试者12周时的ADAS-cog和MoCA-B评分没有显著变化,但按给药剂量分层后,不同剂量组的认知量表评分变化不一致。中等剂量组受试者的ADAS-cog评分表现出持续下降趋势,12周时,较基线下降2.33,MoCA-B评分增加2.38,表明认知表现更好,然而,高剂量组的简易精神状态量表(MMSE)评分几乎没有增加。
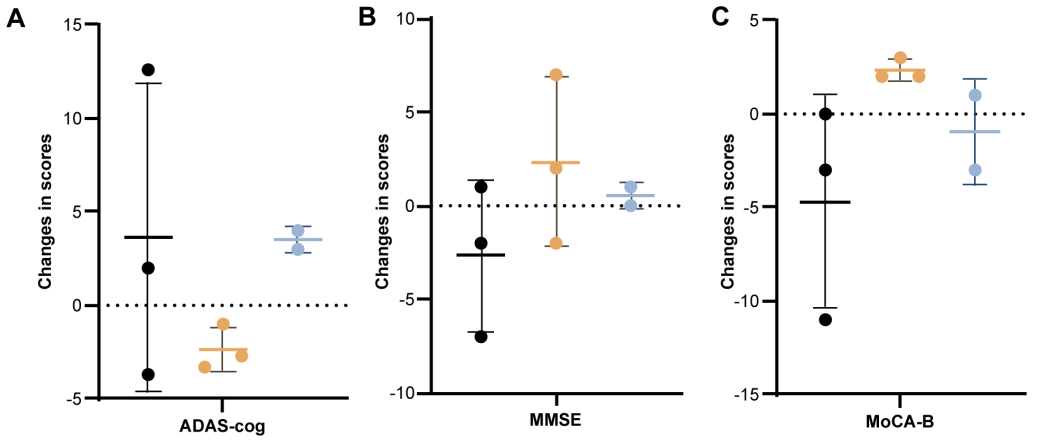
低(黑)、中(黄)、高(蓝)剂量组受试者的ADAS-cog(A)、MMSE(B)和MoCA-B(C)评分
此外,根据神经精神病学量表(NPI),中等剂量组受试者的护理人员神经精神症状导致的痛苦评分下降了5.33,但受试者的神经精神症状并未改善,甚至有恶化趋势,不过受试者的阿尔茨海默病协作研究日常生活活动量表(ADCS-ADL)评分呈上升趋势,日常生活活动量表(ADL)评分呈下降趋势,表明,日常生活能力有所改善。
随访期间,至36周,中等剂量组的ADAS-cog评分持续下降3.98分,MMSE和MoCA评分保持相对稳定。这表明,ahaMSCs-Exos治疗具有长尾效应。MMSE和MOCA评分表明,低剂量和高剂量组尽管在干预或随访后恢复了常规药物治疗,但认知功能均恶化。ADL评分的变化趋势一定程度上和认知功能的变化趋势一致。
随访期间,AD病理标志的ATN谱(Aβ、tau和神经变性)中,Aβ在第一次治疗后约1年增加,但有1例受试者例外,Aβ沉积明显减少,三个剂量组之间没有显著差异,tau沉积没有明显变化,中等剂量组的左海马体积减少0.118,低和高剂量组分别减少0.213和0.181,右海马体积变化类似,虽然中等剂量组的减少更少,但未达到统计学显著性。
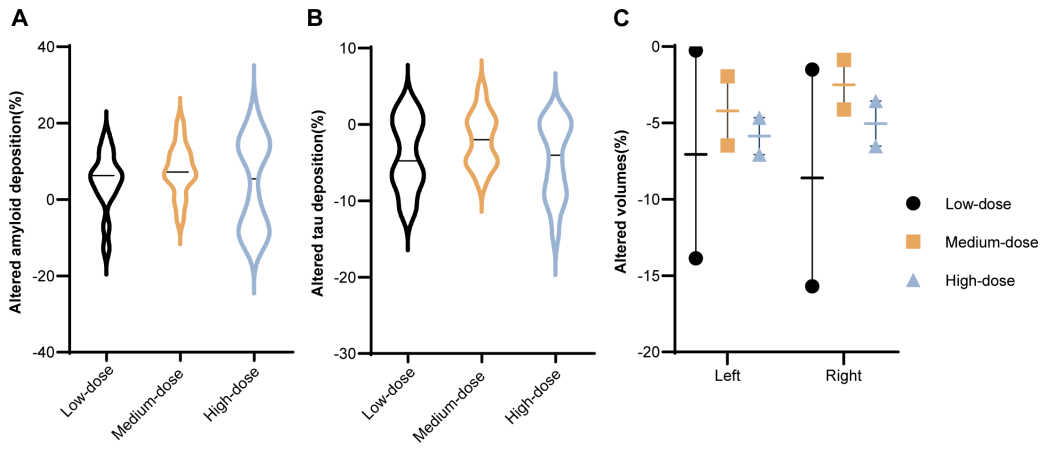
低(黑)、中(黄)、高(蓝)剂量组受试者的Aβ(A)、tau(B)和双侧海马体积(C)变化
综上所述,这项临床试验证明了ahaMSCs-Exos的安全性,所有受试者可耐受一周两次的经鼻给药,至少可选择4×108剂量进行更大规模的多中心临床试验。在下一阶段的临床试验中,应扩大样本量、设置对照组和更严格的纳入标准、延长干预阶段,以及增加外周血的成像和生物标志物轨迹评估。
参考文献:
[1] Xie X, Song Q, Dai C, et al. Clinical safety and efficacy of allogenic human adipose mesenchymal stromal cells-derived exosomes in patients with mild to moderate Alzheimer’s disease: a phase I/II clinical trial[J]. General Psychiatry, 2023, 36(5).
[2] Dinkins M B, Wang G, Bieberich E. Sphingolipid-enriched extracellular vesicles and Alzheimer’s disease: a decade of research[J]. Journal of Alzheimer's Disease, 2017, 60(3): 757-768.
[3] Harrell C R, Fellabaum C, Jovicic N, et al. Molecular mechanisms responsible for therapeutic potential of mesenchymal stem cell-derived secretome[J]. Cells, 2019, 8(5): 467.
[4] Ma X, Huang M, Zheng M, et al. ADSCs-derived extracellular vesicles alleviate neuronal damage, promote neurogenesis and rescue memory loss in mice with Alzheimer's disease[J]. Journal of Controlled Release, 2020, 327: 688-702.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


