《科学·转化医学》:早期阿尔茨海默病患者神经元的“能量工厂”就存在功能障碍!
来源:奇点糕 2022-09-27 10:40
阿尔茨海默病是最常见的神经退行性疾病,其主要症状为认知和记忆的缺失,以及社交能力和机体功能的减退,通常会在疾病病理积累到一定程度才会表现。
阿尔茨海默病是最常见的神经退行性疾病,其主要症状为认知和记忆的缺失,以及社交能力和机体功能的减退,通常会在疾病病理积累到一定程度才会表现。在阿尔茨海默病的研究中,最经典的病理标志物是淀粉样蛋白和tau蛋白沉积[1-3],由此也衍生出了最为主流的两种关于阿尔茨海默病的假说。但针对这两种蛋白和假说所研发的药物,在临床试验中屡屡折戟。因此,科学家们开始重新思考各个假说和疾病的因果关系,并将目光移向了更加早期的细胞活动。
相比起早期集中在淀粉样蛋白和tau蛋白沉积本身,近期更多的研究转向了影响两种病理蛋白形成的细胞机制。线粒体作为细胞中的“能量工厂”,其功能障碍在包括阿尔茨海默病在内的许多疾病病理中扮演着重要的角色[4]。但在阿尔茨海默病中,线粒体损伤和其他已被发现的病理机制的关系却并不明确。
近期一篇由帝国理工和剑桥大学学者们发表在Science Translational Medicine上的研究,为早期阿尔茨海默病中广泛存在的线粒体损伤和内质网应激,与神经元突触缺失的关系提供了体内影像学证据[5]。

越来越多的研究和学者们认为,阿尔茨海默病的发生和发展,与脑内细胞的代谢功能是否健全有重要的关系。而早期阿尔茨海默病的特点之一,是虽然代谢功能障碍在各个脑区广泛存在,但其病理标志物存在着区域选择性。这是不同脑区对疾病敏感程度不一样的结果,也由不同脑区的联通方式、功能活动和代谢机制决定。
多年来,阿尔茨海默病治疗的难点之一,在于疾病早期,由于大脑具有一定的可塑性和功能储备能力,所以尽管存在一些代谢功能障碍,病人依旧能够保持正常的认知水平。因此在认知水平出现下降时再进行治疗,有可能已经错过了最优的治疗时间。所以确定阿尔茨海默病早期的代谢病理过程,可以给后续的治疗提供新的思路和优先选项。
在这项研究中,研究人员招募了12位早期散发型阿尔茨海默病患者作为试验组,以及16位认知正常的志愿者作为对照组,对他们进行了12-18个月的随访。在试验期间,研究通过正电子发射断层扫描(PET),对受试者脑内的线粒体复合物I(MC1),内质网应激标志物(S1R)和突触前囊泡蛋白(SV2A)进行放射性同位素标记,来确认各个标志物在疾病进程中的变化以及相互关系。并且通过核磁共振(MRI)对受试者进行脑部影像扫描,以得到全脑及各个脑区体积随试验标志物和疾病进程的变化。
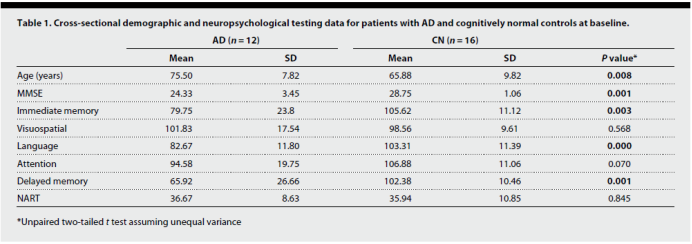
受试患者和健康志愿者的基本信息
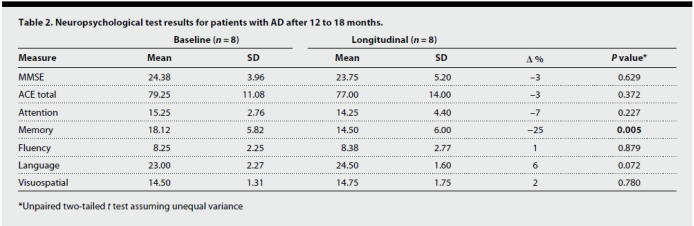
阿尔茨海默病患者12-18个月随访后在精神认知能力测试中的变化
研究通过各个脑区的横向对比和疾病个体的纵向分析后发现,相比于健康志愿者,阿尔茨海默病患者的脑体积出现了显著缩小,其中海马体和颞叶的缩小比例达到了23%和16%(P<0.001)。
随着脑体积的减小,患者的脑血流量也随之降低,与健康对照组相比,各个脑区的脑血流量减少在8%到26%之间。脑血流量减少的最大的脑区分别是海马体(-20%,P=0.023)和丘脑(-26%,P=0.044)。
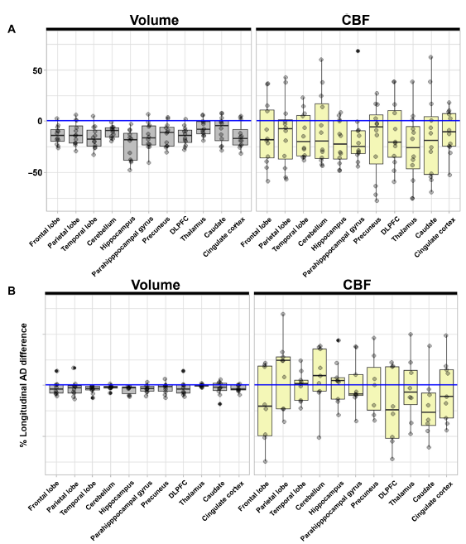
不同脑区中脑体积和脑血流量(CBF)在阿尔茨海默病患者和健康受试者之间的表达差异(A);以及在阿尔茨海默病患者纵向分析中的表达差异(B)
研究结果显示S1R在阿尔茨海默病病人的各个脑区内有显著的升高。但在该研究中,关于S1R表达量升高的发现与之前已发表的一些研究存在一定的差异。据研究人员解释是因为之前的研究中,试验对象使用了一些阻断S1R和SA4503结合的药物,并且试验在配体和受体的选择上有所不同[7-8]。
内质网作为细胞中的细胞器,其相关蛋白的表达也与细胞数量紧密相关。而在阿尔茨海默病中后期,随着疾病病理的累积,大量的锥体细胞死亡,因此研究人员也认为,S1R的表达量会在疾病初期升高然后随疾病进程降低。
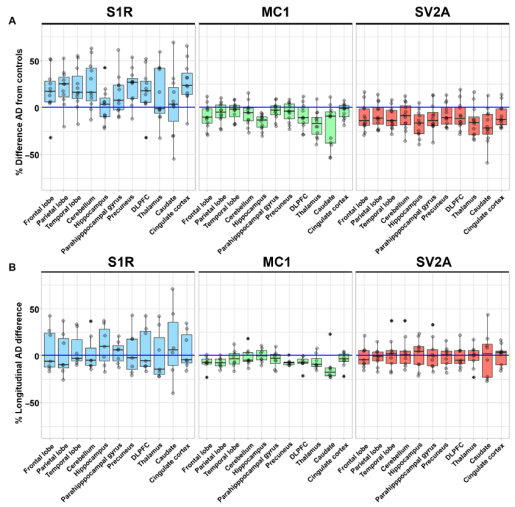
不同脑区中S1R,MC1和SV2A在阿尔茨海默病患者和健康受试者之间的表达差异(A);以及在阿尔茨海默病患者纵向分析中的表达差异(B)
同为细胞中的细胞器,线粒体和内质网在疾病中的重要联系也一直为科学家们所重视。在线粒体中存在着对细胞有氧呼吸至关重要的呼吸链,这条呼吸链由五个复合物组成。MC1是呼吸链中的第一个复合物,它关系到整条呼吸链的工作的顺利进行,因此它的表达也是线粒体功能是否完整的一个重要标志。
研究发现在S1R表达上调的同时,MC1在早期阿尔茨海默病患者的脑中大大减少,在对疾病病理敏感的脑区如海马体(-25%,P=0.02)、丘脑(-23%,P=0.001)和尾状核(-28%,P=0.02),这种变化尤为显著。研究人员猜测,S1R表达上调可能是对线粒体损伤做出的适应性反应。
但研究同时也发现,MC1的减少与阿尔茨海默病中脑血流量的减少并不相关,意味着在早期阿尔茨海默病中,线粒体功能障碍与脑灌注损伤并没有直接联系。在健康对照组中,线粒体的氧化磷酸化和突触分布呈正相关的关系,而在阿尔茨海默病患者中,这一关联并没有被发现,意味着这一通路可能因为疾病发生而失调。
突触缺失是伴随着阿尔茨海默病发生的一个重要病理现象。细胞的树突减少和损伤也被认为与淀粉样蛋白水解产物的毒性有关。试验结果发现在早期阿尔茨海默病患者的大脑中,随着疾病进程的发展,病人的脑体积减小,S1R的升高和MC1的降低,突触前囊泡结合蛋白SV2A的表达也大大降低。减少量最大的区域分别在尾状核(-25%,P=0.07),海马体(-24%,P=0.001)和丘脑(-19%,P=0.012)。但SV2A表达降低在疾病进程中发生的具体时间,和其与疾病进程的速率关系还有待细究。
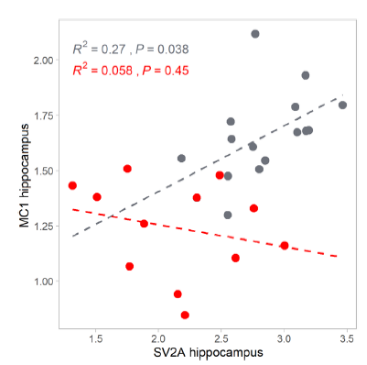
阿尔茨海默病患者(红线)和健康志愿者(灰线)海马体中MC1和SV2A表达变化的关系
该研究是一项体内多模型的分子标志物试验,发现了在早期阿尔茨海默病脑内广泛地存在着升高的氧化应激反应。虽然这项研究仍存在一些局限性和不足,比如样本量较少以及标志物单一,但其结果为早期阿尔茨海默病脑内线粒体氧化应激和内质网应激的关系提供了重要证据。
而这项研究也证明了虽然存在脑区差异,但阿尔茨海默病中的细胞应激是广泛存在于各个脑区的。相较针对特定脑区的研究,这项研究为之后阿尔茨海默病的治疗和早期干预,提供了更多的潜在的病理机制和靶点。
在群雄逐鹿的阿尔茨海默病研究领域,疾病初期体内研究的证据不仅能帮助研究者们更好地了解发病机制,还能为疾病的早筛和预防提供潜在的参考和标志物,让大家有更多应对阿尔茨海默病的时间和治疗策略。
参考资料:
[1] Hardy J, Allsop D. Amyloid deposition as the central event in the aetiology of Alzheimer's disease. Trends Pharmacol Sci. 1991;12(10):383-388. doi:10.1016/0165-6147(91)90609-v [2] Hardy JA, Higgins GA. Alzheimer's disease: the amyloid cascade hypothesis. Science. 1992;256(5054):184-185. doi:10.1126/science.1566067
[3] Scheltens P, De Strooper B, Kivipelto M, et al. Alzheimer's disease. Lancet. 2021;397(10284):1577-1590. doi:10.1016/S0140-6736(20)32205-4 [4] Tönnies E, Trushina E. Oxidative Stress, Synaptic Dysfunction, and Alzheimer's Disease. J Alzheimers Dis. 2017;57(4):1105-1121. doi:10.3233/JAD-161088
[5] Venkataraman AV, Mansur A, Rizzo G, et al. Widespread cell stress and mitochondrial dysfunction occur in patients with early Alzheimer's disease. Sci Transl Med. 2022;14(658):eabk1051. doi:10.1126/scitranslmed.abk1051
[6] Mishina M, Ohyama M, Ishii K, et al. Low density of sigma1 receptors in early Alzheimer's disease. Ann Nucl Med. 2008;22(3):151-156. doi:10.1007/s12149-007-0094-z
[7] Hedskog L, Pinho CM, Filadi R, et al. Modulation of the endoplasmic reticulum-mitochondria interface in Alzheimer's disease and related models. Proc Natl Acad Sci U S A. 2013;110(19):7916-7921. doi:10.1073/pnas.1300677110
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


