J Immunother Cancer:新突破!靶向Eva1的CAR-T细胞在实体瘤治疗中或能发挥巨大潜力
来源:生物谷原创 2025-06-13 14:13
研究结果表明,人源化的Eva1 CAR-T细胞在体外对Eva1阳性肿瘤细胞具有高度的特异性,且能够有效增殖和分泌细胞因子。
在抗癌领域,CAR-T细胞疗法如同一把锐利的剑,已经成功斩断了血液肿瘤的魔爪,然而,面对更为复杂的实体瘤,这把剑似乎失去了往日的锋芒。近年来,科学家们对实体瘤治疗新方法的探讨如火如荼,同时他们也在不断探索新的靶点和优化策略旨在让CAR-T细胞疗法在实体瘤治疗中大放异彩。
近日,一篇发表在国际杂志Journal for ImmunoTherapy of Cancer上题为“Development and optimization of Eva1 (MPZL2) targeting chimeric antigen receptor T cells”的研究报告中,来自名古屋大学医学院等机构的科学家们通过研究为实体瘤的CAR-T细胞治疗带来了新的曙光,文章中,研究人员成功开发了靶向Eva1(MPZL2)的CAR-T细胞,并在多种实体瘤模型中展示了其显著的治疗效果,这一发现无疑为实体瘤患者带来了新的希望。
文章中,研究人员首次将Eva1作为CAR-T细胞疗法的靶点并成功展示了其在实体瘤治疗中的潜力。Eva1是一种在多种实体瘤中高度表达的蛋白,但在正常组织中表达较低,这使得其成为CAR-T细胞疗法的理想靶点,研究者通过开发靶向Eva1的CAR-T细胞为实体瘤患者提供一种新的、有效的治疗手段。
研究中的实验对象包括多种人源肿瘤细胞系、异种移植小鼠模型以及健康志愿者的外周血单核细胞(PBMC),研究人员采用了基因工程技术构建人源化Eva1 CAR-T细胞,并利用流式细胞术、免疫组化、生物发光成像(BLI)等技术对CAR-T细胞的特异性、增殖能力、细胞因子分泌及体内外抗肿瘤效果进行了全面评估。
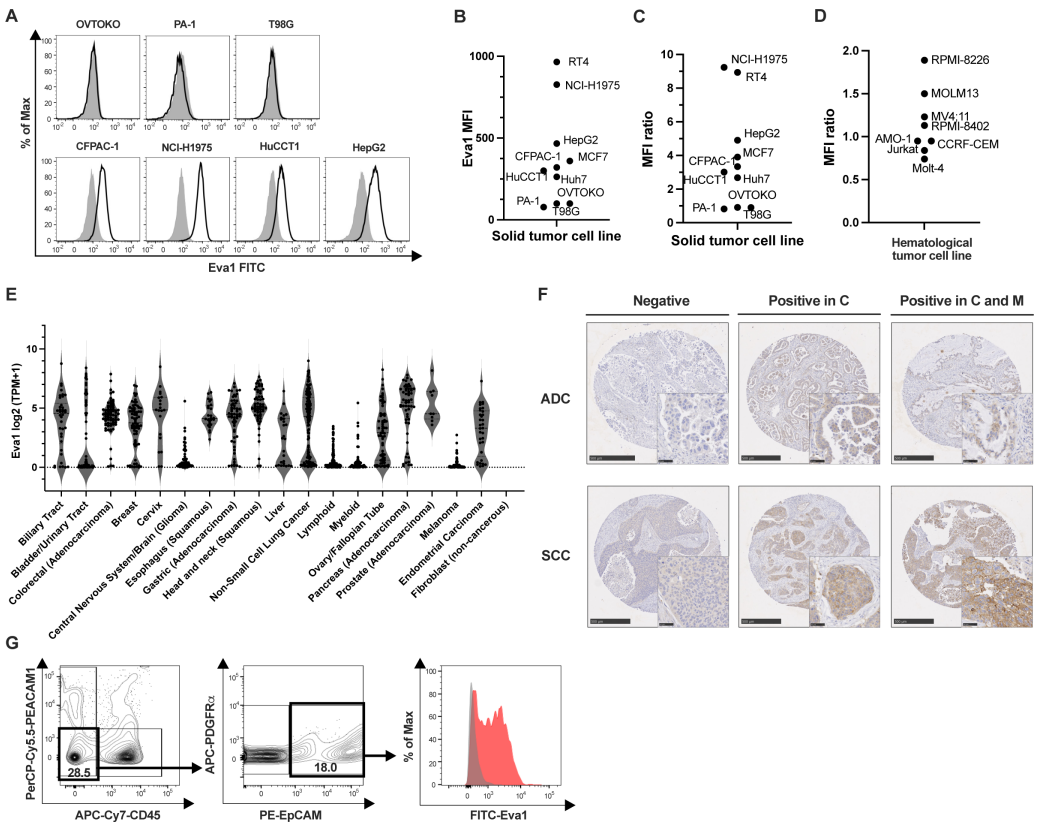
Eva1在多种肿瘤细胞系及原代肿瘤细胞中的表达
研究者首先通过基因工程技术构建了人源化Eva1 CAR-T细胞并对其进行优化,包括改变胞外间隔区的长度和胞内信号域的组合;随后他们利用流式细胞术和免疫组化技术验证了Eva1在多种肿瘤细胞系和临床样本中的表达情况,同时还在体外评估了Eva1 CAR-T细胞的特异性、增殖能力和细胞因子分泌情况,并通过异种移植小鼠模型验证了其体内抗肿瘤效果。最后,他们对Eva1 CAR-T细胞的安全性进行了初步评估。
研究结果表明,人源化的Eva1 CAR-T细胞在体外对Eva1阳性肿瘤细胞具有高度的特异性,且能够有效增殖和分泌细胞因子。在异种移植小鼠模型中,Eva1 CAR-T细胞展示了显著的抗肿瘤效果,能显著抑制肿瘤的生长并延长小鼠的生存期。通过优化胞外间隔区的长度和胞内信号域的组合或能进一步提高Eva1 CAR-T细胞的抗肿瘤效果。
相关研究结果为实体瘤的CAR-T细胞治疗提供了新的靶点和策略,文章中,研究人员成功开发了靶向Eva1的CAR-T细胞,并在多种实体瘤模型中展示了其显著的治疗效果。然而,尽管Eva1在正常组织中表达较低,但仍需进一步评估Eva1 CAR-T细胞的安全性从而确保其在临床应用中的安全性。在抗癌的征途中,CAR-T细胞疗法无疑是一股不可忽视的力量。然而面对实体瘤这一顽固的敌人,研究人员仍需不断探索新的靶点和优化策略。(生物谷Bioon.com)
参考文献:
Masahide Osaki,Seitaro Terakura,Shiho Hirano, et al. Development and optimization of Eva1 (MPZL2) targeting chimeric antigen receptor T cells, Journal for ImmunoTherapy of Cancer (2025). DOI:10.1136/jitc-2024-009825
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


