Mol Cancer Ther:发现小分子MMRi62诱导胰腺癌细胞死亡机制
来源:本站原创 2022-03-08 13:19
在一项新的研究中,来自美国罗斯威尔公园综合癌症中心、纽约州立大学和中国西安交通大学第二附属医院的研究人员发现了一种通过铁代谢途径抑制胰腺癌细胞生长和转移的分子。他们的研究结果为开发一种治疗胰腺癌的新候选药物铺平了道路。
2022年3月8日讯/生物谷BIOON/---在一项新的研究中,来自美国罗斯威尔公园综合癌症中心、纽约州立大学和中国西安交通大学第二附属医院的研究人员发现了一种通过铁代谢途径抑制胰腺癌细胞生长和转移的分子。他们的研究结果为开发一种治疗胰腺癌的新候选药物铺平了道路。相关研究结果近期发表在Molecular Cancer Therapeutics期刊上,论文标题为“Small Molecule MMRi62 Induces Ferroptosis and Inhibits Metastasis in Pancreatic Cancer via Degradation of Ferritin Heavy Chain and Mutant p53”。
这种称为MMRi62的分子靶向铁代谢以杀死癌细胞,并且还靶向促使它们生长和扩散的有害蛋白,这表明对这种化合物的进一步开发和完善可能导致一种新型的胰腺癌疗法。
论文通讯作者、罗斯威尔公园综合癌症中心药理学与治疗学系副教授Xinjiang Wang博士说,“MMRi62会导致一种叫做FTH1的储铁蛋白和一种在胰腺导管腺癌(PDAC)中发生突变的蛋白降解,从而抑制癌症转移和诱导铁死亡(ferroptosis),其中铁死亡是一种由细胞中的游离铁引发的细胞死亡形式。”
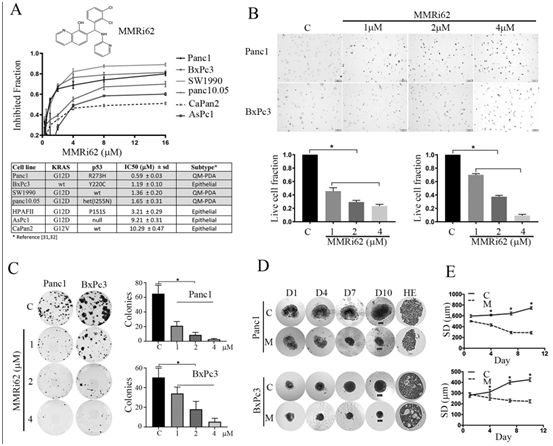
在(QM-PDA)胰腺癌亚型细胞株中,MMRi62选择性抑制增殖并诱导细胞死亡。图片来自Molecular Cancer Therapeutics, 2022, doi:10.1158/1535-7163.MCT-21-0728。
PDAC细胞容易发生铁死亡,这是最近发现的一种由铁引发的细胞死亡类型,已成为癌症研究的焦点。鉴定激活铁死亡的新型药物代表了PDAC潜在疗法的一个新领域,其中PDAC是一种侵袭性和基本无法治愈的疾病,占所有类型胰腺癌的90%。
PDAC的一个独特特征是KRAS和TP53基因发生突变,这两个突变的基因驱动疾病并使肿瘤对化疗产生抵抗性。由于靶向这些突变的药物和治疗方法尚未问世,PDAC患者的治疗选择有限,而且该疾病的5年生存率只有12%。
Wang博士补充说,“我们通过这项研究证实在临床前模型中,MMRi62能够诱导携带KRAS或TP53突变的PDAC细胞发生铁死亡,进而抑制肿瘤生长,防止肿瘤向远处器官转移。虽然目前没有铁死亡诱导剂,但我们希望我们的发现有望开发基于MMRi62的新治疗方法用于治疗诸如PDAC之类的顽固性癌症。”(生物谷 Bioon.com)
参考资料:
Junhui Li et al. Small Molecule MMRi62 Induces Ferroptosis and Inhibits Metastasis in Pancreatic Cancer via Degradation of Ferritin Heavy Chain and Mutant p53. Molecular Cancer Therapeutics, 2022, doi:10.1158/1535-7163.MCT-21-0728.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


