Nature:重大进展!揭示伴侣蛋白ClpB清理有毒蛋白聚集物机制
来源:本站原创 2020-02-04 22:49
2020年2月4日讯/生物谷BIOON/---细胞如何解开聚集在一起的蛋白?在一项新的研究中,来自荷兰国家原子分子研究所(AMOLF)和德国癌症研究中心的研究人员如今发现伴侣蛋白ClpB可强行拉开蛋白链中暴露的环状结构(loop),随后将它们从蛋白聚集物中拉取出来。相关研究结果于2020年1月29日在线发表在Nature期刊上,论文标题为“Processiv
2020年2月4日讯/生物谷BIOON/---细胞如何解开聚集在一起的蛋白?在一项新的研究中,来自荷兰国家原子分子研究所(AMOLF)和德国癌症研究中心的研究人员如今发现伴侣蛋白ClpB可强行拉开蛋白链中暴露的环状结构(loop),随后将它们从蛋白聚集物中拉取出来。相关研究结果于2020年1月29日在线发表在Nature期刊上,论文标题为“Processive extrusion of polypeptide loops by a Hsp100 disaggregase”。
蛋白是在体内进行折叠的氨基酸长链。它们在细胞中执行许多功能,但只有在它们正确折叠后才能做到这一点。但是,错误折叠可能会导致蛋白聚集物---类似于缠结物的蛋白团块---形成,可进一步破坏细胞。蛋白聚集与衰老、阿尔茨海默病和其他医学疾病有关。
ClpB是细胞中的分子清洁机
有机体为这些蛋白团块提供清理服务:一组称为伴侣蛋白的蛋白。众所周知,Hsp100伴侣蛋白家族可以重新溶解蛋白聚集物,而ClpB就是这个伴侣蛋白家族的一员。但是它的内在机制从未被直接测量过。面临的主要挑战是如何可视化观察所有这些蛋白及其运动,它们的运动在非常小的尺度(纳米)上发生,并且是高度随机的。
荷兰国家原子分子研究所的Mario Avellaneda和Sander Tans以及德国癌症研究中心的Bernd Bukau和Axel Mogk解决了这个问题。他们的研究揭示了这些伴侣蛋白如何解开这些聚集在一起的蛋白链。
Tans说,“我们发现环状的ClpB蛋白强行将蛋白链中的环状结构拉过它的中心孔。这些蛋白链中的环状结构存在于蛋白聚集物的表面上。但是,这些蛋白团块太大而无法通过这个中心孔。因此,通过这种拉动作用,ClpB可以从较大的蛋白聚集物中拉取出单个蛋白链。一旦移除,这个蛋白链可以再次折叠并正常发挥功能。通过一次一个地拉出所有蛋白,这种伴侣蛋白可以完全解开整个蛋白聚集物。”
用光进行拉取
这些研究人员通过使用光学镊子抓住蛋白链的两个末端来实现这一点。光学镊子是聚焦的激光束,可以捕获和操纵塑料圆形珠子或玻璃圆形珠子。尽管比蛋白大1000倍,他们却可以在一种蛋白链的两个末端连接这类珠子,从而非常精确地操纵它。通过以这种方式测量一种蛋白链的长度,他们可以知道它是被拉伸还是被压缩和折叠。
在将伴侣蛋白ClpB添加到一种被拉伸的蛋白链中之后,这些研究人员发现这种蛋白链的两个末端之间的距离逐渐变短,直到这两个末端紧挨着。这一令人惊人的观察结果表明这种蛋白链被拉着通过了环形的ClpB。他们认为,当这种蛋白链以环状结构穿过ClpB的中心孔时,它的两个末端确实会被拉在一起。其他实验也证实了这一想法。比如,当通过引入突变对这个中心孔的内部进行修饰时,类似马达的拉动活动被取消了。
可视化观察ClpB
这种蛋白链环状结构拉出从未在任何蛋白中观察到。因此,为了进一步进行测试,这些研究人员开发了一种不同的方法:通过将一种荧光分子连接到伴侣蛋白ClpB上来追踪这种伴侣蛋白如何在蛋白链上移动。最初,他们对此表示怀疑,这是因为这些运动比荧光成像所需的光波长要小。当这些微小的运动确实可见时,他们感到十分吃惊。
这些研究人员发现ClpB最初附着在一种被拉伸的蛋白链的随机位置上。ClpB随后可以将这种蛋白链的左末端拉向自身,也可以将它的右末端拉向自身,或者将它的两个末端拉向自身。这种蛋白链的环状结构的两个臂因此就可以同时被拉着通过环形的ClpB。Tans说,“我们知道将一根双线穿过针眼是多么困难。ClpB能够使用存在于中心孔中的称为孔环(pore loop)的微型驱动杆来实现这一壮举。通过使用细胞产生的ATP燃料分子,ClpB可以像小手指一样上下移动这些驱动杆。这接着使得氨基酸链穿过环形的ClpB。这些驱动杆的确切作用机制尚不清楚。但是,我们发现它们可以突然发作:首先,几个驱动杆连续推动,然后停顿,然后再次推动,等等。很可能需要停顿才能让新的ATP分子结合。”
快速而又高效
Tans说,关于这些ClpB解开蛋白聚集物的作用原理有许多相互矛盾的观点。“一种观点是,许多ClpB以随机的方式结合着蛋白聚集物的粘性部分,有点像溶解脂肪的肥皂分子。其他研究已表明一个蛋白链的一个片段最多只适合于ClpB通道,而且出于这种原因,这个蛋白链的环状结构并不适合。我们如今证实ClpB强行拉动。这种伴侣蛋白的作用原理就像是一个马达,通过拉动暴露的蛋白链环状结构来解开蛋白聚集物。它一直保持拉动直到这个蛋白链被完全拉出。”
Tans和他的同事们的下一步将是研究人伴侣蛋白和其他蛋白。诱人的是,这项研究有可能导致人们开发出治疗阿尔茨海默病的药物。Tans说,“原则上,你可以开始考虑这些事情。但是,在实践中,这远不那么简单。在开始进行临床应用之前,我们需要更好地了解这些分子清洁机器如何在细胞环境中发挥作用。下一步是研究ClpB如何受到调控,这是因为它也可能通过拉动正常蛋白而引起损害。”
Tans说,ClpB可以拉动蛋白链环状结构的事实表明其他蛋白可能也在其他细胞过程中做同样的事情。“比如,细胞持续降解受损的蛋白以产生新的蛋白,换句话说,这就是细胞的循环经济。这如今可以使用我们的方法进行研究。”(生物谷 Bioon.com)
参考资料:
1.Mario J. Avellaneda et al. Processive extrusion of polypeptide loops by a Hsp100 disaggregase. Nature, 2020, doi:10.1038/s41586-020-1964-y.
2.Molecular machine tears toxic protein clumps apart
https://phys.org/news/2020-01-molecular-machine-toxic-protein-clumps.html

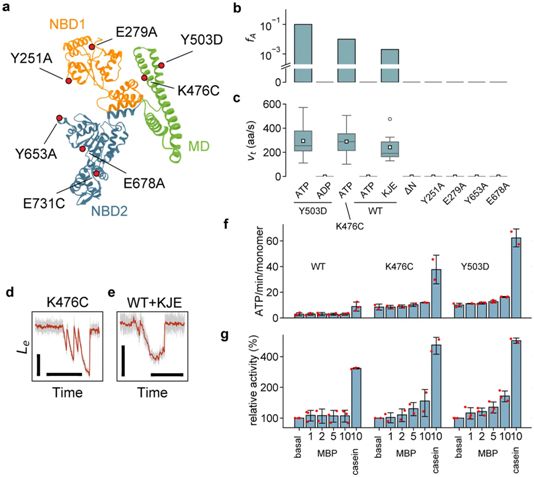
图片来自Nature, 2020, doi:10.1038/s41586-020-1964-y。
蛋白是在体内进行折叠的氨基酸长链。它们在细胞中执行许多功能,但只有在它们正确折叠后才能做到这一点。但是,错误折叠可能会导致蛋白聚集物---类似于缠结物的蛋白团块---形成,可进一步破坏细胞。蛋白聚集与衰老、阿尔茨海默病和其他医学疾病有关。
ClpB是细胞中的分子清洁机
有机体为这些蛋白团块提供清理服务:一组称为伴侣蛋白的蛋白。众所周知,Hsp100伴侣蛋白家族可以重新溶解蛋白聚集物,而ClpB就是这个伴侣蛋白家族的一员。但是它的内在机制从未被直接测量过。面临的主要挑战是如何可视化观察所有这些蛋白及其运动,它们的运动在非常小的尺度(纳米)上发生,并且是高度随机的。
荷兰国家原子分子研究所的Mario Avellaneda和Sander Tans以及德国癌症研究中心的Bernd Bukau和Axel Mogk解决了这个问题。他们的研究揭示了这些伴侣蛋白如何解开这些聚集在一起的蛋白链。
Tans说,“我们发现环状的ClpB蛋白强行将蛋白链中的环状结构拉过它的中心孔。这些蛋白链中的环状结构存在于蛋白聚集物的表面上。但是,这些蛋白团块太大而无法通过这个中心孔。因此,通过这种拉动作用,ClpB可以从较大的蛋白聚集物中拉取出单个蛋白链。一旦移除,这个蛋白链可以再次折叠并正常发挥功能。通过一次一个地拉出所有蛋白,这种伴侣蛋白可以完全解开整个蛋白聚集物。”
用光进行拉取
这些研究人员通过使用光学镊子抓住蛋白链的两个末端来实现这一点。光学镊子是聚焦的激光束,可以捕获和操纵塑料圆形珠子或玻璃圆形珠子。尽管比蛋白大1000倍,他们却可以在一种蛋白链的两个末端连接这类珠子,从而非常精确地操纵它。通过以这种方式测量一种蛋白链的长度,他们可以知道它是被拉伸还是被压缩和折叠。
在将伴侣蛋白ClpB添加到一种被拉伸的蛋白链中之后,这些研究人员发现这种蛋白链的两个末端之间的距离逐渐变短,直到这两个末端紧挨着。这一令人惊人的观察结果表明这种蛋白链被拉着通过了环形的ClpB。他们认为,当这种蛋白链以环状结构穿过ClpB的中心孔时,它的两个末端确实会被拉在一起。其他实验也证实了这一想法。比如,当通过引入突变对这个中心孔的内部进行修饰时,类似马达的拉动活动被取消了。
可视化观察ClpB
这种蛋白链环状结构拉出从未在任何蛋白中观察到。因此,为了进一步进行测试,这些研究人员开发了一种不同的方法:通过将一种荧光分子连接到伴侣蛋白ClpB上来追踪这种伴侣蛋白如何在蛋白链上移动。最初,他们对此表示怀疑,这是因为这些运动比荧光成像所需的光波长要小。当这些微小的运动确实可见时,他们感到十分吃惊。
这些研究人员发现ClpB最初附着在一种被拉伸的蛋白链的随机位置上。ClpB随后可以将这种蛋白链的左末端拉向自身,也可以将它的右末端拉向自身,或者将它的两个末端拉向自身。这种蛋白链的环状结构的两个臂因此就可以同时被拉着通过环形的ClpB。Tans说,“我们知道将一根双线穿过针眼是多么困难。ClpB能够使用存在于中心孔中的称为孔环(pore loop)的微型驱动杆来实现这一壮举。通过使用细胞产生的ATP燃料分子,ClpB可以像小手指一样上下移动这些驱动杆。这接着使得氨基酸链穿过环形的ClpB。这些驱动杆的确切作用机制尚不清楚。但是,我们发现它们可以突然发作:首先,几个驱动杆连续推动,然后停顿,然后再次推动,等等。很可能需要停顿才能让新的ATP分子结合。”
快速而又高效
Tans说,关于这些ClpB解开蛋白聚集物的作用原理有许多相互矛盾的观点。“一种观点是,许多ClpB以随机的方式结合着蛋白聚集物的粘性部分,有点像溶解脂肪的肥皂分子。其他研究已表明一个蛋白链的一个片段最多只适合于ClpB通道,而且出于这种原因,这个蛋白链的环状结构并不适合。我们如今证实ClpB强行拉动。这种伴侣蛋白的作用原理就像是一个马达,通过拉动暴露的蛋白链环状结构来解开蛋白聚集物。它一直保持拉动直到这个蛋白链被完全拉出。”
Tans和他的同事们的下一步将是研究人伴侣蛋白和其他蛋白。诱人的是,这项研究有可能导致人们开发出治疗阿尔茨海默病的药物。Tans说,“原则上,你可以开始考虑这些事情。但是,在实践中,这远不那么简单。在开始进行临床应用之前,我们需要更好地了解这些分子清洁机器如何在细胞环境中发挥作用。下一步是研究ClpB如何受到调控,这是因为它也可能通过拉动正常蛋白而引起损害。”
Tans说,ClpB可以拉动蛋白链环状结构的事实表明其他蛋白可能也在其他细胞过程中做同样的事情。“比如,细胞持续降解受损的蛋白以产生新的蛋白,换句话说,这就是细胞的循环经济。这如今可以使用我们的方法进行研究。”(生物谷 Bioon.com)
参考资料:
1.Mario J. Avellaneda et al. Processive extrusion of polypeptide loops by a Hsp100 disaggregase. Nature, 2020, doi:10.1038/s41586-020-1964-y.
2.Molecular machine tears toxic protein clumps apart
https://phys.org/news/2020-01-molecular-machine-toxic-protein-clumps.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


