怪不得发烧生病后不想社交!Cell:大脑中缝背核神经元是"幕后推手",IL-1β 信号解锁行为密码
来源:生物谷原创 2025-11-29 09:25
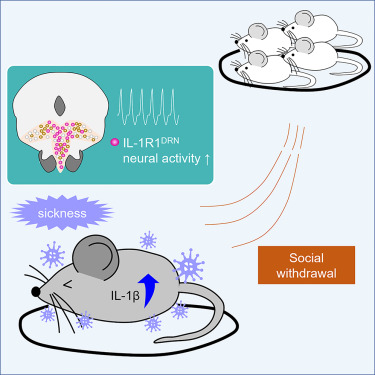
免疫系统分泌的细胞因子白细胞介素-1β(IL-1β),会精准结合大脑中缝背核(DRN)神经元上的 IL-1R1 受体,激活其与中间外侧隔膜(LSI)的神经连接,从而主动抑制社交行为。
生病时总爱独处、拒绝社交,这不是性格孤僻,而是身体的进化性保护机制——既避免病菌传播,也为康复保留能量。但这种行为改变背后,免疫系统与大脑如何协同运作一直是未解之谜。
近日,麻省理工学院皮考尔学习与记忆研究所的科学家团队在《细胞》杂志发表的突破性研究,终于揭开了这一谜底:免疫系统分泌的细胞因子白细胞介素-1β(IL-1β),会精准结合大脑中缝背核(DRN)神经元上的 IL-1R1 受体,激活其与中间外侧隔膜(LSI)的神经连接,从而主动抑制社交行为。这一发现完美解释了 “病来如山倒,社交兴致无” 的生理本质,也为理解免疫与神经的跨界沟通提供了全新视角。

社交互动是物种生存的基础,但也伴随着病菌传播风险。进化过程中,动物逐渐形成了 “生病即隔离” 的适应性行为,但这种行为是主动选择还是因病虚弱的被动结果,长期存在争议。
麻省理工学院皮考尔研究所和脑与认知科学系副教授 Gloria Choi、哈佛医学院免疫学副教授 Jun Huh 带领团队,通过一系列精准实验证实:免疫激活后的社交隔离是 “自我施加” 的主动行为,由特定神经通路驱动,而非乏力、发热等生理症状的附带产物。这一结论打破了 “生病少社交只是身体虚弱” 的固有认知,揭示了免疫系统与神经系统跨系统调控行为的精妙机制。
为找到驱动社交回避的核心分子,研究团队向小鼠大脑注射了 21 种不同细胞因子,模拟感染时的免疫激活状态,并与注射脂多糖(LPS,模拟细菌感染)的小鼠行为对比。
结果显示,只有 IL-1β 能完全重现 LPS 引发的社交回避——小鼠会主动远离同伴,更倾向于待在无社交对象的区域;同时,IL-1β 也会导致小鼠倦怠,但后续实验证明,社交回避与倦怠是两条独立通路调控的行为,互不干扰。进一步研究发现,IL-1β 的作用依赖其受体 IL-1R1,而全脑筛查显示,IL-1R1 在中缝背核(DRN)神经元中高度富集——这一脑区不仅已知调控社交行为,还紧邻大脑导水管,能直接接触脑脊液中的细胞因子,成为免疫信号进入大脑的 “门户”。
深入分析表明,中缝背核中表达 IL-1R1 的神经元,绝大多数是合成血清素的神经元,而血清素本身就是调控社交、情绪的关键神经递质。实验证实,IL-1β 会直接激活这些神经元:通过纤维光度法检测到,IL-1β 注射后,DRN 神经元的钙信号迅速升高,且持续激活;而通过化学遗传学技术激活这些神经元,即便没有感染,小鼠也会出现明显社交回避。反之,抑制这些神经元的活动,或基因敲除其 IL-1R1 受体,能有效阻断 IL-1β 或 LPS 诱导的社交回避,但不会改变小鼠的倦怠状态,这清晰证明,社交回避是 IL-1β-IL-1R1-DRN 通路调控的特异性行为,与身体虚弱无关。
为追踪完整神经环路,团队通过病毒标记和光遗传学技术,绘制了 DRN 神经元的下游投射图谱。结果发现,DRN 神经元会投射到多个调控社交的脑区,但只有激活其与中间外侧隔膜(LSI)的连接时,才会引发社交回避,且这种激活不影响小鼠的运动能力,进一步验证了该环路的特异性。
更关键的是,在沙门氏菌感染的小鼠模型中,这一通路同样被激活,小鼠表现出明显社交隔离,而抑制 DRN 神经元或敲除 IL-1R1 后,社交行为可显著恢复,证明该机制在真实感染场景中同样成立。
研究还发现,IL-1β 的来源具有双重性:外周免疫细胞分泌的 IL-1β 可启动信号,而大脑内小胶质细胞分泌的 IL-1β 会形成 “自我强化环路”,维持社交回避行为直至感染消退。这一设计确保了行为调控的持续性,让动物在康复前持续保持隔离状态,最大化降低传播风险。此外,实验排除了体温升高对社交行为的影响——IL-1β 诱导的发热与社交回避在时间上不同步,且抑制 DRN 神经元可阻断社交回避但不影响体温,说明二者是独立的生理调控过程。
这项研究不仅解开了生病后社交意愿下降的分子神经机制,更揭示了免疫系统与神经系统跨界协作的精准模式。未来,这一发现可能为多种疾病的行为干预提供新思路:比如通过调控 IL-1β-IL-1R1 通路,帮助自身免疫病患者改善社交功能,或为感染后的情绪低落提供靶向干预方向。
同时,研究也留下了新的探索空间:中缝背核的 IL-1R1 神经元是否调控食欲减退、睡眠改变等其他疾病行为?血清素在社交回避中扮演何种具体角色?这些问题的解答,将进一步完善我们对 “疾病行为” 的全面理解。(生物谷Bioon.com)
参考文献:
Liu Yang et al, IL-1R-positive dorsal raphe neurons drive self-imposed social withdrawal in sickness, Cell (2025). DOI: 10.1016/j.cell.2025.10.040.
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->





