Cell:你的心脏是左派还是右派?心脏血管的"左右抉择"
来源:生物探索 2025-03-13 09:00
研究团队利用美国退伍军人事务部的百万退伍军人计划(Million Veteran Program)数据库,完成了迄今最大规模的冠状动脉解剖基因组研究(GWAS)。
为什么每个人的心脏血管走向如同指纹般独一无二?这个困扰医学界的解剖学谜题,3月5日被斯坦福大学研究团队揭开了关键一角。通过对6.1万名退伍军人的基因图谱解密,研究团队发现了一个名为CXCL12的"血管导航基因",它像GPS般精准指导着胚胎期冠状动脉的布局——这项发表于《Cell》的突破性研究“CXCL12 drives natural variation in coronary artery anatomy across diverse populations”,不仅解开了心脏发育的密码,更可能彻底改变心血管疾病的防治策略。
数据显示,80%人群的冠状动脉呈"右优势型",但仍有20%的人因血管走向差异面临独特的健康风险。这种解剖变异曾被归因于随机发育,但新研究证明:我们的DNA中早已写就血管的"生长路线图"。当研究人员将目光投向人类胚胎心脏,发现CXCL12在孕13周便活跃于心肌细胞之间,如同化学信号灯般引导血管内皮细胞定向迁移。更惊人的是,携带特定基因变异的人群,其左优势型风险可升高46%,这种遗传效应在欧裔、非裔人群中高度一致。
这项发现的意义远超解剖学范畴——CXCL12基因座竟与冠状动脉疾病风险区域重叠!这意味着,先天血管布局与后天心脏病风险共享着相同的遗传开关。当研究人员在小鼠心脏中敲除这个基因,血管果然"迷路"偏移;而补充CXCL12蛋白后,梗死心脏竟自发长出新的"生物搭桥"。这些发现暗示:未来或可通过调控发育基因,实现"从胚胎到老年"的全周期心血管保护。此刻,我们正站在改写心血管医学史的门槛上,一个通过基因密码优化心脏"生命线"的新纪元即将开启……

你的心脏里藏着一套精密的"高速公路系统"——冠状动脉网络。这些血管负责为心肌输送氧气,它们的走向直接影响着心脏的健康状态。斯坦福大学团队在《细胞》杂志发表的重磅研究,首次揭示了决定这条"生命线"走向的遗传密码:一个名为CXCL12(C-X-C motif chemokine ligand 12)的神秘基因。
心脏里的"交通规则":80%人都不知道的解剖秘密
当我们讨论心脏健康时,很少有人注意到一个惊人的解剖学事实:每个人心脏后壁的供血方式存在天然差异。在医学上,这种差异被称为"冠状动脉优势型(coronary dominance)"。具体来说:
右优势型(Right dominance):后降动脉(PDA)来自右冠状动脉(RCA),约占80%
左优势型(Left dominance):后降动脉来自左回旋支(LCx),约占10%
共同优势型(Co-dominance):左右冠状动脉共同参与供血,占剩余10%
这种解剖差异就像指纹一样独特,但直到现在,研究人员都不清楚这种"血管走位"是如何在胚胎发育过程中被决定的。斯坦福团队通过对6.1万名退伍军人的基因分析发现,这种差异竟与我们的DNA密切相关——特别是CXCL12这个基因。
基因侦探行动:61,043人的血管"地图"揭秘
研究团队利用美国退伍军人事务部的百万退伍军人计划(Million Veteran Program)数据库,完成了迄今最大规模的冠状动脉解剖基因组研究(GWAS)。这项"基因侦探"行动有几个关键发现:
中度遗传性:冠状动脉优势型的遗传度约为27.7%,说明基因确实在血管走向中扮演重要角色
10个关键基因位点:在全基因组范围内发现10个显著相关区域
跨种族验证:CXCL12基因在欧裔(EUR)和非裔(AFR)人群中都显示出最强关联
剂量效应:携带特定基因变异者,左/共同优势型的发生风险增加25-46%
特别值得注意的是,在宾夕法尼亚大学生物样本库(PMBB)的独立验证中,CXCL12附近的rs559580位点与左/共同优势型的关联强度达到惊人的46%(p=6.7×10^-5),完美复现了主研究的发现。
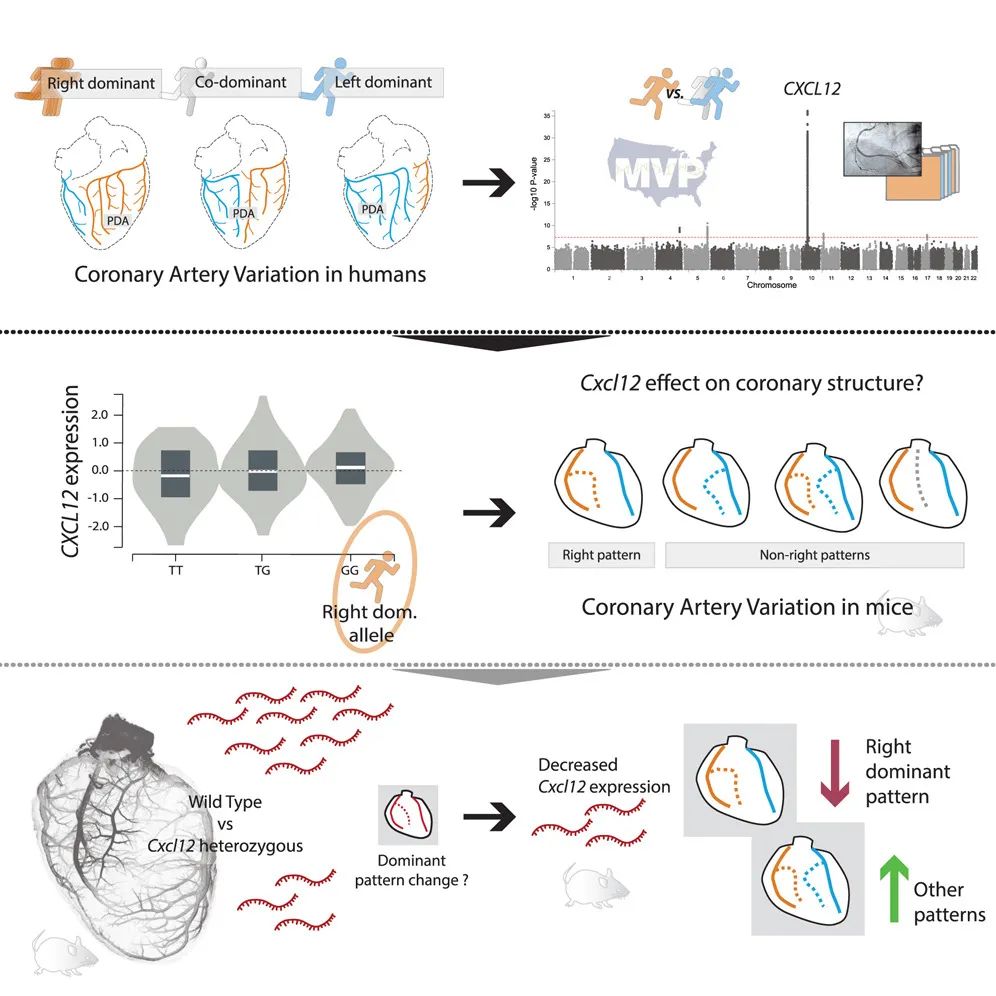
模式图(Credit: Cell)
CXCL12:胚胎心脏里的"血管导航员"
这个神秘基因CXCL12究竟有什么魔力?研究团队通过多维度证据揭示:
时空特异性表达:在人类胚胎心脏(孕13-22周)的冠状动脉形成关键期,CXCL12在心肌细胞、心外膜衍生细胞中活跃
配体-受体定位:其受体CXCR4(C-X-C chemokine receptor type 4)在血管内皮细胞高表达
三维空间信号:单细胞测序显示,CXCL12+细胞环绕在CXCR4+动脉周围,形成精确的化学梯度
基因剂量效应:小鼠实验证明,Cxcl12杂合敲除导致室间隔动脉(SpA)向左偏移,右优势型比例从79%降至58%
就像GPS导航引导车辆行驶路线,CXCL12通过化学信号引导血管内皮细胞的迁移方向。当这个基因的表达量降低时,原本应该沿右心室肌小梁延伸的血管,就会"迷路"转向左侧。
从DNA到血管:基因变异的精妙调控
研究团队深入解析了CXCL12区域的遗传密码,发现了三个独立的调控元件:
rs115213152位点:破坏KLF(Kruppel-like factor)转录因子结合,可能影响血流响应
rs5784627位点:干扰bZIP家族(如JUN/FOS)的DNA结合能力
rs559580位点:与冠状动脉疾病(CAD)风险位点rs649192高度连锁(r²=0.92)
通过深度学习模型分析胚胎心脏的染色质开放区域,研究人员发现这些变异都位于关键的调控区域。当这些"基因开关"发生改变时,CXCL12的表达水平就会下降,导致血管无法准确"感知"生长方向。
双重身份:同一个基因影响先天结构和后天疾病
惊人的是,CXCL12基因座与冠状动脉疾病(CAD)存在显著共定位:
共享变异:rs649192等位基因同时关联血管走向和动脉粥样硬化风险
双重机制:可能通过发育期血管布局和成年期血管修复双重途径影响心脏健康
临床启示:左优势型可能具有"双刃剑"效应——既改变血流动力学,又影响侧支循环建立
这解释了为什么某些冠心病患者更容易发生心肌梗死:如果优势血管同时是病变血管,侧支代偿能力将大打折扣。而CXCL12正是连接这两个过程的关键枢纽。
小鼠心脏里的"基因改造实验"
为验证这一发现,研究人员在模式生物中进行了精妙实验:
Cxcl12杂合小鼠:心脏CXCL12表达量降低50%
室间隔动脉改变:右优势型比例从79%降至58%,共同优势型从18%升至28%
发育时间窗:胚胎14.5-17.5天是血管走向决定的关键期
空间定位证据:正常小鼠的SpA沿右心室肌小梁生长,而基因缺陷者出现左偏
这些发现完美复现了人类遗传学研究结果,证实CXCL12剂量敏感性在物种间高度保守。更令人振奋的是,通过局部注射CXCL12蛋白,研究人员成功诱导了新生小鼠心脏的侧支血管再生——这为未来的"生物搭桥"治疗带来了曙光。
改写心血管医学的未来图景
这项突破性研究不仅解开了胚胎发育的百年之谜,更为临床医学带来多重启示:
个性化风险评估:通过基因检测预判血管解剖,优化支架/搭桥手术方案
再生医学突破:CXCL12蛋白或可诱导"天然搭桥",修复梗死心肌
疾病预防新思路:调控发育相关基因,从源头优化心血管布局
我们现在手握了改写血管生长规则的密码。未来可能通过调控CXCL12通路,实现“医学血运重建”——用发育生物学的智慧对抗心血管疾病。
当研究人员在显微镜下观察胚胎心脏跳动的瞬间,那些舞动的血管正在书写每个人独特的生命密码。而今天,我们终于读懂了这段基因诗篇中最关键的一行。这不仅是对生命奥秘的致敬,更是通向心血管健康新时代的钥匙。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


