2025年3月Science期刊精华
来源:生物谷原创 2025-03-31 09:57
2025年3月份已经结束,3月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Science:新研究解析出线粒体超级复合物的高分辨率结构
doi:10.1126/science.ads8738
我们星球上的大多数生物,无论是植物、动物还是人类,其细胞中都含有线粒体。线粒体是我们细胞中的能量工厂,它们的主要功能是为几乎所有的细胞过程提供能量。
为了实现这一目标,线粒体利用呼吸中的氧气和食物中的碳水化合物来再生ATP,其中ATP是细胞的通用能量货币。这种功能是由称为呼吸复合物(respiratory complex)的蛋白质执行的,它们在能量产生过程中协同工作。尽管这些呼吸复合物是在70年前发现的,但是在此之前,它们在线粒体内的确切组织仍然难以捉摸。
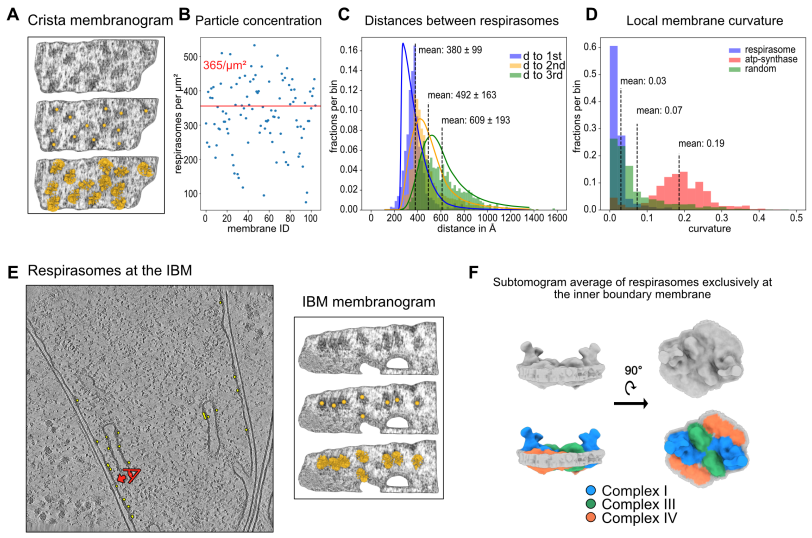
在一项新的研究中,由瑞士巴塞尔大学生物中心的Florent Waltz博士和Ben Engel教授领导的一个研究团队利用前沿的低温电子断层扫描技术,以前所未有的分辨率深入了解了线粒体的结构。他们发现,负责能量产生的蛋白质会组装成大型的“超级复合物”,在提供细胞能量方面发挥着至关重要的作用。
Waltz解释道,“我们的数据显示,呼吸链中的蛋白在线粒体的特定膜区域分布,粘附在一起并形成一种主要类型的超级复合物。使用电子显微镜,可以清楚地看到单个超级复合物——我们可以直接看到它们的结构和工作原理。这种呼吸超级复合物将质子泵送到线粒体膜上。这些产生ATP的超级复合物的作用类似于水磨,利用这种质子流来驱动ATP的产生。”
2.Science:揭示Treg细胞在感染期间保护身体免受自身免疫反应
doi:10.1126/science.adk3248
在感染期间,免疫系统需要区分入侵细菌和病毒表达的外来抗原与身体细胞表达的自身抗原。否则,免疫系统会错误地攻击自己的细胞,对组织造成持久的损伤,并可能导致长期疾病。
芝加哥大学的一项新研究展示了经过特殊训练的免疫细胞群体如何通过防止其他免疫细胞攻击自身组织来保持和平。这一发现有助于更好地了解了感染期间的免疫调节,并为开发预防或逆转自身免疫性疾病的干预措施提供了基础。相关研究结果发表在Science杂志上。
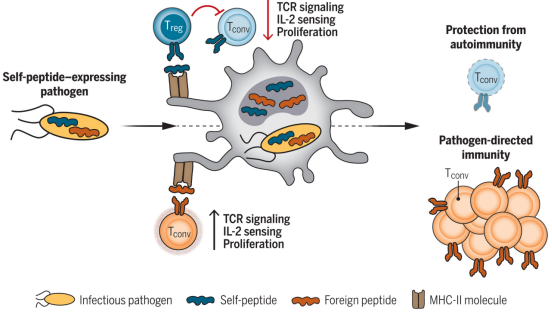
在感染过程中,Treg细胞通过选择性地抑制具有共同自我特异性的Tconv细胞来加强自我-非自我区分
几组白细胞有助于协调免疫反应。树突细胞从外来病原体中获取蛋白质,将其切割成称为抗原的肽,并将其展示在表面上。CD4+常规T(conventional T, Tconv)细胞检查树突细胞呈递的肽。
如果呈递的肽是外来抗原,这些Tconv细胞会大量扩增并转化为活化状态,专门用于根除病原体。如果树突细胞携带“自身肽”,即来自身体自身组织的肽,Tconv细胞应该会停止工作。在自身免疫反应期间,辅助性T细胞不能正确区分外源肽抗原和自身肽,无论如何都会继续攻击。为了防止这种情况发生,另一组称为CD4+调节性T细胞(regulatory T, Treg)的T细胞应该进行干预,防止Tconv细胞的友好攻击。
论文共同通讯作者、芝加哥大学病理学教授Pete Savage博士说,“可以把它们(Treg细胞)看作是维和细胞。”Treg细胞显然在大多数时候都做得很好,但Savage说,它们如何知道何时进行干预并防止Tconv细胞开启自身免疫反应,以及何时抑制并让它们对抗感染,这一点一直不清楚。因此,Savage和他的团队想探索免疫系统的这种特性,即自我-非自我区分(self-nonself discrimination)。
3.Science:新研究在细胞和亚细胞水平上阐明记忆形成的结构特征
doi:10.1126/science.ado8316
在一项新的研究中,研究人员揭示了小鼠大脑中广泛的神经元网络中记忆形成的结构基础。这项研究揭示了记忆如何产生的根本灵活性,以前所未有的分辨率详细描述了细胞和亚细胞水平上与学习相关的变化。理解这种灵活性可能有助于解释为什么记忆和学习过程有时会出错。相关研究结果发表在Science杂志上。
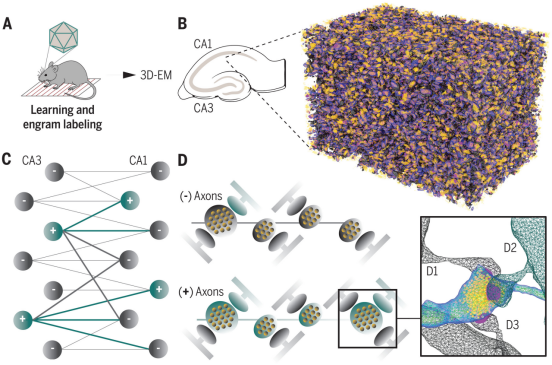
小鼠海马体记忆印迹物理基质的超微结构分析
这些研究结果表明,被分配到某个记忆痕迹(memory trace)的神经元通过一种称为多突触扣结(multi-synaptic bouton)的非典型连接重新组织了它们与其他神经元的连接。在多突触丛中,传递信号和信息的神经元轴突与接收信号的多个神经元接触。根据研究人员的说法,多突触扣结可能使先前研究中观察到的信息编码的细胞灵活性成为可能。
研究人员还发现,参与记忆形成的神经元并没有优先相互连接。这一发现挑战了传统学习理论所预测的“一起放电的神经元连接在一起”的观点。
此外,研究人员观察到,分配给某个记忆痕迹的神经元重组了某些细胞内结构,这些结构提供能量并支持神经元连接中的交流和可塑性。这些神经元还与称为星形胶质细胞的支持细胞增强了相互作用。
通过结合先进的遗传工具、三维电子显微镜和人工智能,斯克里普斯研究所的科学家Marco Uytiepo、Anton Maximov博士及其同事们重建了参与学习的神经元的接线图,并确定了这些神经元的结构变化及其在细胞和亚细胞水平上的连接。
4.Science:我们为何记不起婴儿时发生的事情?新研究提供新的线索
doi:10.1126/science.adt7570
虽然我们在生命的最初几年学到了很多东西,但作为成年人,我们无法记住那个时候发生的具体事件。长期以来,科学家们一直认为,我们不会记住这些经历,因为大脑中负责保存记忆的部分——海马体——在青春期仍在发育,在我们生命最初的岁月里无法对记忆进行编码。但是耶鲁大学的一项新研究发现,事实并非如此。
在这项研究中,耶鲁大学的研究人员向婴儿展示了新的图片,然后测试了他们是否记得这些图片。当婴儿的海马体在第一次看到图片时更活跃时,他们更有可能在以后认出那张图片。这些研究结果表明,在我们生命的最初几年,记忆确实可以在我们的大脑中编码。他们如今正在研究这些记忆随着时间的推移会发生什么。相关研究结果发表在Science杂志上。
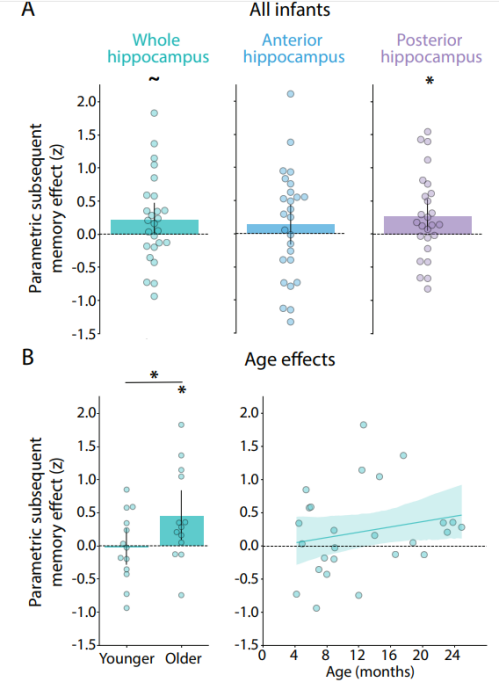
婴儿海马体后续记忆的参数分析
在这项新的研究中,该团队在过去十年中开创了对清醒婴儿进行功能性磁共振成像(fMRI)的方法(由于婴儿的注意力持续时间短,无法保持静止或遵循指示,这在历史上一直很困难),他们在婴儿查看图片时测量了其海马体的活动。
具体来说,研究人员评估了海马体活动是否与婴儿的记忆强度有关。他们发现,当婴儿看到一幅新图片时,海马体的活动越大,婴儿看到它的时间就越长。海马体的后部(靠近后脑勺的部分)是编码活动最强的区域,也是与成年人情景记忆最相关的区域。
5.Science:新研究揭示细菌的跳跃基因控制近三分之一染色体的端粒
doi:10.1126/science.adp1973
作为一种DNA片段,转座子,也称为“跳跃基因”,可以从基因组的一部分移动到另一部分。它们是细菌进化和抗生素耐药性发展的关键。
如今,在一项新的研究中,来自康奈尔大学的研究人员发现了跳跃基因在具有线性DNA的细菌中生存和增殖的新机制。这一发现表明它们有潜力用于生物技术和药物开发。相关研究结果发表在Science杂志上。

研究人员指出,转座子可以靶向并插入细菌宿主内称为端粒的线性染色体末端。在历史上经常用于抗生素开发的链霉菌(Streptomyces)中,他们发现转座子控制着近三分之一染色体的端粒。
论文通讯作者、康奈尔大学微生物学教授Joseph Peters说,“这是它们生物学的重要组成部分。细菌就像小修补匠。它们总是收集这些可移动的DNA片段,并且一直在创造新的功能——抗生素耐药性的一切实际上都是关于可移动的遗传因子和几乎总是可以在细菌之间移动的转座子。”
6.Science: 新研究揭示靶向巨噬细胞的过氧化物酶体有望治疗新冠病毒等呼吸道病毒感染引起的肺部问题
doi:10.1126/science.adq2509
在一项新的研究中,来自弗吉尼亚大学医学院的研究人员发现严重的新冠肺炎(COVID-19)如何破坏免疫细胞修复肺部的能力,这有助于解释长新冠(long COVID)的持续影响。这些发现为长新冠以及流感病毒等呼吸道感染引起的其他短期和慢性疾病提供了一种新的治疗方法。
在弗吉尼亚大学医学院的Jie Sun博士的领导下,研究人员发现,包括新冠肺炎和流感在内的严重病毒感染会严重损害称为巨噬细胞的免疫细胞中的一种关键细胞器:过氧化物酶体(peroxisome)。Sun 和他的团队发现,巨噬细胞在组织损伤后指导肺部修复,但它们这样做的能力因过氧化物酶体的丧失而受到削弱。相关研究结果发表在Science杂志上。
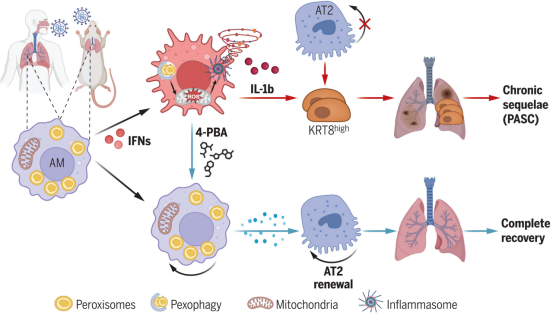
新模型用于研究过氧化物酶体在病毒损伤后巨噬细胞介导的肺泡再生中的功能
令人鼓舞的是,Sun团队发现,他们可以使用一种已经获得美国食品药品管理局(FDA)批准的药物来增强受损的过氧化物酶体的功能,并提高免疫系统治愈肺部损伤的能力。
Sun说,“新冠肺炎会破坏我们细胞内的这些微小结构,使得肺部无法正常愈合。我们的发现很重要,因为它不仅解释了为什么一些人在最初患病后很长一段时间仍有呼吸问题,而且还为我们提供了一种潜在的治疗方法,即通过靶向关键免疫细胞内的一种微小细胞器来帮助他们康复。这种微小的细胞器可以发挥重要作用。我希望我们的研究能够带来新的以过氧化物酶体为中心的疗法,以便帮助长新冠患者。”
7.帕金森病的“破局者”!Science:科学家首次揭示PINK1蛋白结构,为治疗带来新希望
doi:10.1126/science.adu6445
帕金森病是一种隐匿的神经退行性疾病,通常需要数年甚至数十年才能被诊断出来。这种疾病不仅伴有震颤,还可能导致认知障碍、语言问题、体温调节异常和视力问题等近40种症状。
PINK1是一种与帕金森病直接相关的蛋白,早在20多年前就被发现。然而,尽管科学家们知道PINK1在帕金森病中扮演重要角色,但长期以来,他们一直无法看到人类PINK1的结构,也不清楚它是如何附着在受损线粒体表面并被激活的。
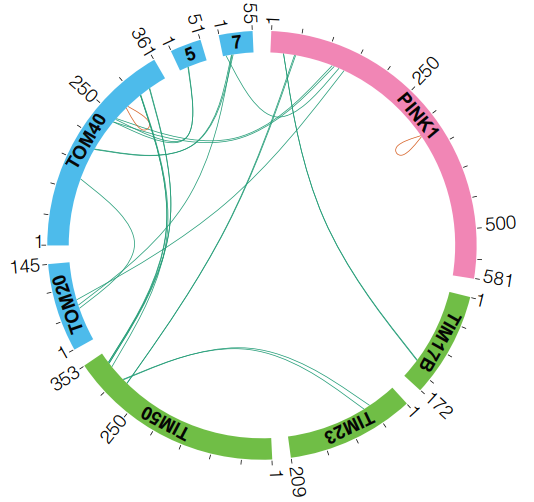
针对PINK1-TOM-TIM23复合物成分的XL-MS分析
最近,沃尔特与伊丽莎-霍尔医学研究所(WEHI)的研究人员在《Science》杂志上发表了一项突破性研究,首次揭示了与线粒体结合时的人类PINK1结构。这一发现不仅解开了长达数十年的谜团,还为开发治疗帕金森病的新药物铺平了道路。
线粒体是细胞的“能量工厂”,负责为细胞提供能量。需要大量能量的细胞(如脑细胞)可能包含数百甚至数千个线粒体。PINK1蛋白由PARK6基因编码,其主要功能是检测受损的线粒体并标记它们以便清除。在健康人中,当线粒体受损时,PINK1会聚集在线粒体膜上,并通过一种名为泛素的小蛋白发出信号,指示受损的线粒体需要被清除。
然而,在帕金森病患者中,PINK1的突变导致这一过程无法正常进行,受损的线粒体在细胞中积累,最终导致脑细胞死亡。脑细胞对能量需求极高,因此对线粒体损伤特别敏感。
论文通讯作者David Komander教授表示,他的团队经过多年的研究,终于揭开了人类PINK1的神秘面纱。他们首次看到了PINK1如何在线粒体上组装并被激活。Komander教授激动地说:“这是帕金森病研究的一个重要里程碑。终于看到PINK1并了解它是如何与线粒体结合的,这令人难以置信。我们的结构揭示了许多改变PINK1的新方法,这将改变帕金森病患者的生活。”
8.Science:科学家利用冷冻电镜技术揭示DNA复制过程隐藏的机制,并阐明新型癌症疗法靶点
doi:10.1126/science.adt1978
在我们的身体里,每天都有数十亿个细胞在忙碌地分裂,它们像是勤劳的工人,用新细胞替换掉那些老去或受伤的细胞,而每次细胞分裂时,我们机体中拥有超过30亿个碱基对的庞大基因组都需要被精准地从母细胞复制到新生成的子细胞中;然而这个看似平常的过程却暗藏危机,一旦出现“复制压力”,就容易出错,从而导致基因突变,进而可能引发癌症和其它疾病。
而一种名为G-四链体(G4s,G-quadruplexes)的特殊DNA结构就是这种危机的潜在源头之一。G4s是一种非B型的DNA二级结构,其在基因组中广泛存在,尤其是在富含鸟嘌呤(G)的区域中。这些结构比正常的DNA双螺旋更加紧凑,有点像是DNA的“小疙瘩”,会让负责复制的生物机器—复制体(replisome)卡住,从而阻碍DNA的正常复制。
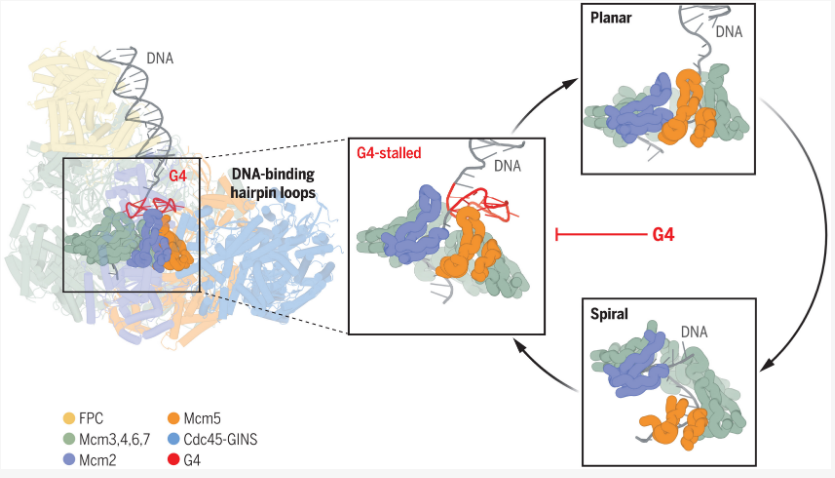
G4s或能延缓真核生物的复制解旋酶
近日,一篇发表在国际杂志Science上题为“G-quadruplex–stalled eukaryotic replisome structure reveals helical inchworm DNA translocation”的研究报告中,来自美国纪念斯隆-凯特琳癌症中心等机构的科学家们通过使用冷冻电镜技术(cryo-EM)对G4s进行了深入研究。相关研究结果揭示了G4s如何阻碍DNA复制,还首次详细捕捉到了人类细胞中驱动细胞复制机器沿DNA移动的“引擎”—CMG解旋酶的详细图像。
研究者Sahil Batra博士表示,即使在前导链模板中存在一个G4,也足以通过阻止CMG解旋酶来使复制体停滞;而冷冻电镜的结构显示,折叠的G4被困在会被困在CMG中心通道内,从而就会阻止其移动,这一发现不仅为理解G4s如何影响基因组稳定性提供了新的视角,也为癌症治疗提供了新的思路。
9.Science:新研究表明在出生后早期暴露于都柏林念珠菌可降低1型糖尿病的风险
doi:10.1126/science.adn0953
一项针对小鼠的新研究发现,肠道微生物组在婴儿期塑造了胰岛素分泌细胞的发育,导致代谢和糖尿病风险的长期变化。这些结果最终可能通过提供帮助胰腺生长和愈合的特定肠道微生物来帮助医生降低1型糖尿病的风险,甚至可能恢复成年后失去的代谢功能。
研究人员发现,从长远来看,早年接触广谱抗生素的小鼠代谢健康状况较差。如果小鼠在出生后不久的10天内接受抗生素治疗,它们会产生更少的β细胞——胰腺中调节血糖的胰岛素分泌细胞。接受抗生素治疗的小鼠在成年后血糖水平也较高,胰岛素水平较低。

都柏林念珠菌定植促进出生后胰腺的发育
论文共同通讯作者、犹他大学健康学院病理学教授June Round博士说,“对我来说,这令人震惊,也有点可怕。这表明肠道微生物群在这个非常短的早期发育阶段是多么重要。”
通过测试影响不同类型肠道微生物的各种抗生素,研究人员确定了几种特定的肠道微生物增加了胰岛素产生组织的数量和血液中的胰岛素水平。有趣的是,其中一种促进代谢的肠道微生物是一种名为都柏林念珠菌(Candida dubliniensis)的未经研究的真菌,这种真菌在健康的成年人中没有发现,但在婴儿中可能更常见。
至关重要的是,早年暴露于都柏林念珠菌也大大降低了高危雄性小鼠患1型糖尿病的风险。当遗传上易患1型糖尿病的雄性小鼠在婴儿期被代谢“中性”的肠道微生物定植时,它们90%的时间都会患上这种疾病。它们被都柏林念珠菌感染的同胞患糖尿病的几率不到15%。
10.狗狗和人一样,有这个基因就容易胖!Science揭示狗与人类的“肥胖基因”
doi:10.1126/science.ads2145
近年来,肥胖不仅困扰着人类,也悄悄“传染”给了我们的宠物狗。据统计,大约40%~60%的宠物狗超重或肥胖,这可能导致一系列健康问题,如糖尿病、关节炎和心血管疾病。有趣的是,狗不仅是人类最好的朋友,还是研究肥胖的绝佳模型。它们和人类一样,在相似的环境影响下产生肥胖,而且由于特定品种的狗具有高度的遗传相似性,科学家们更容易将它们的基因与疾病联系起来。

身体状况评分描述符和图像用于评分肥胖的狗。该图表是由世界小动物兽医协会提供的全球营养委员会工具包的一部分
最近,剑桥大学的研究团队通过对英国拉布拉多猎犬的研究,发现了多个与狗肥胖相关的基因,并证明这些基因也与人类肥胖密切相关。其中,最引人注目的是DENND1B基因。这个基因不仅存在于狗体内,也在人类基因组中被发现,并且与人类的肥胖风险显著相关。
DENND1B基因直接影响大脑中的瘦素-黑皮质素通路(leptin-melanocortin pathway),这是调节能量平衡和食欲的关键通路。简单来说,这个通路就像身体的“能量调节器”,控制着我们何时感到饥饿,何时停止进食。当这个通路出现问题时,身体可能会“误判”能量需求,导致暴饮暴食和体重增加。
除了DENND1B,研究团队还发现了另外四个与狗肥胖相关的基因,尽管它们的影响较小,但这些基因同样在人类基因组中找到了“对应版本”。这一发现进一步证明了狗和人类在肥胖机制上的相似性。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


