Nature:毛囊干细胞的“兼职工作”——死亡细胞的吞噬与清除
来源:生物探索 2024-09-11 11:06
本研究利用毛发生长周期中组织“再生-退化”的周期性模型,发现毛囊干细胞通过感知邻近凋亡细胞释放的脂质和健康细胞释放的维甲酸,激活 RARγ–RXRα 信号,从而精确调控吞噬相关基因的表达。
一般来说,生物体内的死亡细胞主要通过吞噬作用(phagocytosis)被清除,该过程涉及免疫系统中的特定细胞,如巨噬细胞、中性粒细胞和树突状细胞。当吞噬作用发生时,吞噬细胞会识别死亡细胞表面的特定信号分子(如磷脂酰丝氨酸),包围并吞噬它们,形成吞噬泡(phagosome)。吞噬泡与细胞内的溶酶体融合,形成吞噬溶酶体(phagolysosome),继而利用其中的各种消化酶分解死亡细胞的各种成分,分解后的产物可以被吞噬细胞利用或者通过特定途径排出体外【1】。
然而,在正常生理状态下,组织处理死亡细胞通常会优先召集上皮细胞、间充质细胞和神经元等一些非专门化的吞噬细胞来执行吞噬任务。与专门化的吞噬细胞相比,大多数“兼职”吞噬细胞的运动性较弱,其吞噬活动仅限于附近细胞,且吞噬活动迅速并“集约”【2,3】。然而,这些非运动性的“兼职”吞噬细胞是如何在发挥其 “本职”功能的同时感知和消除濒死细胞的,目前仍亟待研究。
毛发生长周期的破坏阶段(destructive phase)是研究“兼职”吞噬细胞吞噬调控机制的极佳模型。每次毛囊再生和毛发形成(生长期)同步进行后,小鼠毛囊的上皮干细胞区以下的整个毛囊都会在凋亡和吞噬过程中(catagen, 退行期)被破坏,这一过程从毛囊最底部开始,并逐渐向干细胞区推进【4】。研究表明,毛发发育中的吞噬过程受到严格的调控,以维持干细胞的生存和组织稳态【5】。然而,毛发生长周期中非专一性吞噬细胞识别并清除凋亡细胞的机制目前仍不清楚。
洛克菲勒大学HHMI研究员Elaine Fuchs实验室在Nature杂志发表了题为Stem cells tightly regulate dead cell clearance to maintain tissue fitness 的研究文章,利用小鼠毛囊干细胞介导的毛发周期性再生模型,作者详细分析了毛囊再生过程中凋亡细胞的清除过程及其对干细胞和组织健康的影响,揭示了毛囊干细胞通过感知凋亡细胞释放的脂质和健康细胞释放的维甲酸,激活 RARγ–RXRα 信号通路,精准调控吞噬相关基因的表达,并在适当时机清除凋亡细胞。本研究揭示了毛囊干细胞在通过其干细胞活性维持组织完整性的同时,“兼职”执行吞噬任务分子机制。

处于静止期(休止期)的毛囊干细胞(HFSCs)位于毛囊上部外根鞘(uORS)的凸起区,负责启动毛发再生周期。当毛囊干细胞与下方的特化间充质细胞(dermal papilla,真皮乳头)之间的交流达到阈值时,会启动新的生长期,促使毛囊干细胞短暂增殖,并产生短命的后代(short-lived progeny),启动毛发的生长。随着新的毛囊生长并将真皮乳头向下推移,uORS恢复到静止状态,为下一个毛发周期保留一个新的HFSCs库(bulge, 凸起区),与此同时短命的后代则在成熟毛囊的基部推动毛发的形成【4】。
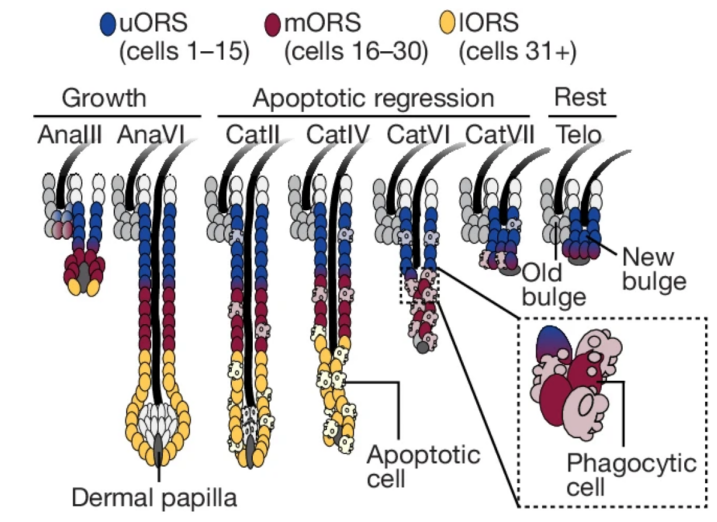
图1 小鼠的毛发生长周期示意图 (Credit: Nature)
之前研究发现,当成熟毛囊的基部集中发生细胞死亡时,清除尸体细胞的是下部外根鞘(lORS)细胞,而不是CD45+吞噬细胞【5】。而当凋亡波及到干细胞区时,尸体细胞的清除机制尚不清楚。通过探究HFSCs在毛囊生命周期中,特别是在退行期清除凋亡细胞的机制,作者发现位于uORS的HFSCs通过吞噬凋亡的邻近细胞而维持自身稳态,并为下一个毛囊周期做好准备。值得一提的是,与免疫细胞不同,非运动性的HFSCs清除凋亡细胞时依赖于近距离接触,并表现出多次吞噬能力。
尽管早期退行期 lORS 细胞会死亡,但一些晚期退行期的 HFSCs 却能幸免,并且一旦凋亡波消退,它们就必须抑制吞噬作用,以便为下一个毛发周期提供动力。因此作者接下来探究了HFSCs是如何在晚期退行期抑制凋亡小体清除功能,并在凋亡波结束后恢复常规干细胞功能的时空调控机制。通过单细胞转录组分析,作者发现退行期毛囊中的HFSCs显著富集了与吞噬作用相关的基因,并通过实验证实了其中的TAM家族受体和磷脂酰丝氨酸中介蛋白编码基因在凋亡细胞清除中的关键作用。进一步的体内实验显示,阻断TAM受体或抑制磷脂酰丝氨酸暴露会延迟凋亡细胞的清除,表明这些机制在维持毛囊周期中的吞噬活动中发挥着重要作用。
与主要负责清除死亡细胞的专一性吞噬细胞不同,HFSCs的吞噬程序具有短暂性,为了探明HFSCs介导吞噬作用的动态调控机制,作者利用ATAC-seq分析了HFSCs在毛发生长周期中的染色质结构变化。作者发现,退行期染色质开放区域中富集了编码凋亡细胞受体、可溶性磷脂酰丝氨酸桥接分子和细胞吞噬的基因。通过筛选介导该染色质可及性动态变化的候选转录因子,作者发现RXRα 通过调控染色质可接近性和转录活性,启动了毛囊干细胞在退行期的吞噬程序。RXRα 的调节对于毛囊干细胞清除凋亡邻居细胞至关重要,且其缺失会导致凋亡细胞残留,引发继发性坏死。
尽管 RXR 可以作为许多核受体的异二聚体伴侣,但其DR2 基序(在ATAC-seq中富集度最高)已被证明与 “RXR-视黄酸受体(RARs)”异二聚化有关。通过探究RXRα 和 RARγ 在HFSCs吞噬作用中的协同功能,作者发现HFSCs 通过感知邻近的凋亡细胞,激活 RXRα 和 RARγ,从而上调吞噬相关基因并清除凋亡细胞,且RXRα 和 RARγ 的核受体活性为吞噬过程所必需。进一步研究显示,RXRα 缺失会导致 HFSCs 对凋亡细胞的清除能力减弱,并且 RXRα 和 RARγ 是协同而非独立作用的。与专一性的吞噬细胞不同,HFSCs 不需要吞噬或消化尸体即可激活 RXRα–RARγ 信号,这些信号通过视黄酸(RA)与LPC/AA 的互作,共同促进核受体活性,启动吞噬程序。一旦尸体细胞被清除,这一信号通路就会关闭,剩余的干细胞自动进入休眠状态,为下一个毛发周期做好准备。通过ATAC-seq 和 CUT&RUN 实验表征吞噬相关基因对 RXRα–RARγ信号的依赖性,作者发现HFSCs 能够通过与局部RA 结合,感知凋亡尸体信号,从而激活核 RXRα–RARγ 活性,诱导一种短暂的吞噬状态。因此,RXRα–RARγ 信号通路在HFSCs吞噬相关基因活性的调控中发挥了关键作用。
在多种组织中,当非专一性吞噬作用发挥作用时,巨噬细胞或树突状细胞会被激活以弥补上皮细胞凋亡清除能力的不足【6】。作者探讨了皮肤中常驻的专一性吞噬细胞是否也能激活以增强凋亡细胞清除活性。作者发现皮肤中常驻的专一性吞噬细胞(如巨噬细胞和朗格汉斯细胞)虽然能够感知未被清除的细胞尸体并做出反应,但其免疫反应速度较慢,导致组织损伤信号的积累;此类损伤信号激活了 HFSCs 中的 AP-1 和 STAT3 等转录因子,促使其进入增殖状态,并最终导致毛发周期的休止期缩短。此外,当HFSCs暴露于无法吞噬的尸体所产生的坏死碎片时,它们会激活损伤反应,暂时刺激增殖,但最终会损害细胞的适应性。这些结果表明,HFSCs 在清除细胞尸体失败的情况下,会经历一段短暂的增殖高峰,但这种损伤反应对其长期功能具有负面影响。
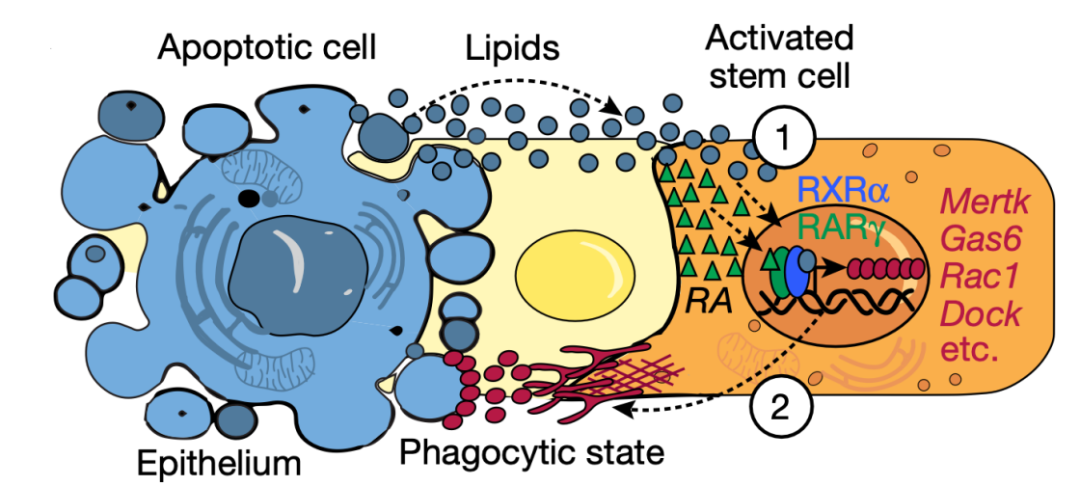
模式图(Credit: Nature)
综上所述,本研究利用毛发生长周期中组织“再生-退化”的周期性模型,发现毛囊干细胞通过感知邻近凋亡细胞释放的脂质和健康细胞释放的维甲酸,激活 RARγ–RXRα 信号,从而精确调控吞噬相关基因的表达。这种机制不仅能确保毛囊干细胞在适当的时机和地点执行吞噬功能,还维持了干细胞在维持组织完整性的 “本职工作”和执行吞噬任务这一“兼职工作”之间的平衡。
参考文献
1. Nagata, S. Apoptosis and clearance of apoptotic cells. Annu. Rev. Immunol. 36, 489–517 (2018).
2. Doran, A. C., Yurdagul, A. Jr & Tabas, I. Efferocytosis in health and disease. Nat. Rev.Immunol. 20, 254–267 (2020).
3. Lu, Z. et al. Phagocytic activity of neuronal progenitors regulates adult neurogenesis. Nat. Cell Biol. 13, 1076–1083 (2011).
4. Greco, V. et al. A two-step mechanism for stem cell activation during hair regeneration. Cell Stem Cell 4, 155–169 (2009).
5. Mesa, K. R. et al. Niche-induced cell death and epithelial phagocytosis regulate hair follicle stem cell pool. Nature 522, 94–97 (2015).
6. Rothlin, C. V., Hille, T. D. & Ghosh, S. Determining the effector response to cell death. Nat. Rev. Immunol. 21, 292–304 (2021).
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


