BJC:科学家首次发现,血液微生物DNA可用于食管癌的早筛和预后!
来源:奇点糕 2022-11-11 15:05
该研究首次表明,基于循环mbDNA的宏基因组在食管腺癌早筛和预后诊断中具有强大的生命力。此外,该研究鉴定的与食管腺癌诊断和预后相关的重要微生物,未来或可成为潜在的治疗靶点。
火锅、煲汤和各类热饮都是我们冬天的最爱,它们既暖胃又让我们快乐!然而,当我们沉醉热饮热食时,有一个幽灵——食管癌(EC)也在悄悄接近!
食管癌(EC)是全球第七大癌症和第六大癌症死因[1]。我国食管癌负担严重,据WHO数据,2020年我国食管癌新发病例为32.4万例,死亡病例为30.1万例,分别占全球食管癌发病与死亡的50%以上[2]!
食管癌可分为食管鳞状细胞癌(ESCC)和食管腺癌(EAC)[2-3]。我国以食管鳞状细胞癌为主,西方国家以食管腺癌为主[1-3]。食管癌早期缺乏典型的临床症状,因此大多数患者就诊时已达中晚期,患者预后较差[3,4]。早期食管癌患者在接受治疗后,5年生存率可达95%[5]。因此,开发高效的食管癌早筛早诊工具,对于提高食管癌患者的生存率至关重要!
近年来,基于循环微生物DNA(mbDNA)开发的癌症检测工具,在多个实体瘤筛查的基础研究中大放异彩[6]。然而,目前尚无针对食管腺癌的检测工具问世。
近日,由美国希望之城医学中心贝克曼研究所Ajay Goel领衔的研究团队,在《英国癌症杂志》(British Journal of Cancer)发表重要研究成果[7]。
研究者发现食管腺癌患者具有独特的血液mbDNA特征,而且他们首次开发了基于mbDNA的食管腺癌诊断和预后评估的宏基因组工具,该工具检测性能优异。
该研究表明,mbDNA具有作为食管腺癌的早筛早诊、预后生物标志物和干预靶点的潜力。

论文首页截图
冰冻三尺非一日之寒!在诊断为食管腺癌前,患者往往需要经历从胃食管反流病(GERD)-巴雷特食管(BE)-高度不典型增生(HGD/Dysplasia)-食管腺癌的恶性转变[8-9]。
迄今为止,虽然有研究报道了与GERD、BE和食管腺癌相关的食管组织微生物组的特征。然而,目前尚无患者血液mbDNA特征的研究。为此,研究者使用了食管腺癌致癌过程中不同患者的血清样本,并对其血清样本进行了宏基因组测序。
接下来我们就一起来看看Ajay Goel团队是如何开展这项研究的。
这项研究纳入了2016-2018年间,在阿勒格尼健康网络食管和肺研究所治疗的81名患者,包括51名食管腺癌患者、10名不典型增生患者、10名BE和10名GERD患者。所有患者均超过18岁。
研究者发现,与GERD患者相比,用于估计微生物群α多样性的香农指数(Shannon index)在食管腺癌患者中显著降低(图1a)。与食管腺癌患者相比,GERD患者的微生物丰富度明显更高(图1b-c)。此外,食管腺癌患者微生物群的β多样性与其他组明显不同(图1d)。
总之,在从GERD到食管腺癌的疾病进程中,患者会出现血液循环微生物失调。
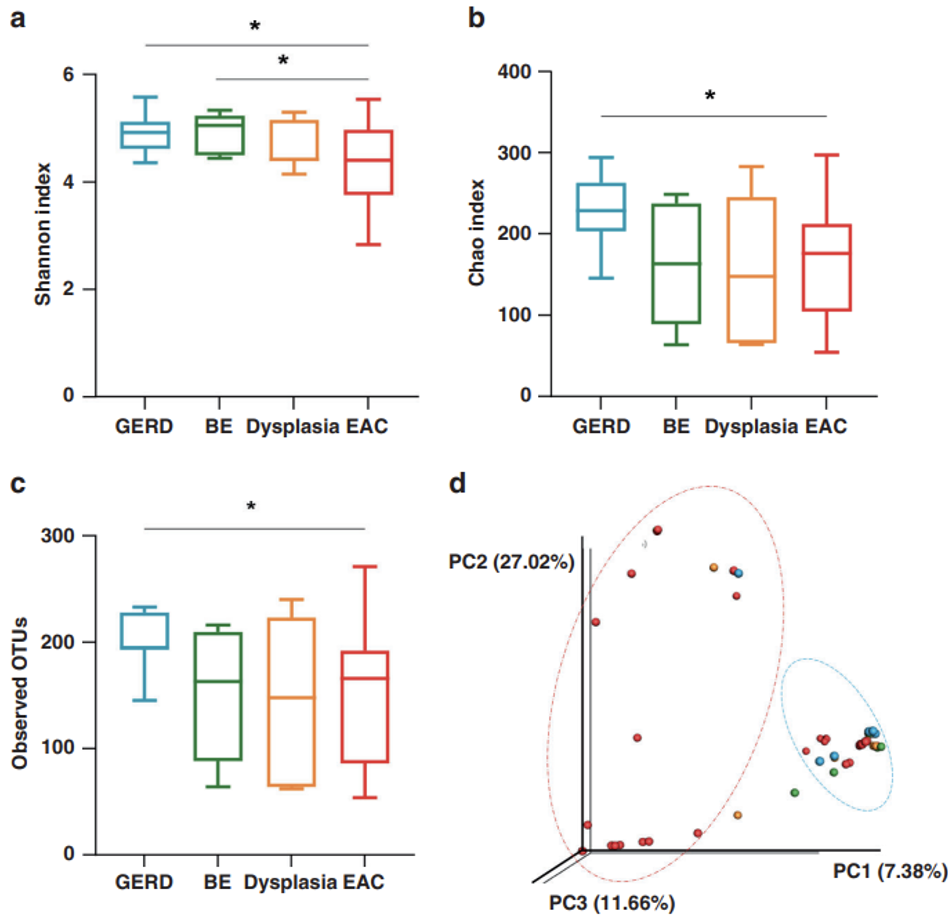
图1食管腺癌患者mbDNA特征显著改变
研究者进一步探究了患者血清微生物组成的差异。研究者发现,假长双歧杆菌(B. pseudolongum)、清酒乳杆菌(L.sakei)和大肠杆菌(E.coli)分别是不同组间丰度最高的细菌。
研究者还检测了这些细菌在每组患者血清中的平均丰度。数据分析显示,L.sakei在GERD患者中的相对丰度最高,在HGD和食管腺癌患者中不存在(p<0.0001,图2)。相比之下,E.coli在GERD组中不存在,但在食管腺癌患者中的丰度最高(p=0.53)。
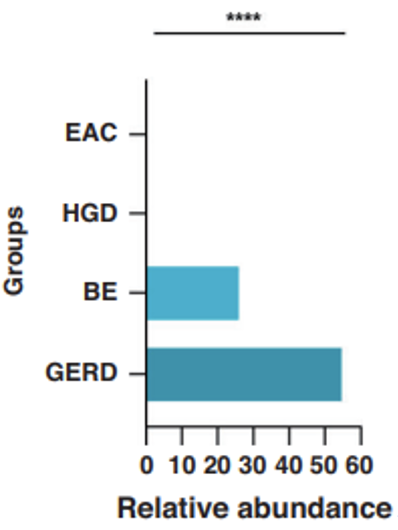
图2与GERD组相比,HGD和食管腺癌组血清中的L.sakei相对丰度显著降低
LEfSe即LDA效应分析,可分析组间菌群差异[10]。利用LEfSe,研究者可获得在不同组间丰度有显著差异的细菌物种,并将其作为生物标志物[10]。
研究者指出,当LDA分数截止值大于4时,不同组患者间有显著差异的细菌物种主要是多种乳酸杆菌(图3)。与其他三组相比,L.sakei在GERD组中显著富集(p<0.00001;图3)。当GERD组与食管腺癌组两两比较时,L.sakei、弯曲乳杆菌(L.curvatus)、柯林斯氏菌(C.stercoris)和粪便拟杆菌(B.stercoris)在GERD组显著富集,相比之下,大肠杆菌在食管腺癌患者中显著富集(图3)。
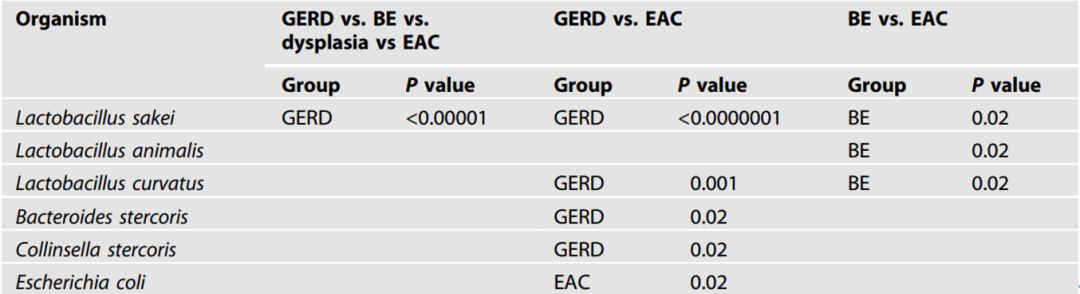
图3在种水平上,不同组患者LEfSe分析结果
为验证上述结果,研究者整合这5种特异性菌种(L.sakei、L.curvatus、C.stercoris、B.stercoris和E.coli),开发了基于mbDNA的宏基因组食管腺癌诊断工具。
研究者使用逻辑回归模型,对该工具的诊断性能进行了验证。ROC曲线显示,该工具对GERD和食管腺癌的鉴别表现出优秀的性能,AUC值为0.89,最佳灵敏度为60%,特异性为95%(图4)。
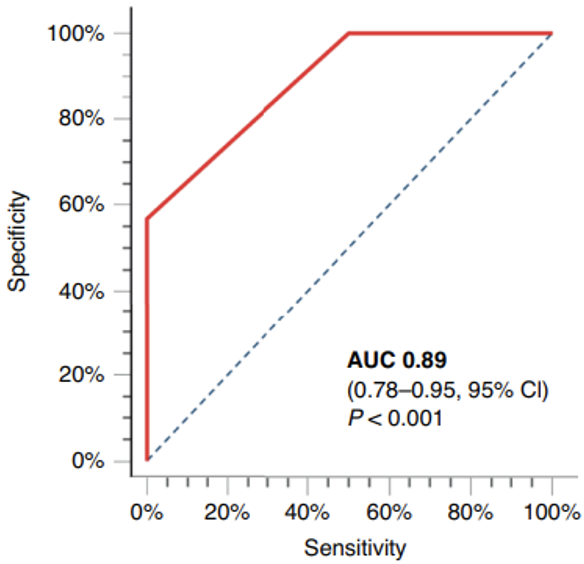
图4宏基因组工具表现出优秀的食管腺癌早筛效果
那么宏基因组能否用于预测食管腺癌患者生存期呢?研究者以食管腺癌患者总生存期(OS)是否达到24个月为标准,将患者分为两类:OS<24个月和OS≥24个月。
研究者对不同类别患者的样本进行了LEfSe分析。研究者发现,沙门氏菌噬菌体球衣(Salmonella phage jersey)和大肠杆菌病毒P1(Escherichia virus P1)在OS≥24个月组中显著富集(图5a)。随后,研究者构建了一个包含这两种噬菌体和大肠杆菌的宏基因组工具,用于预测食管腺癌患者的生存期。
当该工具与患者临床TNM分期相结合时,ROC曲线显示,该工具对鉴别OS≥24个月的患者表现出不俗的性能,AUC为0.84,最佳灵敏度86%,特异性65%(图5b)。
此外,与单独使用临床TNM分期相比,当TNM分期与宏基因组结合时,后者能够预测更长的OS,风险比(HR)为6.23(p<0.001)(图5c)。
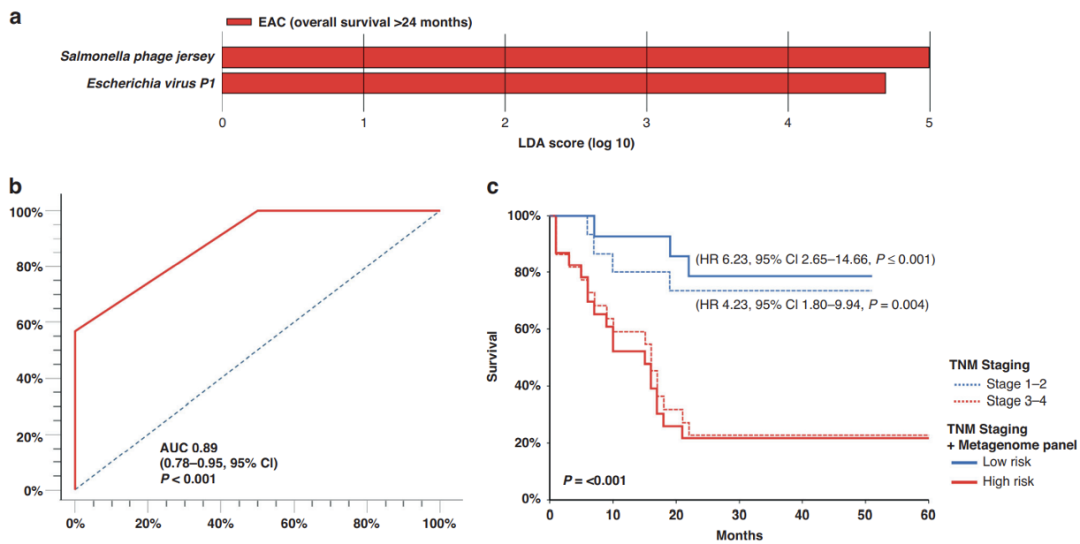
图5宏基因组特征可作为食管腺癌患者预测OS的生物标志物
总的来说,该研究首次表明,基于循环mbDNA的宏基因组在食管腺癌早筛和预后诊断中具有强大的生命力。此外,该研究鉴定的与食管腺癌诊断和预后相关的重要微生物,未来或可成为潜在的治疗靶点。
参考文献
[1] Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021;71(3):209-249. doi:10.3322/caac.21660
[2] 赫捷, et al.中国食管癌筛查与早诊早治指南(2022,北京). 中国肿瘤 31.06(2022):401-436.
[3] Arnold M, Ferlay J, van Berge Henegouwen MI, Soerjomataram I. Global burden of oesophageal and gastric cancer by histology and subsite in 2018. Gut. 2020;69(9):1564-1571. doi:10.1136/gutjnl-2020-321600
[4] Kambhampati S, Tieu AH, Luber B, Wang H, Meltzer SJ. Risk Factors for Progression of Barrett's Esophagus to High Grade Dysplasia and Esophageal Adenocarcinoma. Sci Rep. 2020;10(1):4899. Published 2020 Mar 17. doi:10.1038/s41598-020-61874-7
[5] Duggan MA, Anderson WF, Altekruse S, Penberthy L, Sherman ME. The Surveillance, Epidemiology, and End Results (SEER) Program and Pathology: Toward Strengthening the Critical Relationship. Am J Surg Pathol. 2016;40(12):e94-e102. doi:10.1097/PAS.0000000000000749
[6] Poore GD, Kopylova E, Zhu Q, et al. Microbiome analyses of blood and tissues suggest cancer diagnostic approach. Nature. 2020;579(7800):567-574. doi:10.1038/s41586-020-2095-1
[7] Zaidi AH, Pratama MY, Omstead AN, et al. A blood-based circulating microbial metagenomic panel for early diagnosis and prognosis of oesophageal adenocarcinoma [published online ahead of print, 2022 Sep 12]. Br J Cancer. 2022;10.1038/s41416-022-01974-5. doi:10.1038/s41416-022-01974-5
[8] Bhat S, Coleman HG, Yousef F, et al. Risk of malignant progression in Barrett's esophagus patients: results from a large population-based study [published correction appears in J Natl Cancer Inst. 2013 Apr 17;105(8):581]. J Natl Cancer Inst. 2011;103(13):1049-1057. doi:10.1093/jnci/djr203
[9] Chen X, Yang CS. Esophageal adenocarcinoma: a review and perspectives on the mechanism of carcinogenesis and chemoprevention. Carcinogenesis. 2001;22(8):1119-1129. doi:10.1093/carcin/22.8.1119
[10] Segata N, Izard J, Waldron L, et al. Metagenomic biomarker discovery and explanation. Genome Biol. 2011;12(6):R60. Published 2011 Jun 24. doi:10.1186/gb-2011-12-6-r60
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


