Nature子刊:平渊团队开发基因编辑溶瘤病毒-T细胞嵌合体,用于癌症免疫治疗
来源:生物世界 2024-02-13 11:05
该研究发现,T细胞能够增强eOA的实体瘤靶向输送,通过在瘤内基因编辑PD-L1基因改善肿瘤微环境,可以同时增强溶瘤病毒疗法和过继T细胞疗法的实体瘤治疗。
浙江大学药学院/良渚实验室平渊团队基于CRISPR/Cas9基因编辑递送技术以及过继T细胞增强技术的基础上,,在 Nature Biotechnology 期刊发表了题为:An oncolytic virus–T cell chimera for cancer immunotherapy 的研究论文。
该研究开发了一种名为ONCOTECH的技术(溶瘤病毒-T细胞嵌合体)。该技术首先构建了一个表达CRISPR/Cas9的溶瘤腺病毒,使用含有特定抗原表达的生物膜对该溶瘤腺病毒进行膜包被,再通过T细胞表面的T细胞受体携带膜包被的基因编辑溶瘤腺病毒(命名为eOA)。该研究发现,T细胞能够增强eOA的实体瘤靶向输送,通过在瘤内基因编辑PD-L1基因改善肿瘤微环境,可以同时增强溶瘤病毒疗法和过继T细胞疗法的实体瘤治疗。

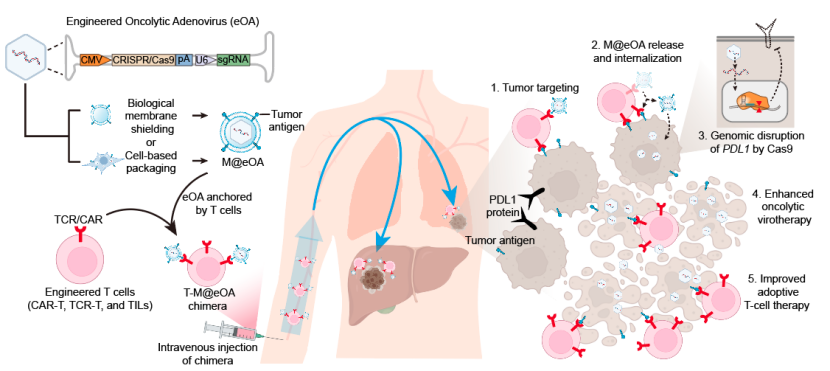
图1:基因编辑溶瘤病毒-T细胞嵌合体用于增强溶瘤病毒疗法和过继T细胞疗法的示意图
ONCOTECH的主要原理:首先将一种能够编码CRISPR-Cas9基因编辑器的溶瘤腺病毒(Oncolytic Adenoviruses,OAs)包裹在一个表达T细胞特异性抗原的生物膜中,然后将这些膜伪装的肿瘤溶病毒通过识别T细胞受体(TCRs)或嵌合抗原受体(CARs)的方式物理地附着在T细胞的表面。这种锚定策略不会影响T细胞的功能,而且一旦携带肿瘤溶病毒的T细胞到达肿瘤细胞并识别出它们的特异性抗原,溶瘤腺病毒就会被释放出来,并感染肿瘤细胞。
更为重要的是,由于溶瘤病毒疗法和过继T细胞疗法都会在实体瘤内造成PD-L1的高表达,从而逃避免疫监控和T细胞的进一步杀伤。而基因编辑溶瘤腺病毒中携带的Cas9编辑器能够靶向破坏肿瘤细胞和肿瘤内的免疫抑制细胞中的PD-L1基因,降低它们的PD-L1表达水平,从而逆转肿瘤微环境的免疫抑制作用,这有利于T细胞治疗和溶瘤病毒的肿瘤溶解作用。
研究团队首先提取表达OVA的肿瘤细胞膜对eOA进行包被,再使用OT-1鼠来源的OVA靶向的CD8+ T细胞携带膜包被的eOA,作为第一代ONCOTECH技术进行了一系列的鼠源肿瘤模型的验证实验,包括小鼠皮肤癌皮下、复发和转移模型以及小鼠乳腺癌模型。为了进一步推进临床转化,研究团队构建了第二代的ONCOTECH技术,在该技术中,他们使用了表达特定抗原的HEK293细胞来一步包装和制备纳米囊泡包被的基因编辑溶瘤病毒,再使其携带到特定特定抗原的CAR-T细胞表面,使用具有人免疫系统的人源化小鼠,在人原位脑瘤模型、人原位肺癌、人胰腺癌PDX模型中进一步验证了该系统的治疗效果。
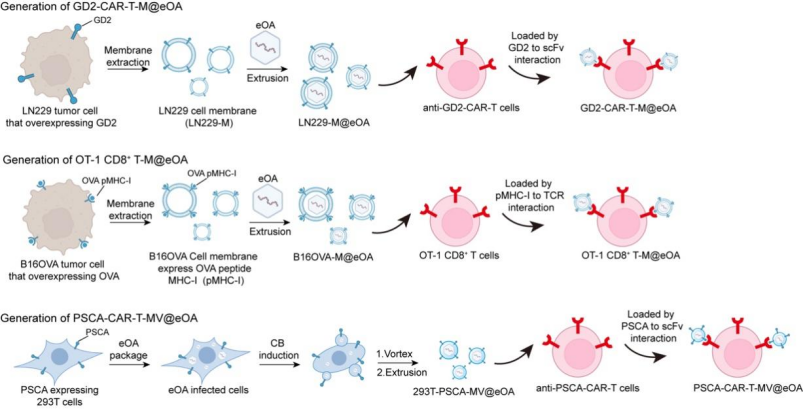
图2:ONCOTECH技术的构建步骤与原理
结果表明,ONCOTECH能够有效地抑制多种类型的肿瘤生长,包括皮肤癌、乳腺癌、肺癌等,并且比单独使用肿瘤溶病毒或T细胞治疗更有效。此外,ONCOTECH也能够诱导肿瘤的长期免疫记忆,防止肿瘤的复发。该研究为癌症治疗提供了一种新的思路和方法,也为溶瘤病毒治疗的床应用开辟了新的可能性。
浙江大学药学院博士生陈宇轩、陈小红博士为该论文共同第一作者,浙江大学药学院/良渚实验室平渊教授为该论文通讯作者,合作者包括中国科学院过程工程研究所魏炜研究员团队及厦门大学刘刚教授团队。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


