Nature子刊:我国科学家揭示干细胞衍生性外泌体修复缺血性肌肉损伤机制
来源:本站原创 2021-04-14 09:19
2021年4月14日讯/生物谷BIOON/---下肢缺血是一种严重的临床症状,影响着全世界许多患者,目前尚无有效的治疗方法。缺血激活NLRP3炎性体,通过释放炎症性细胞因子IL-1β和IL-18触发组织损伤。然而,NLRP3炎性体激活的分子机制在很大程度上仍然未知。在一项新的研究中,来自中国苏州大学、广州医科大学、阜外医院、中山大学和吉林大学第二医院的研究人员
2021年4月14日讯/生物谷BIOON/---下肢缺血是一种严重的临床症状,影响着全世界许多患者,目前尚无有效的治疗方法。缺血激活NLRP3炎性体,进而通过释放炎症性细胞因子IL-1β和IL-18触发组织损伤。然而,NLRP3炎性体激活的分子机制在很大程度上仍然未知。
在一项新的研究中,来自中国苏州大学、广州医科大学、阜外医院、中山大学和吉林大学第二医院的研究人员利用RNA测序(RNAseq)比较了缺血的肌肉和正常肌肉的mRNA表达。RNAseq显示Rb1(retinoblastoma-1)、NLRP3炎性体、IL-1β和IL-18的mRNA水平增加(图1a,b),这一点在qRT-PCR实验中得到证实(图1c)。这些发现也通过Western blot(图1d)和ELISA(图1e)在蛋白水平上得到了验证。对这些上调的基因进行基因本体分析,揭示了缺血肌肉中与炎症反应途径和NLRP3炎性体相关的生物学过程,从而证实炎症相关信号通路参与缺血诱导的肌肉损伤(图1f)。为了验证RNAseq数据,这些作者还进行了蛋白测序。热图(heat map)和Spearman相关分析显示,缺血肌肉中Rb1、NLRP3、IL-1β和IL-18存在良好的蛋白-mRNA相关性。

Rb1蛋白是一种已知的肿瘤抑制蛋白,Rb1的失活会促进骨骼肌细胞的增殖,但是Rb1在缺血性肌肉损伤中的作用仍然未知。为了解决这个问题,这些作者构建出肌肉特异性Rb1基因敲除(Rb1-mKO)小鼠。在缺血性后肢损伤后,Rb1-mKO小鼠的血流恢复比对照组小鼠快。在损伤后28天时,Rb1-mKO小鼠的后肢握力、耐力以及骨骼肌与体重的比值也较高。这些结果表明,Rb1基因的丢失可以促进损伤后的骨骼肌修复。此外,Rb1-mKO小鼠肌肉中NLRP3和Caspase-1的蛋白表达以及IL-1β和IL-18的血浆水平均低于对照组小鼠,这表明Rb1基因的缺失导致NLRP3信号通路受到抑制。为了证实这些发现,他们通过用脂多糖(LPS)和ATP刺激C2C12成肌细胞(myoblast),建立了炎性体激活的体外模型。敲降Rb1(Rb1-siRNA)增强了细胞增殖,降低了NLRP3和Caspase-1的激活,并降低了IL-1β和IL-18的水平。
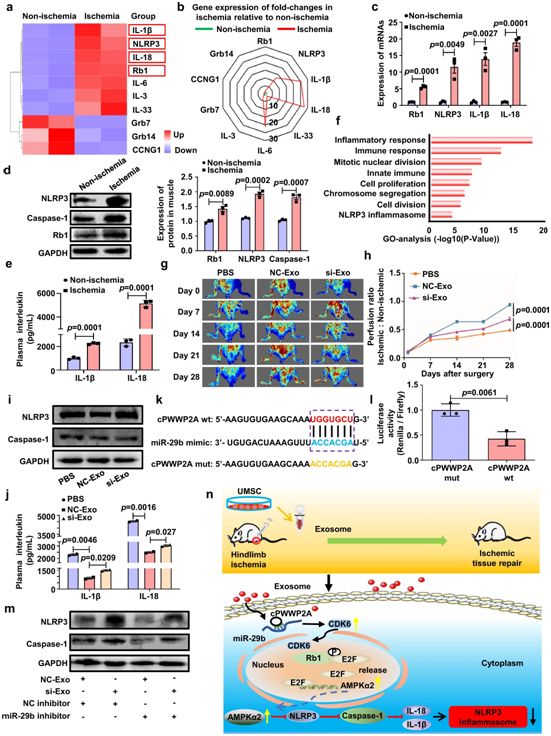
图1.肿瘤抑制蛋白Rb1是骨骼肌中的一种NLRP3炎性体诱导剂。图片来自Signal Transduction and Targeted Therapy, 2021, doi:10.1038/s41392-021-00520-8。
这些作者利用STRING数据库鉴定出调控Rb1的上游信号分子,发现它与CDK6和转录因子E2F相互作用。以前的研究已表明miR-29b靶向CDK6,因此他们研究了miR-29b是否调节CDK6/Rb1。正如Targetscan所示,CDK6 mRNA的3’UTR有miR-29b的多个结合位点,而且双荧光素酶实验证实CDK6是miRNA-29b的靶点。此外,miR-29b模拟物抑制了C2C12细胞中CDK6蛋白的表达和Rb1蛋白的磷酸化。
为了确定miR-29b是如何被调控的,这些作者使用环状RNA (circRNA)测序来比较缺血肌肉和正常肌肉中circRNA的表达。在缺血肌肉中检测到几种促进细胞增殖的circRNA(cPWWP2A、circ_CCDC66和circ_HECTD1)。在这些circRNA中,cPWWP2A的表达最强,但在缺血条件下,它的表达量急剧下降。这些发现在qRT-PCR实验中得到证实。
由于干细胞衍生的外泌体可以促进组织修复,这些作者将对照外泌体(NC-Exos)或沉默cPWWP2A表达的外泌体(si-Exos)注入缺血肌肉,以确定cPWWP2A是否参与介导源自人脐带衍生间充质干细胞(UMSC)的外泌体(UMSC-Exos)在肌肉中的有益作用。NC-Exos处理导致肌肉中cPWWP2A的表达增加,而si-Exos减弱了这种表达。与注射NC-Exos的小鼠相比,si-Exos处理导致血流恢复较慢 (图1g、h),运动功能较差,肌肉力量和跑步距离减少,肌肉与体重比降低,NLRP3、Caspase-1表达较高(图1i),血浆中IL-1β和IL-18水平增加(图1j)。这些注射到小鼠体内的外泌体直径为30~100nm,仅在肌肉中检测到。与转染NC-Exos的细胞相比,转染si-Exos的C2C12细胞中NLRP3和Caspase-1的表达量明显更高。因此,在si-Exos处理后,IL-1β和IL-18的水平增加了,并且细胞增殖受到抑制。
这些作者基于CircBank分析确定了miR-29b和cPWWP2A之间的相互作用(图1k)。cPWWP2A和miR-29b之间的联系在双荧光素酶实验中得到证实,该实验显示miR-29b与cPWWP2A存在较强的结合(图1l)。miR-29b在缺血肌肉中的表达增加了,这与cPWWP2A的表达相反。这些结果表明,cPWWP2A是miR-29b的分子海绵(molecular sponge)。为了验证cPWWP2A/miR-29b调控NLRP3信号通路,用miR-29b抑制剂处理C2C12细胞,这降低了NLRP3和Caspase-1的表达以及IL-1β和IL-18的释放,但增强了C2C12细胞增殖,不过这些效应可被si-Exos逆转(图1m)。相应地,敲降C2C12细胞中的cPWWP2A导致CDK6 mRNA和蛋白的表达减少。此外,C2C12细胞的分化被cPWWP2A siRNA抑制,但被miR-29b抑制剂激活。这些数据表明,cPWWP2A通过miR-29b/CDK6途径调节Rb1。
以前的研究已表明,Rb1的下调导致E2F转录因子的释放,进而激活AMP激酶α2(AMPKα2)的转录。
AMPKα2抑制平滑肌细胞中NLRP3的激活。这些作者试图确定Rb1是否调节骨骼肌中AMPKα2的表达。他们的数据显示,Rb1-mKO小鼠中AMPKα2 mRNA和蛋白的表达增加。AMPKα2沉默导致NLRP3和Caspase-1的表达增加,IL-1β和IL-18在细胞上清液中的释放增加,细胞增殖减少。此外,在肌肉中注射AMPKα2 siRNA可增加肌肉中NLRP3、Caspase-1、IL-1β和IL-18的mRNA表达,NLRP3和Caspase-1的蛋白表达,以及小鼠血浆中IL-1β和IL-18的水平。这些数据表明,Rb1的下调通过激活AMPKα2来抑制NLRP3的激活。
综上所述,Rb1蛋白是一种已知的肿瘤抑制蛋白,但是这些作者发现它在骨骼肌中作为NLRP3炎症体诱导剂起作用。他们进一步证实,下调Rb1可通过E2F/AMPKα2介导的信号通路阻止NLRP3炎性体的激活。Rb1被CDK6失活,而CDK6是miR29b的下游靶点。在缺血肌肉中,miR29b的水平增加,导致CDK6的表达减少和Rb1的过度激活。因此,他们破解了一种新的机制,即通过cPWWP2A/Rb1/AMPKα2/NLRP3信号通路调节NLRP3炎性体(图1n)。重要的是,他们发现,UMSC-Exos可以补充缺血肌肉中cPWWP2A的丢失。因此,Rb1基因敲除方法可以通过使用释放cPWWP2A以促进肌肉修复的UMSC-Exos转化为临床应用。(生物谷 Bioon.com)
参考资料:
Yanli Wang et al. Stem cell-derived exosomes repair ischemic muscle injury by inhibiting the tumor suppressor Rb1-mediated NLRP3 inflammasome pathway. Signal Transduction and Targeted Therapy, 2021, doi:10.1038/s41392-021-00520-8.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


