Journal for ImmunoTherapy of Cancer:抗凝治疗可通过缓解缺氧促进肿瘤免疫微环境并增强免疫治疗疗效
来源:生物谷 2021-08-27 22:03
有限的肿瘤灌注会导致药物输送受损、氧合不足并对肿瘤微环境(TME)产生不利影响,从而降低化疗、免疫治疗、放疗和纳米医学等的疗效,灌注受限最难以克服的后果是肿瘤缺氧。
有限的肿瘤灌注会导致药物输送受损、氧合不足并对肿瘤微环境(TME)产生不利影响,从而降低化疗、免疫治疗、放疗和纳米医学等的疗效,灌注受限最难以克服的后果是肿瘤缺氧。TME中的缺氧通过癌细胞、免疫细胞和分泌细胞因子的复杂相互作用发挥免疫调节作用,因此,人们越来越关注通过呼吸高氧、氧合等策略来改善肿瘤氧合药物或缺氧诱导因子(HIF)抑制剂来减少免疫抑制,缓解肿瘤缺氧可能是增强抗肿瘤免疫和免疫治疗药物疗效的有吸引力的策略。癌症相关血栓形成(CAT)在大多数实体瘤中很常见,但其对肿瘤组织中血液灌注和缺氧的影响被极大地低估了,因此,研究者假设血管中形成血凝块和肿瘤的间质区域充当主要的运输屏障,减少肿瘤灌注并加重缺氧,认为持续使用适当的抗凝剂可以缓解缺氧,使TME变得更具免疫支持性,这也将增强免疫治疗的疗效。
图片来源:http://dx.doi.org/10.1136/jitc-2021-002332
低分子量肝素(LMWH)在临床上被广泛用作癌症患者CAT的治疗选择,然而,由于它不能口服,直接口服抗凝剂(DOAC)越来越多地用作治疗CAT替代LMWH的共识指南。为了克服这一限制并进一步改善其药代动力学,研究者之前开发了一种口服活性肝素偶联物,即STP3725作为一种新的DOAC,它是依诺肝素和四聚脱氧胆酸盐的结合物,发现STP3725具有口服活性,大鼠的口服生物利用度为26.3%,并且其给药成功地防止了动物模型中VTE的形成。研究者在该研究中验证了他们的假设,即CAT是一个主要的屏障,可以限制肿瘤灌注并加重肿瘤缺氧,还验证了STP3725是通过减少缺氧和培养支持免疫的微环境来增强免疫疗法的功效。
CAT加重缺氧同时减少免疫细胞浸润 图片来源:http://dx.doi.org/10.1136/jitc-2021-002332
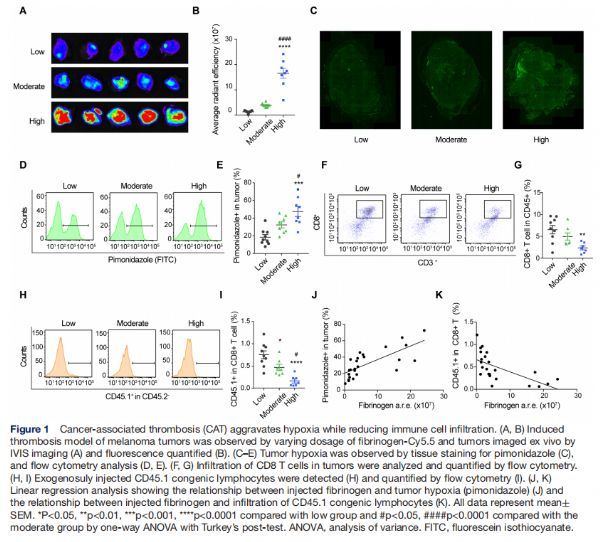
在高度血栓形成的B16F10.OVA黑色素瘤(卵清蛋白转染的B16F10黑色素瘤)携带C57BL/6小鼠中,通过注射荧光标记的纤维蛋白原建立诱导血栓形成模型。纤维蛋白原-Cy5.5剂量从低、中到高不等,通过IVIS(体内成像系统)成像显示相应的荧光模式并被量化,结果显示“高”组与“低”组相比增加了12.30倍;通过免疫荧光染色和流式细胞术,匹莫硝唑检测肿瘤缺氧显示与纤维蛋白原-Cy5.5量相关的模式增加,与“低”组相比,“高”组增加了 2.58 倍。肿瘤内CD8+ T细胞的检测显示与注射的纤维蛋白原-Cy5.5呈负相关;定量流式细胞术分析显示,与“低”组相比,“高”组的T细胞数量减少了2.76倍。类似地,在携带黑色素瘤的野生型小鼠的收获肿瘤中检测到外源注射CD45.1+同类T淋巴细胞,显示新浸润淋巴细胞的减少模式,量化值显示“高”组与“低”组相比减少了4.56倍。进一步对注射纤维蛋白原与肿瘤缺氧(匹莫硝唑)的关系进行线性回归分析,结果表明它们呈正相关,而注射纤维蛋白原与CD45.1+同类淋巴细胞浸润呈负相关。这些结果表明,这种诱导血栓形成模型显示出CAT施加的肿瘤缺氧,并且这种纤维蛋白原介导的有限肿瘤灌注显示出相应的肿瘤缺氧模式和现有的、新引入的淋巴细胞的肿瘤浸润。
抗凝治疗增强肿瘤灌注并减少缺氧 图片来源:http://dx.doi.org/10.1136/jitc-2021-002332
研究者在同一黑色素瘤模型中,进行了各种实验以研究抗凝治疗对肿瘤灌注和缺氧的影响,P选择蛋白敲除(Psel-/-)小鼠用于阴性对照,因为P选择蛋白对于CAT的形成至关重要。对对照组、P sel-/-、依诺肝素和STP3725处理的小鼠进行了血栓评估发现,野生型小鼠的血栓发生率最高。此外,在该模型中使用三维(3D)多普勒分析来可视化和量化B16F10中肿瘤组织的灌注发现,STP3725给药增加了肿瘤组织中的断面血流量和总血量。STP3725增强了肿瘤灌注,随后减少了肿瘤缺氧,通过流式细胞术分析显示,与对照相比,STP3725治疗的小鼠中缺氧(哌莫硝唑+)细胞减少了44.39±7.64%;通过对肿瘤组织进行GLUT-1染色也发现,在缺氧条件下过度表达,STP3725治疗小鼠的肿瘤染色显著减少35.06±4.32%;使用FMISO染料通过PET/MR观察到肿瘤缺氧的实时成像,结果表明与对照相比,STP3725使SUVR(标准化摄取值/区域)值降低了27.27±5.55%。研究者得出结论,使用抗凝治疗预防CAT可以成为增强肿瘤灌注同时减轻缺氧的有效策略。
该研究系统地验证了CAT作为主要的灌注屏障,它限制了肿瘤中的氧气供应,使用口服抗凝治疗预防CAT有效减少缺氧。
CAT形成是肿瘤发展过程中持续存在的不可避免的因素,临床上积极探索治疗癌症患者CAT的方法,因此,利用其作为灌注限制屏障的作用作为由抗凝剂和免疫疗法组成的联合方案的目标是有吸引力的。由于抗凝治疗可用于增强免疫治疗的疗效,口服活性依诺肝素STP3725可以通过预防CAT来增强肿瘤灌注和缓解缺氧,通过培养支持免疫的微环境来帮助提高免疫疗法的疗效,还可与其他缺氧缓解策略联合使用,在增强抗肿瘤免疫方面发挥协同作用。该策略具有将抗凝治疗的组合标准扩展到其他类型的免疫治疗的巨大潜力,并且非常适合临床转化。(生物谷 bioon)
参考文献
Jeong Uk Choi et al. Anticoagulation therapy promotes the tumor immune-microenvironment and potentiates the efficacy of immunotherapy by alleviating hypoxia. Journal for ImmunoTherapy of Cancer (2021 Aug 02) doi:http://dx.doi.org/10.1136/jitc-2021-002332
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。