Sci Adv:中国科学家发现有望治疗人类卵巢癌的潜在选择性小分子抑制剂
来源:生物谷原创 2023-11-30 10:21
来自上海交通大学等机构的科学家们通过研究识别出了有望治疗卵巢癌的潜在治疗性靶点和临床前候选药物。
转录失调是卵巢癌复发的病理学标志,同时也是一种新出现的治疗易感性靶点;近日,一篇发表在国际杂志Science Advances上题为“Therapeutic targeting of CPSF3-dependent transcriptional termination in ovarian cancer”的研究报告中,来自上海交通大学等机构的科学家们通过研究识别出了有望治疗卵巢癌的潜在治疗性靶点和临床前候选药物,文章中,研究人员开发出了一种名为CPSF3的新型小分子抑制剂,其或能作为理解和聚腺苷酸化的特异性因子(CPSF,cleavage and polyadenylation specificity factor)复合体的关键模块,来催化前mRNA的剪接并调节转录终止反应。
卵巢癌是一种最致命的妇科癌症,其通常在晚期阶段才会被诊断出来,在治疗卵巢癌的过程中,手术和全身性的化疗能适度改善患者的生存率,而基于PARP抑制剂的靶向性疗法仅对有限数量的卵巢癌患者有效;卵巢癌通常会以频繁的拷贝数改变和基因表达失调为主要特征,这就会使得转录成为药物疗法的潜在攻击点。
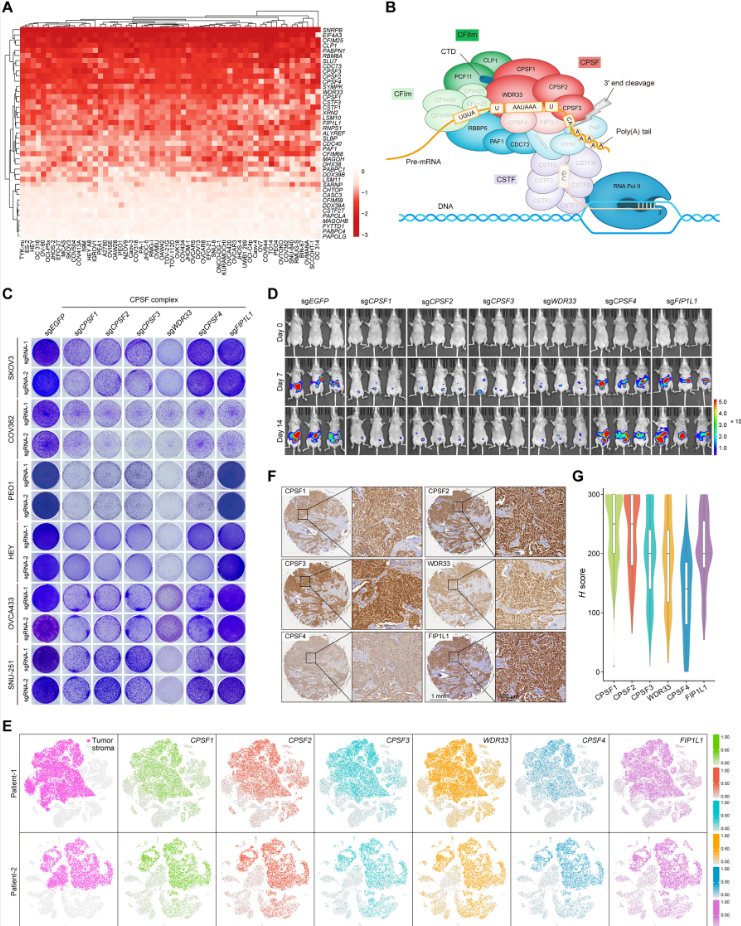
中国科学家发现有望治疗人类卵巢癌的潜在选择性小分子抑制剂。
图片来源:Science Advances (2023). DOI:10.1126/sciadv.adj0123
这项研究中,研究人员通过联合研究系统性地调查了卵巢癌中CPSF复合体的调节性功能,并发现卵巢癌能独特地依赖于转录终止机制,其中CPSF3的内切酶活性是不可或缺的。有了这些研究发现,研究人员就能通过寻找能在细胞和体内药理性地干预CPSF3酶类活性的小分子抑制剂,从而来验证CPSF3是否能作为一种潜在的治疗性靶点;基于已经报道的抗菌或抗肿瘤药物能共享一种共同的benzoxaborole分子片段,于是研究人员就推测,oxaborole基团或许能协调CPSF3的催化锌离子。
基于这些研究结果,研究人员最终开发出了一种潜在的、选择性地、生物可利用性且可耐受的CPSF3抑制剂(包括HQY426),后一种抑制剂及其类似物能在多种卵巢癌细胞系中展现出较强的抗增殖效应,且能单独使用、与顺铂或PARP抑制剂联合使用时在体内有效抑制卵巢癌肿瘤的生长。相比之下,此前报道的CPSF3抑制剂几乎是无活性的,此外,CPSF3催化位点中关键残基的点突变就足以介导卵巢癌细胞对HQY426及其类似物的耐受性,这就进一步证实了这些靶向性抑制剂的特异性。
综上,本文研究结果表明,研究人员所发现的抑制剂或能帮助确立CPSF3依赖性的转录终止或许就是卵巢癌对治疗干预措施易感的关键机制,同时还有望为开发靶向性抗癌药物疗法提供一种有前途的含硼引导物。(生物谷Bioon.com)
原始出处:
PEIYE SHEN,KAIYAN YE,HUAIJIANG XIANG, et al. Therapeutic targeting of CPSF3-dependent transcriptional termination in ovarian cancer, Science Advances (2023). DOI:10.1126/sciadv.adj0123
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


