默克PD-L1单抗一线治疗肾细胞癌III期研究未达到OS主要终点
来源:医药魔方 2024-05-24 09:30
阿维鲁单抗是默克开发的一款PD-L1单抗,于2017年3月首次在美国获批上市。2019年5月,FDA基于JAVELIN Renal 101研究的中期积极数据批准阿维鲁单抗联合阿昔替尼用于一线治疗肾细胞
5月23日,默克在ASCO 2024网站上公布了阿维鲁单抗联合阿昔替尼治疗肾细胞癌的III期JAVELIN Renal 101研究最新数据。结果显示,患者在接受该联合疗法治疗后,其总生存期(OS)未实现显著延长。
该研究是一项多中心、随机、开放标签临床试验(n=886),评估了阿维鲁单抗联合阿昔替尼对比舒尼替尼一线治疗晚期肾细胞癌患者的疗效和安全性。研究的主要终点为无进展生存期(PFS)和OS。
该研究的PFS终点已于2019年达到。在总体人群中,阿维鲁单抗联合阿昔替尼组患者的PFS相比舒尼替尼组显著延长(13.8 vs. 8.4个月,HR=0.69,P<0.001);在PD-L1+人群中,阿维鲁单抗联合阿昔替尼组患者的PFS相比舒尼替尼组亦显著延长(13.8 vs. 7.2个月,HR=0.61,P<0.001)。
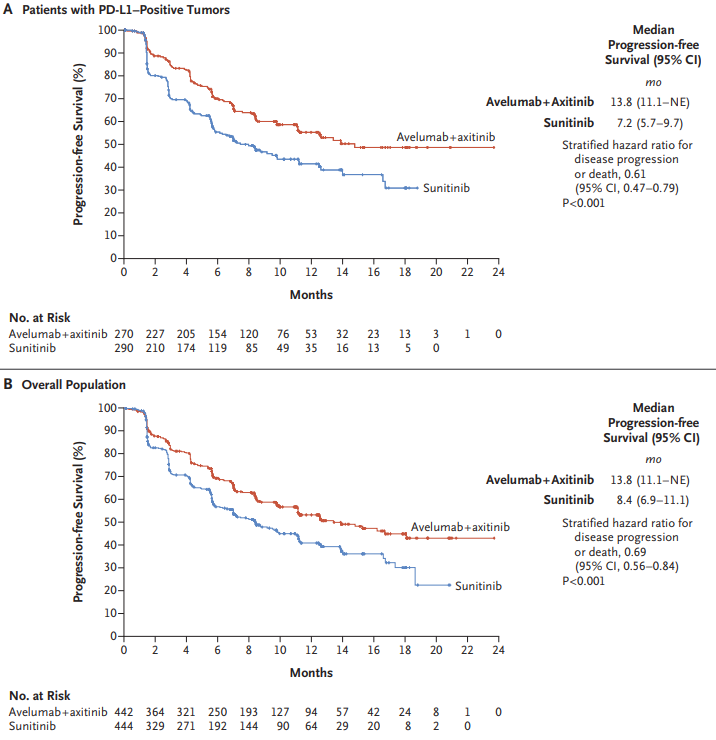
来源:NEJM
此次更新的数据显示,截至2023年8月31日,在总体人群中,阿维鲁单抗联合阿昔替尼组患者的PFS相比舒尼替尼组显著延长(13.9 vs. 8.5个月,HR=0.66,P<0.0001),但OS数据无显著性差异(44.8 vs. 38.9个月,HR=0.88,P=0.067);在PD-L1+人群中,阿维鲁单抗联合阿昔替尼组患者的PFS相比舒尼替尼组亦显著延长(13.9 vs. 8.2个月,HR=0.57,P<0.0001),OS数据同样无显著性差异(43.2 vs. 36.2个月,HR=0.86,P=0.076)。
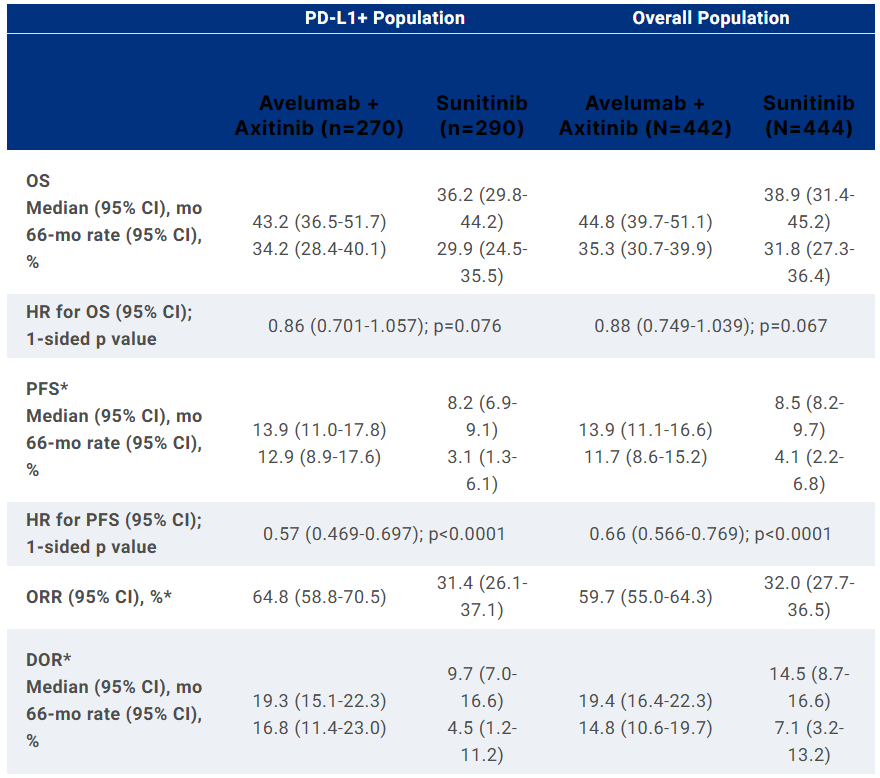
来源:ASCO 2024
安全性方面,阿维鲁单抗联合阿昔替尼组和舒尼替尼组患者发生3级治疗相关不良事件(TRAE)的比例分别为66.8%和61.5%。
阿维鲁单抗是默克开发的一款PD-L1单抗,于2017年3月首次在美国获批上市。2019年5月,FDA基于JAVELIN Renal 101研究的中期积极数据批准阿维鲁单抗联合阿昔替尼用于一线治疗肾细胞癌患者。
目前,PD-1/PD-L1赛道仅阿维鲁单抗、帕博利珠单抗、特瑞普利单抗和纳武利尤单抗4款药物获批用于一线治疗肾细胞癌。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


