Cell子刊:井然等人揭示增强iPSC-CAR-T细胞抗肿瘤效果新方法
来源:生物世界 2024-11-12 14:45
组蛋白赖氨酸甲基转移酶G9a/GLP是T细胞命运的抑制因子,化学抑制G9a/GLP能够诱导人iPSC来源的CAR-T细胞的成熟和持久性,从而产生更强、更持久的抗肿瘤活性。
哈佛大学医学院George Daley团队(井然博士为第一作者)在 Cell 子刊 Cell Stem Cell 上发表了题为Maturation and persistence of CAR T cells derived from human pluripotent stem cells via chemical inhibition of G9a/GLP 的研究论文。
该研究发现,组蛋白赖氨酸甲基转移酶G9a/GLP是T细胞命运的抑制因子,化学抑制G9a/GLP能够诱导人iPSC来源的CAR-T细胞的成熟和持久性,从而产生更强、更持久的抗肿瘤活性。

该团队此前开发了一种完全不依赖基质细胞的T细胞分化平台,这有效简化了iPSC到T细胞的分化流程,显著提高了分化效率和成熟度,为后续的高通量筛选奠定了基础。
在这项最新研究中,研究团队使用上述不依赖基质细胞的人iPSC-T细胞分化平台,筛选了影响T细胞分化的表观遗传调控因子,确定了组蛋白赖氨酸甲基转移酶G9a/GLP作为T细胞命运的抑制因子。
该研究发现,在造血干细胞/祖细胞(HSPC)分化的特定时间窗内,G9a/GLP的抑制可使细胞命运向淋巴系倾斜。抑制G9a/GLP促进了斑马鱼胚胎造血过程中淋巴样细胞的产生,这表明了G9a/GLP功能在进化上的保守性。
更重要的是,化学抑制G9a/GLP有助于成熟的iPSC-T细胞的产生,而iPSC-T细胞具有与外周血αβ T细胞相似的转录特征。
通过基因工程改造表达嵌合抗原受体(CAR)后,经过表观遗传工程改造的iPSC-CAR-T细胞在体外表现出增强的效应功能,并且在异种移肿瘤再挑战模型中表现出持久的抗肿瘤活性。
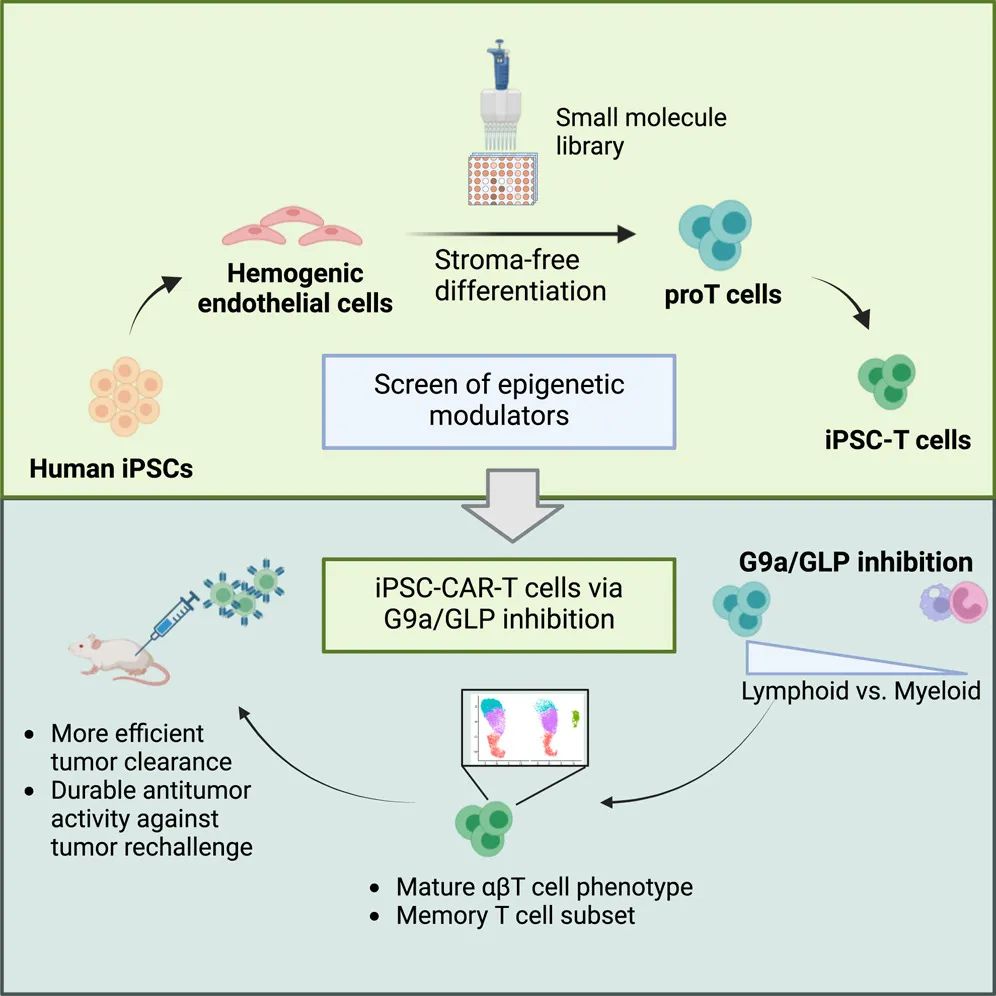
该研究的核心发现:
-
化学筛选确定iPSC-T细胞分化的表观遗传调节因子;
-
G9a/GLP影响iPSC来源的血源性内皮细胞的淋巴样分化;
-
在T细胞分化过程中抑制G9a/GLP产生成熟的iPSC-T细胞;
-
通过G9a/GLP抑制获得的CAR iPSC-T细胞显示出更强的抗肿瘤活性。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


