Immunity:组织驻留Treg——定植特化模型vs 泛组织模型
来源:生物探索 2024-10-01 10:46
这项研究揭示组织间Treg表型和TCR相似且定居时间较短,并提出组织驻留Treg的泛组织迁移模型,为组织驻留Treg的认知提供另一种理解。
组织驻留性免疫细胞对维持机体稳态和对抗感染具有重要意义。然而,我们对于组织驻留免疫细胞的构成和特性仍缺乏足够的理解。关于组织驻留免疫细胞的认识大多来自巨噬细胞的研究,在胚胎发育早期,造血祖细胞种植在各种组织并特化发育为独特的巨噬细胞【1】。
组织驻留性记忆细胞(tissue-resident memory,Trm)的发现打破了αβT细胞的循环迁移模型【2】。抗原经历的记忆T细胞会长期甚至无限期停留在抗原暴露组织,一旦抗原再次出现迅速做出应答反应。近几年,多篇文献报道组织驻留Treg的重要作用【3】,例如脂肪Treg的维持机体代谢稳态作用【4,5】、肌肉Treg参与肌肉修复【6】、脑Treg驱动少突胶质细胞分化、皮肤Treg抑制纤维化【7,8】和子宫Treg促进胎儿生长【9】等。在表型上类似于Trm,组织Treg同样表达CD69、CD103、CD11a和PD-1。虽然这种相似性支持组织Treg的定植特化模型,但尚缺乏直接的数据。
近日,英国剑桥大学病理学系Adrian Liston研究团队在Immunity杂志在线发表题为The tissue-resident regulatory T cell pool is shaped by transient multi-tissue migration and a conserved residency program的研究文章。该研究通过高维流式细胞术、TCR-seq、RNA-seq和parabiosis分析,向传统定植特化的长期驻留模型发起挑战,提出组织驻留Treg的泛组织迁移模型,为组织Treg提供另一种理解。

团队首先在小鼠的48个组织中分析Treg的浸润和表型,包括淋巴、非淋巴和肠相关组织。结果发现Treg在各组织占CD4+T细胞的10-20%,在骨髓、皮肤和舌头占比上升到50%。在绝对数量上,淋巴组织Treg为104-107,肠相关组织为103-105,非淋巴组织为10-104。整体上看,淋巴组织Treg占机体Treg的98%,肠相关组织为0.8%,非淋巴组织为0.3%。
流式降维分析将Treg分为5群,包括血液、淋巴、骨髓、组织和肠相关Treg,这种分群大致反应解剖位置,但也存在例外如胃Treg聚类到组织Treg。进一步分析发现组织Treg基本为活化和CD69+Treg,包括ST+和KLRG1+群。值得注意的是,这些表型在不同组织间基本无差别。总之,这些数据表明几乎所有组织存在Treg,且在非淋巴非肠道组织Treg表型相似。随后,作者探究性别、年龄和肠道菌群对组织Treg的影响。结果发现Treg表型在雌雄之间几乎无差别,除了雌性唾液腺Treg增加而雄性白色脂肪Treg增加;而组织Treg在老龄小鼠中增加5-20倍,增加最多的是白色脂肪组织和肝脏。除了白色脂肪组织和肌肉,Treg占CD4+T细胞的比例基本稳定,表明Treg的增加可能是由于整体CD4+T细胞的炎性扩增;除了骨髓和肠道粘膜固有层趋势相反,大部分组织Treg随肠道菌群复杂性增加而增加。Treg表型除了ICOS表达随菌群复杂性增加而增加外其余表达稳定。这些数据表明组织Treg数量受年龄和肠道菌群影响,但Treg表型较为稳定。
作者分离各个组织Treg行RNA-seq分析,包括血液、淋巴组织(脾脏、淋巴结和派氏结)、肠相关组织(上皮间白细胞和黏膜固有层)和非淋巴非肠道组织(肝、肺、胰腺和肾)。结果表明肠相关Treg和非淋巴组织Treg在转录组上相似,且各个非淋巴组织Treg也呈现高度相似特征。之后,团队分析组织驻留相关基因,包括CD69、ST2、KLRG1、CD103、Blimp、BATF、CD11a、S1PR2、Areg和HIF1α,对组织Treg的影响。通过WT小鼠和上述基因缺失小鼠构建1:1嵌合小鼠,作者发现除了Blimp和BATF3,其余组织浸润相关基因对组织Treg影响较小,且观察到的差异也是泛组织而非组织特异。这些结果说明组织Treg不仅有统一的表型,同时也分享相同的组织驻留关键分子。
这种表型和分子依赖的相似性是由于Treg的多样性被抑制还是组织驻留时间有限?为此,作者构建多时间点的CD45.1-CD45.2 parabiosis模型,结果发现在淋巴组织,CD69+Treg在淋巴结停留3天,脾脏17天、肠系膜淋巴结4周;在非淋巴组织,CD69+Treg平均停留3周,白色脂肪组织则达到8周;肠相关Treg停留时间为7-8周。在平均停留3周后,大多数CD69+Treg离开组织。总之,这些结果表明组织驻留Treg在组织停留时间较短,并支持活化Treg进入-短暂停留-离开的循环迁移模型。
尽管上述数据不支持Treg的长期驻留,但仍可能存在两种情况。1. 克隆限制的循环迁移,即克隆限制Treg在一个组织和淋巴组织之间循环迁移。2. 泛组织迁移模型,即Treg在多个组织循环迁移。作者首先评价组织Treg的TCR克隆性,结果发现非淋巴组织驻留Treg具有高度克隆共享。相反,肠黏膜固有层Treg的TCR在非肠道组织很少观察到。随后,作者挑选组织Treg的TCR并通过编码联合逆转录病毒对造血干细胞进行逆基因再表达并过继入小鼠体内,发现60%逆基因再表达细胞分化为Treg且大部分Treg均遵循泛组织迁移模型,仅少数TCR有组织特异性分布倾向。总之,这些数据支持泛组织Treg迁移驻留模型。
综上所述,这项研究揭示组织间Treg表型和TCR相似且定居时间较短,并提出组织驻留Treg的泛组织迁移模型,为组织驻留Treg的认知提供另一种理解。
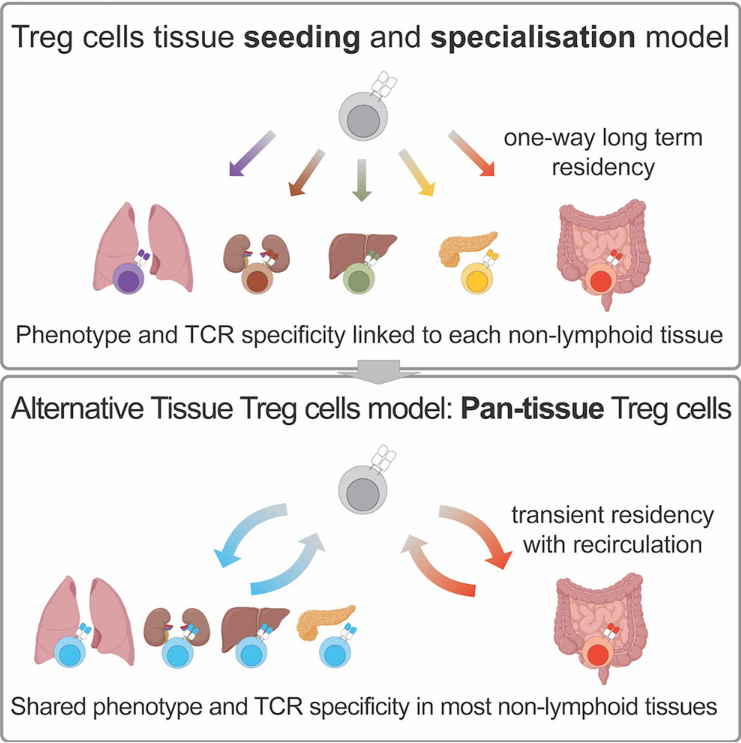
模式图(Credit: Immunity)
1. Florent, Ginhoux., Martin, Guilliams.(2016). Tissue-Resident Macrophage Ontogeny and Homeostasis. Immunity, 44(3), 0. doi:10.1016/j.immuni.2016.02.024
2. Marcus, Buggert., David A, Price., Laura K, Mackay., Michael R, Betts.(2023). Human circulating and tissue-resident memory CD8(+) T cells. Nat Immunol, 24(7), 0. doi:10.1038/s41590-023-01538-6
3. Andrés R, Muñoz-Rojas., Diane, Mathis.(2021). Tissue regulatory T cells: regulatory chameleons. Nat Rev Immunol, 21(9), 0. doi:10.1038/s41577-021-00519-w
4. Markus, Feuerer., Laura, Herrero., Daniela, Cipolletta., Afia, Naaz., Jamie, Wong., Ali, Nayer., Jongsoon, Lee., et al.(2009). Lean, but not obese, fat is enriched for a unique population of regulatory T cells that affect metabolic parameters. Nat Med, 15(8), 0. doi:10.1038/nm.2002
5. Tianli, Xiao., P Kent, Langston., Andrés R, Muñoz-Rojas., Teshika, Jayewickreme., Mitchell A, Lazar., Christophe, Benoist., Diane, Mathis.(2022). T(regs) in visceral adipose tissue up-regulate circadian-clock expression to promote fitness and enforce a diurnal rhythm of lipolysis. Sci Immunol, 7(75), 0. doi:10.1126/sciimmunol.abl7641
6. Dalia, Burzyn., Wilson, Kuswanto., Dmitriy, Kolodin., Jennifer L, Shadrach., Massimiliano, Cerletti., Young, Jang., Esen, Sefik., Tze Guan, Tan., Amy J, Wagers., Christophe, Benoist., Diane, Mathis.(2013). A special population of regulatory T cells potentiates muscle repair. Cell, 155(6), 0. doi:10.1016/j.cell.2013.10.054
7. Lokesh A, Kalekar., Jarish N, Cohen., Nicolas, Prevel., Priscila Muñoz, Sandoval., Anubhav N, Mathur., et al.(2019). Regulatory T cells in skin are uniquely poised to suppress profibrotic immune responses. Sci Immunol, 4(39), 0. doi:10.1126/sciimmunol.aaw2910
8. Niwa, Ali., Bahar, Zirak., Robert Sanchez, Rodriguez., Mariela L, Pauli., Hong-An, Truong., Kevin, Lai., Richard, et al.(2017). Regulatory T Cells in Skin Facilitate Epithelial Stem Cell Differentiation. Cell, 169(6), 0. doi:10.1016/j.cell.2017.05.002
9. Florez, L.M., Fourcade, G., Darrassse-Je` ze, G., Barennes, P., GanFernandez, K., Re´ gnier, P., Nehar-Belaid, D., et al. (2023). Tissue-resident uterine regulatory T cells support fetal growth. Preprint at bioRxiv. https://doi.org/10.1101/2023.09.07.554921.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


