Theranostics: DDR抑制剂可以为改善神经内分泌肿瘤患者提供有希望的途径
来源:生物谷原创 2023-12-26 14:58
使用177lutetium - dota - octreoate (LuTate)治疗神经内分泌肿瘤(NET)的肽受体放射性核素疗法(PRRT)目前已在许多国家获得批准,尽管原发性或继发性耐药性继续限
使用177lutetium - dota - octreoate (LuTate)治疗神经内分泌肿瘤(NET)的肽受体放射性核素疗法(PRRT)目前已在许多国家获得批准,尽管原发性或继发性耐药性继续限制其有效性或持久性。研究者假设全基因组CRISPR/Cas9筛选将确定对LuTate和基因靶点的关键反应介质,这可能为NET患者提供新的联合治疗机会。

图片来源:https://pubmed.ncbi.nlm.nih.gov/37771787/
近日,来自彼得·麦卡勒姆癌症中心的研究者们在Theranostics.杂志上发表了题为“A genome-wide CRISPR/Cas9 screen identifies DNA-PK as a sensitiser to 177Lutetium-DOTA-octreotate radionuclide therapy”的文章,该研究表明DDR抑制剂,特别是DNA-PK抑制剂,可以为改善NET患者对PRRT的反应提供有希望的途径。
研究者在LuTate处理的细胞中使用全基因组CRISPR-Cas9筛选来鉴定影响细胞对LuTate的敏感性或抗性的基因。通过单基因敲除验证命中。评估了LuTate耐药细胞,以确认LuTate摄取和保留,以及生长抑素受体2 (SSTR2)表达的持久性。通过使用特定抑制剂的药理学致敏以及这些抑制剂与LuTate联合的体内疗效分析,进一步表征了赋予LuTate敏感性的基因敲除。
研究结果表明:CRISPR-Cas9筛选确定了对PRRT具有抗性和敏感性的几个潜在靶点。体外产生LuTate抗性的两个基因敲除,ARRB2和MVP,分别具有与LuTate结合和保留以及dna损伤修复(DDR)途径调节相关的潜在机制。
筛选显示,体外对LuTate治疗的敏感性可以通过丢失多种参与DDR通路的基因来获得,其中涉及非同源末端连接(Non-Homologous End-Joining, NHEJ)的基因丢失是最致命的。由于基因丢失或两种不同抑制剂的抑制,NHEJ关键基因PRKDC (DNA-PK)的丢失导致细胞暴露于LuTate后细胞存活率显著降低。在sstr2阳性的携带异种移植物的小鼠中,与单独使用LuTate相比,nedisertib(一种DNA-PK特异性抑制剂)和LuTate联合使用对肿瘤生长和生存率的控制更强。
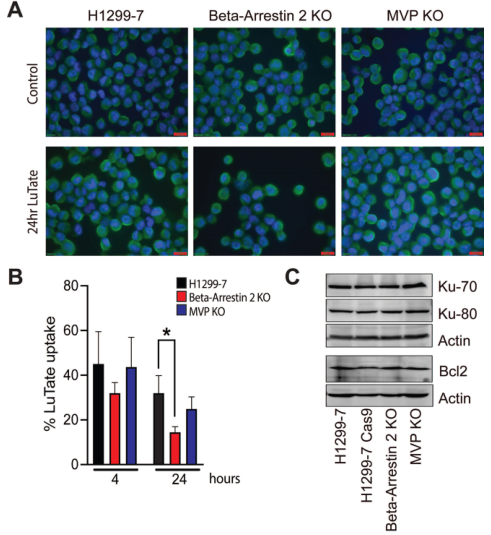
评估β -抑制蛋白2和MVP丢失时可能导致对LuTate产生耐药性的机制
图片来源:https://pubmed.ncbi.nlm.nih.gov/37771787/
综上所述,DDR通路对于感知和修复辐射诱导的DNA损伤至关重要,DDR通路的调控可能涉及对PRRT的抗性和敏感性。此外,在临床前模型中,DNA-PK抑制剂联合LuTate PRRT显著提高了治疗效果,进一步证明了该联合治疗的临床疗效。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


