“蜘蛛侠”跨界科研!蜘蛛丝竟能稳定P53,增加抗癌能力
来源:生物谷原创 2022-04-03 13:10
前一段时间,《蜘蛛侠:英雄无归》刷爆朋友圈,让一众影迷直呼过瘾。
前一段时间,《蜘蛛侠:英雄无归》刷爆朋友圈,让一众影迷直呼过瘾。
However,无论蜘蛛侠在漫威的世界里归不归,我们的漫漫科研之路却始终都要回归到Article 上。
最近,一篇最新发表在Cell子刊Structure 的文章《A "spindle and thread" mechanism unblocks p53 translation by modulating N-terminal disorder》让我们看到了蜘蛛侠不仅能拯救地球,还能够在细胞里跟肿瘤“干架”,拯救我们的生命。下面,就让我们来仔细分解下“蜘蛛侠如何联名跨界科研圈”!

从标题中我们可以看到曾经大名鼎鼎的P53基因,在近几年火热的PD1/PDL1崛起之前,说起肿瘤基因,P53绝对是头一号热门词汇(在15年前,不懂P53基因出门都不好意思说自己是研究癌症的)。P53基因是控制细胞增殖的关键基因,在多达60%的人类癌症中都能发现P53突变失活的存在,因此如何恢复P53基因的正常功能成为治疗癌症的一个有效策略,本文正是从这一角度出发,在这一经典分子上做文章。
以往的研究多集中于如何纠正P53基因的DNA结合域来稳定细胞内P53基因。但是在本文中,作者创新性地使用融合蛋白这一思路通过融合一个强力的伴侣蛋白从而将p53蛋白稳定下来而免遭降解。基于这种思路,作者终于将目光么瞄向了“蜘蛛侠的拿手绝技”——蛛丝蛋白。蛛丝蛋白具有一个高度保守的N端结构域,并且非常容易聚集而不会被降解,这些特性使得作者考虑是否能够通过这些特性使得P53蛋白稳定下来而不被降解。
因此,在这篇文章中,作者利用蛛丝蛋白结构域的这种特性融合表达P53蛋白从而产生了一种稳定表达的具有生物活性蛛丝-P53蛋白突变体,这种稳定的蛋白策略有望用于开放新的药物和结构生物学研究。
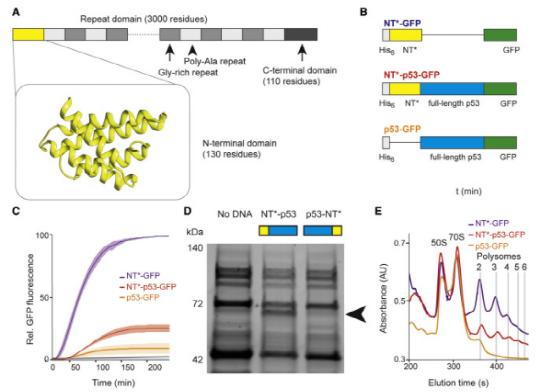
Figure 1. NT∗ increases the translation efficiency of p53
翻译水平是蛋白表达的直接表现,因此作者首先评估了对蛛丝蛋白结构域对P53基因翻译的影响。作者将蛛丝蛋白结构域,P53全长和GFP进行融合表达,进而通过检测GFP荧光强度的变化来表征p53转录和翻译水平的变化。该方法可以比较真实的反映蛛丝-p53融合蛋白的翻译效率。结果发现在只有在p53N端连接的蛛丝蛋白结构域可以增加P53体外翻译水平。进一步作者又对比P53-GFP和蛛丝-P53-GFP蛋白表达间核糖体活性的差异确实了融合表达蛛丝蛋白能够增加P53翻译水平。
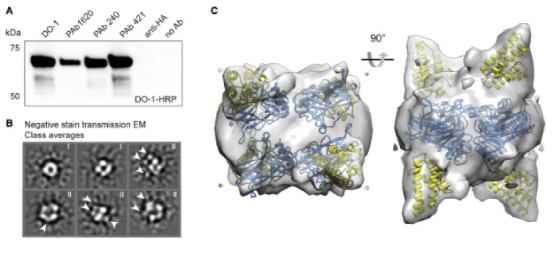
Figure 2. The TEM structure of the NT∗-p53 fusion protein
蛛丝-p53融合表达的高产让作者进一步去思考:融合蛋白是如何影响p53原本的蛋白结构。因此,作者纯化出了蛛丝-p53融合蛋白进行了蛋白结构分析,通过戊二醛交联蛋白和Western Blot实验发现蛛丝蛋白结构域的存在并不会已共享原本P53蛋白的结构构象和寡聚形式。此外,由于以往对于P53蛋白折叠的核心结构域的研究虽然较多,其反式激活结构域的方向一直难以确定。因此,作者推测额外的蛛丝标签可以使得我们对p53蛋白反式激活结构域的方向有所了解。通过投射电镜作者对蛛丝-p53融合蛋白中蛛丝标签的方向就行了确定,结果发现蛛丝蛋白结构域与p53蛋白的四个DNA结合域密切相关且p53的N端区域没有在其中延伸。
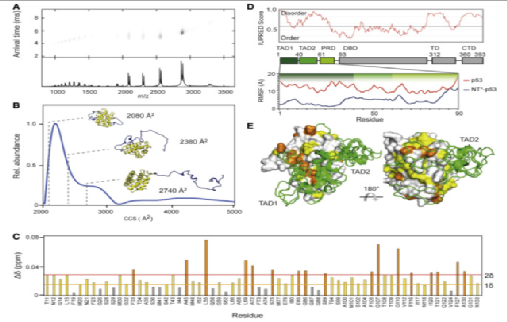
Figure 3. NT∗ induces compaction of the p53 TADs
由于投射电镜并无法解析p53蛋白结构中无序区域。因此,作者又转向使用离子迁移质谱(IM-MS)来评估融合蛋白中反式激活结构域1和2的整体构象。结果表明该蛋白在上述区域呈现松散状态。进一步地,通过核磁共振对其进行结构分析发现蛛丝蛋白融合并没有改善p53蛋白结构中的反式激活结构域的无序状态。同时结合对于p53蛋白序列中的前90个氨基酸序列进行全原子分子动力学(MD)模拟,作者确定了蛛丝蛋白结构域在 p53 融合蛋白中保持折叠并诱导融合蛋白的紧凑构象,其中 p53 N 末端反式激活区域包裹在蛛丝蛋白周围。
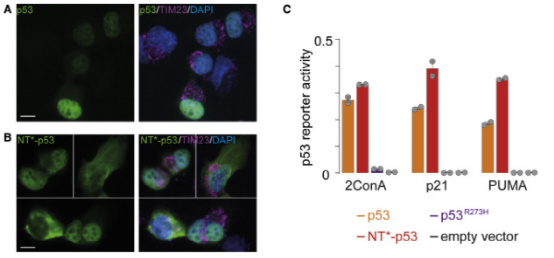
Figure 4. NT∗-p53 is active in H1299 cells
在对蛛丝-p53融合蛋白的结构进行了充分解析后,作者探究了其在H1299癌细胞中是否存在稳定的活性,从而可以作为潜在的癌症治疗方法。转染细胞后通过免疫组化,作者发现融合蛋白不会在细胞质内聚集而是与野生型P53蛋白一样进入细胞核中。同时,荧光素酶报告实验证明了融合蛋白对p53基因转录因子的活性没有影响。
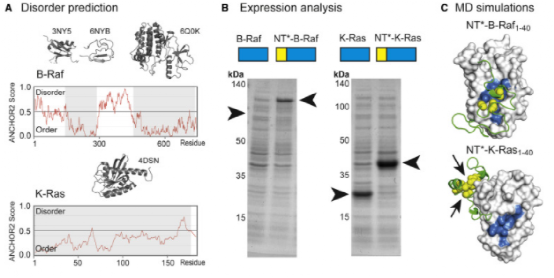
Figure 5. Application of the NT∗ strategy to B-Raf and K-Ras
最后,作者通过两种原癌蛋白B-raf和K-Ras验证了蛛丝蛋白结构域增加p53翻译水平和减少N端无限结构之间的关系。结果表明蛛丝蛋白结构域可以促进B-raf的表达,但是不影响K-Ras表达。而进一步地MD模拟揭示了上述现象的结构机制。
“在细胞中创造更稳定的p53变体一种很有希望的癌症治疗方法,现在我们有了一个值得探索的工具,”卡罗琳斯卡研究所高级教授David Lane说,“我们最终希望开发出一种基于mRNA的癌症疫苗,但在此之前,我们需要知道这种蛋白质在细胞中是如何处理的,以及大量的蛋白质是否有毒。”
参考文献:
[1] Kaldmäe M, et al. A "spindle and thread" mechanism unblocks p53 translation by modulating N-terminal disorder. Structure. 2022 Mar 10:S0969-2126(22)00049-1.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


