Molecular Therapy: Foxp3的表达增强了免疫治疗黑色素瘤的疗效
来源:生物谷原创 2022-09-22 17:14
过继细胞疗法(ACT)是新一代癌症治疗方法,可能会彻底改变临床策略。然而,T细胞的生物学特性和肿瘤微环境(TME)限制了ACT的疗效。
过继细胞疗法(ACT)是新一代癌症治疗方法,可能会彻底改变临床策略。然而,T细胞的生物学特性和肿瘤微环境(TME)限制了ACT的疗效。尽管转移的T细胞获得完全的效应功能是有效控制肿瘤生长的必要条件,但终末分化效应T细胞(TEF)的半衰期很短,而且这些细胞缺乏替代限制了ACT对肿瘤的长期控制。
此外,在T细胞分化为TEF细胞的过程中,T细胞开始表达抑制受体,以此作为控制免疫反应的一种手段。调节性T细胞在肿瘤微环境(TME)中压倒传统T细胞,这要归功于FOXP3驱动的代谢程序,该程序允许它们参与不同的代谢途径。

图片来源: https://doi.org/10.1016/j.ymthe.2022.08.017
近日,来自纳瓦拉大学的研究者们在Mol Ther杂志上发表了题为“FOXP3 expression diversifies the metabolic capacity and enhances the efficacy of CD8 T cells in adoptive immunotherapy of melanoma”的文章,该研究发现表明FOXP3在CD8T细胞对TME的适应中发挥了迄今未知的作用,这可能会增强它们在ACT中的疗效。
利用过继T细胞疗法(ACT)的黑色素瘤模型,研究者发现FOXP3在成熟的CD8 T细胞中过表达可以提高它们的抗肿瘤效果,有利于它们的肿瘤募集、增殖和细胞毒性。Foxp3过表达(Foxp3UP)的CD8T细胞具有组织驻留的记忆性和效应性T细胞的特征,但没有抑制活性。
肿瘤浸润性Foxp3UP CD8 T细胞的转录分析显示,多种代谢途径,如糖酵解、脂肪酸(FA)代谢和氧化磷酸化(OXPHOS)均为阳性。瘤内Foxp3UP CD8 T细胞对葡萄糖和脂肪酸的摄取能力增强,细胞内脂质积聚。
有趣的是,Foxp3UP CD8 T细胞通过激活有氧糖酵解来补偿线粒体呼吸驱动的ATP产生的损失。此外,在有限的营养条件下,这些细胞进行FA氧化来驱动OXPHOS以满足其能量需求。重要的是,它们结合糖酵解和OXPHOS的能力使它们能够在葡萄糖限制下维持增殖。
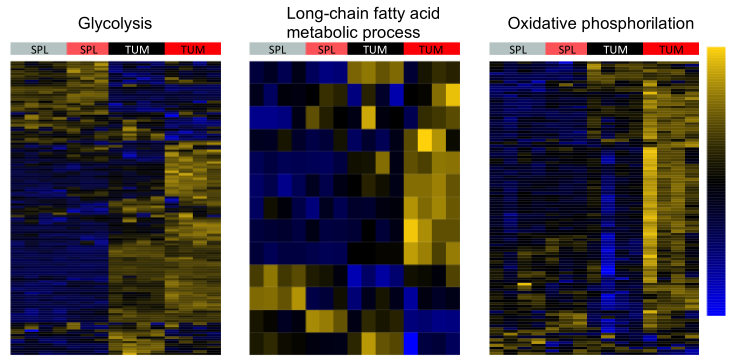
增强的FOXP3表达增加CD8T细胞的细胞毒作用
图片来源: https://doi.org/10.1016/j.ymthe.2022.08.017
综上所述,考虑到在FOXP3的驱动下,CD4Tregs能够调整其代谢以在敌意的TM中生存和增殖,以及关于FOXP3+CD8T细胞作为肿瘤特异性效应T细胞的推测的发现,研究者在成熟的CD8T细胞中过表达FOXP3,并检测了影响其代谢能力和在黑色素瘤过继免疫治疗中的抗肿瘤效果。(生物谷Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


