《细胞发现》:西湖大学发明全球首个基于蛋白质组学判断甲状腺结节良恶性的AI模型!
来源:奇点糕 2022-10-17 11:27
总的来说,这个研究构建了首个基于蛋白质组学对甲状腺结节良恶性进行预测的AI模型,仅通过19种蛋白,即可准确地区分甲状腺结节的良恶性,同时还有较高的敏感性和特异性。
相信学医的朋友都会有这样的感受:突然收到来自亲戚朋友的问候,同时被“顺便”咨询体检发现的某处结节,其中最常见的就是肺结节和甲状腺结节。
这问题看似简单,但其实并不那么容易回答。就比如甲状腺结节,很多人都有,但其中仅有约十分之一的结节是恶性的[1]。
目前对于结节良恶性的判断(手术取得病理标本之前),大多依靠医生临床经验和影像评估,换个人来阅片或者评估甚至可能会得出相左的结论。
对于甲状腺结节来说,即使进行细针穿刺活检(取少量细胞进行检测,目前术前最常用也是最可靠的检测手段[2]),也有大概三分之一的病例仍然无法得到确切的诊断[3]。
近日,来自西湖大学的郭天南和李子青团队,联合新加坡国家癌症中心的Oi Lian Kon和Narayanan Gopalakrishna Iyer团队,在《细胞发现》杂志发表重要研究成果[4]。
他们通过人工智能(AI)的方式对甲状腺结节蛋白质组学进行分析,建立了用于诊断结节良恶性的神经网络模型,准确率达到90%以上。在外部验证队列中,准确率也在85%以上。
这是全球首个基于蛋白质组学的甲状腺结节良恶性诊断AI模型,具有很强的临床转化价值,其良好的准确性或可使相当一部分良性结节患者免于手术之苦。

文章首页截图
为了建立区分甲状腺结节良恶性的AI模型,研究人员首先对来自新加坡总医院578位病人的579个结节(共1724个福尔马林固定石蜡包埋的组织样本)进行质谱分析,获得蛋白质组数据,并与其病理诊断相匹配,从而构建神经网络模型。
研究的测试集来自于中国和新加坡12家医院的回顾性福尔马林固定石蜡包埋组织样本数据(288个结节),和前瞻性队列的细针穿刺活检数据(294个结节)。
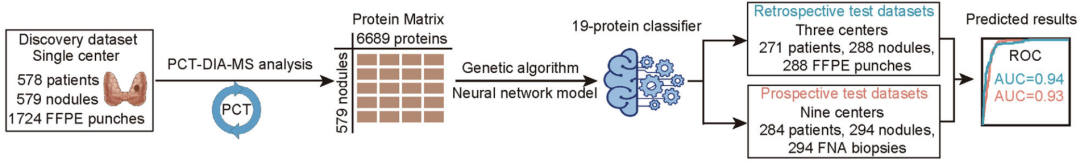
研究设计流程图
在先前的研究中,郭天南团队已构建了甲状腺特异性的蛋白质图谱[5],通过统一流形逼近和投影(UMAP,一种数据降维算法)对数据进行可视化后,他们发现乳头状甲状腺癌(PTC)与其他组织显著分离,而正常样本(N)与多结节性甲状腺肿(MNG)混杂在一起,滤泡性甲状腺腺瘤(FA)和滤泡性甲状腺癌(FTC)也无法分离。
这表明虽然良恶性结节的蛋白质组是存在一定差异的(N、MNG和FA为良性,FTC和PTC为恶性),但无法通过蛋白质组学的常规分析而直接区分良恶性结节(如FA何FTC)。
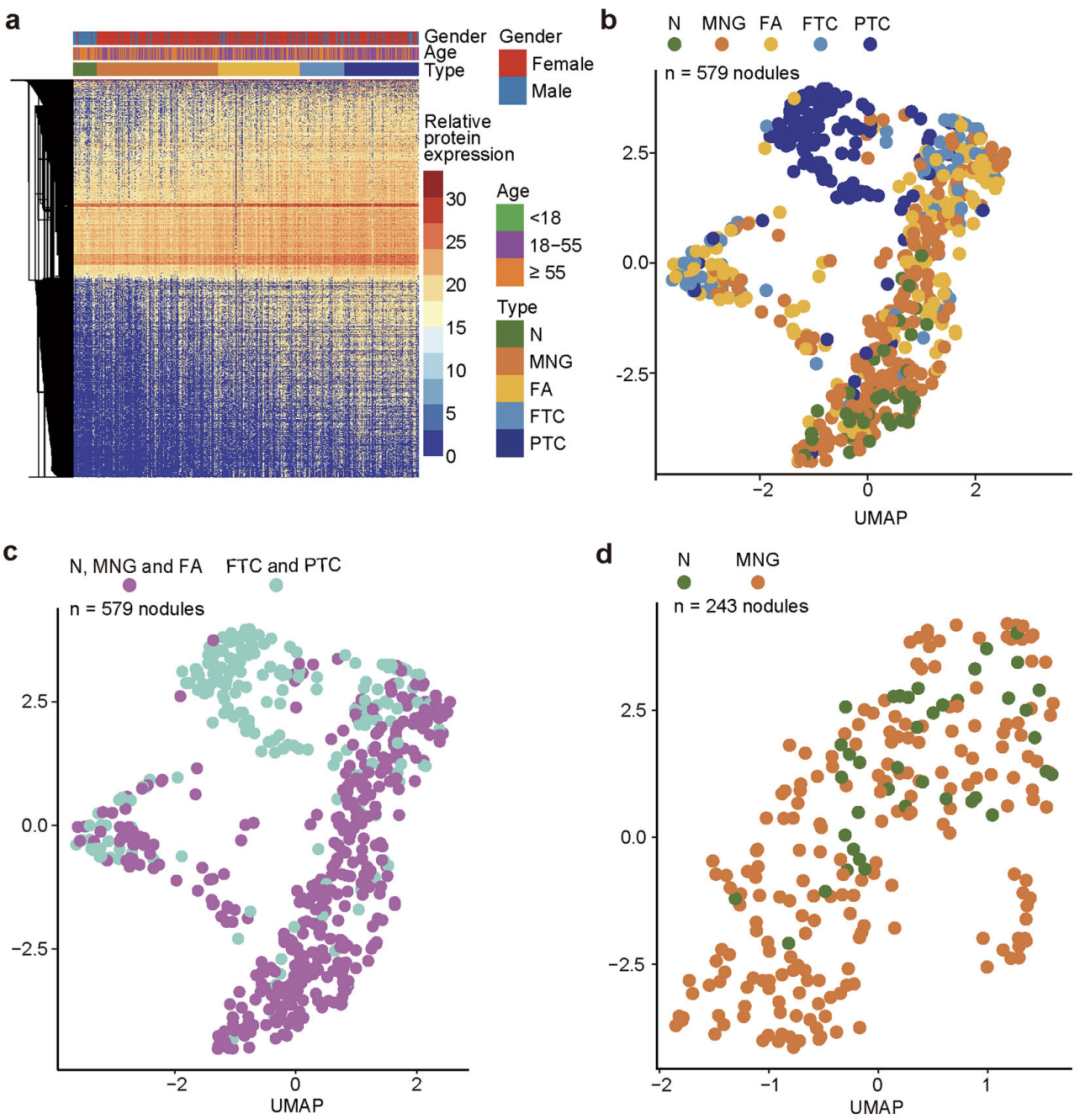
甲状腺良恶性结节无法通过蛋白质组学的常规分析而直接区分出来
紧接着,研究人员便想到通过神经网络模型来对良恶性结节进行区分。
通过对579个结节样本(40个N,203个MNG,137个FA,75个FTC和124个乳头状甲状腺癌PTC)进行三次交叉验证,最后选出了19个区分良恶性结节最准确的蛋白。
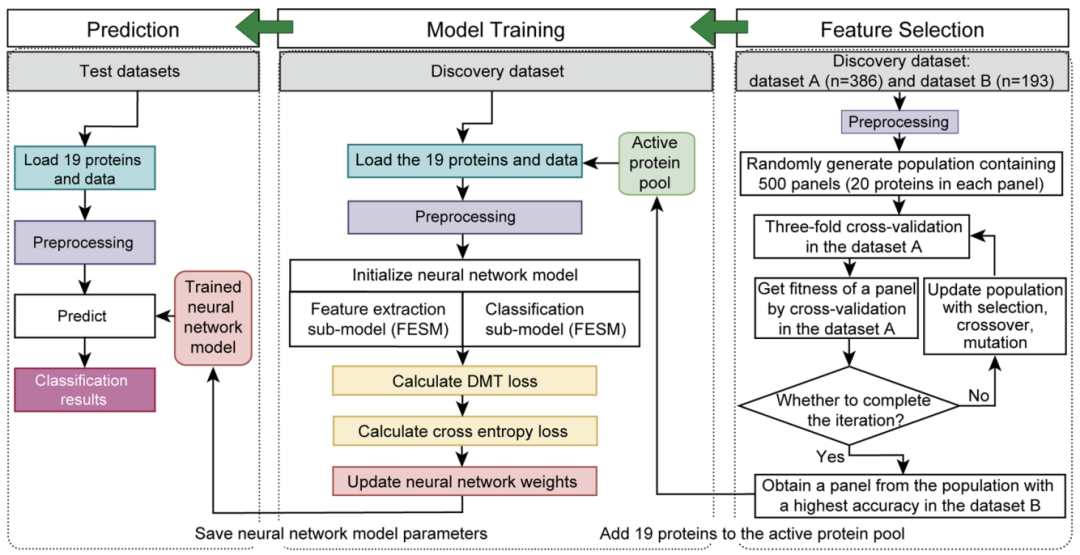
AI模型构建示意图
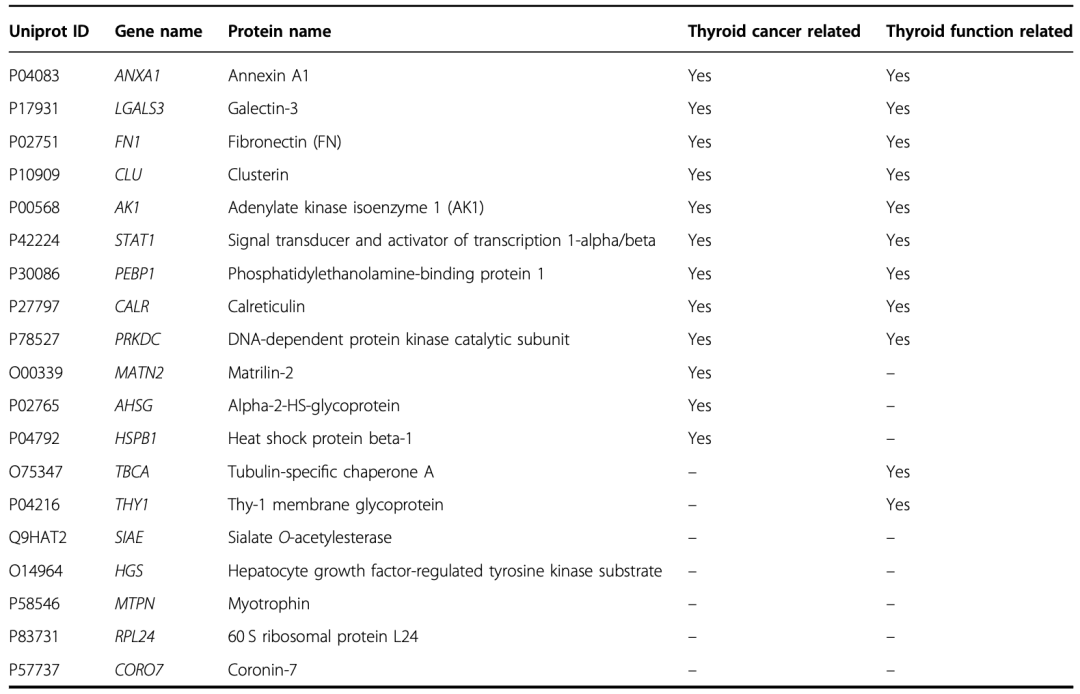
筛选出的19个蛋白质的详细资料
由于目前临床中甲状腺结节被过度治疗,因此在构建模型时研究人员尤其关注模型诊断的特异性,同时保证较高的灵敏度。
相比于6个其他机器学习模型(SVM,LASSO,决策树,MLP,随机森林,Logistic回归),以这19个选定的蛋白构建的AI预测模型具有最高的AUC(0.93)。
UMAP也显示,通过这19种蛋白,可将良恶性结节较好地区分。
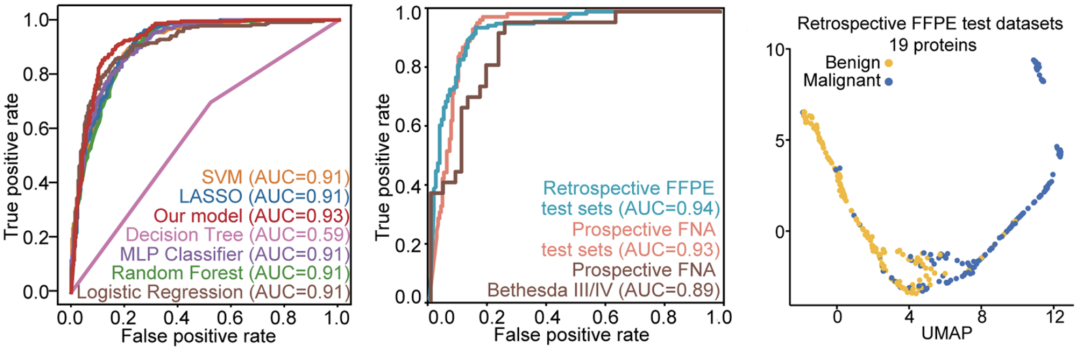
以19个选定的蛋白构建的AI预测模型具有良好的预测性能
随后,研究人员在外部测试集中对该模型的预测性能进行验证。
第一个测试集为288例福尔马林固定石蜡包埋的组织样本,其中144例为良性,其余144例为恶性。在该测试集中,AUC值可达到0.94,准确性为89%,敏感性和特异性分别为84%和94%。
第二个测试集为来自9家医院的294例细针穿刺活检数据,这一测试集的意义更为重大,因为本研究的初衷是开发在术前可用于预测结节良恶性的AI模型,而细针穿刺活检则是术前最为普遍的检测手段。在这一测试集中,AUC值同样高达0.93,准确率为85%,敏感性和特异性分别为92%和71%。
此外,研究人员还进一步检测了这个AI模型在不同Bethesda分类(甲状腺细针穿刺细胞学活检结果病理报告系统)细针穿刺活检样本中的性能,结果显示,对于Bethesda分类III和IV类的良恶性不确定的甲状腺结节,此AI模型的AUC值为0.89。
值得一提的是,细胞病理学家对Bethesda分类II、V和VI类样本的总体诊断准确率为82%,而本模型对这些相同结节的诊断准确率为88%。
同时,研究人员还指出,这个AI模型对于直径≥1 cm结节的预测准确率(87.7%)高于直径<1 cm结节(75.8%)。这可能是由于小结节采样的准确性较差的缘故。
对于淋巴细胞浸润明显的结节,这个AI模型难以将其与恶性结节区分开(淋巴细胞浸润性结节预测准确率为66%)。这可能是由于目前数据集所包括的淋巴细胞浸润性样本数量很少的缘故,从而导致了淋巴细胞性甲状腺炎的诊断准确性。
总的来说,这个研究构建了首个基于蛋白质组学对甲状腺结节良恶性进行预测的AI模型,仅通过19种蛋白,即可准确地区分甲状腺结节的良恶性,同时还有较高的敏感性和特异性。
同时,该模型不仅适用于传统的组织标本,对于甲状腺细针穿刺活检所取得的少量细胞蛋白,此模型同样具有很好的预测效果。
这一点在临床中尤为重要,对于细针穿刺活检无法明确性质的结节,通过这个模型进行良恶性判断,将会减少相当多的良性结节病人做原本并不需要的手术,具有很强的临床意义。
参考文献:
1.Durante C, Grani G, Lamartina L, Filetti S, Mandel SJ, Cooper DS: The Diagnosis and Management of Thyroid Nodules: A Review. JAMA 2018, 319(9):914-924.
2.Faquin WC, Bongiovanni M, Sadow PM: Update in thyroid fine needle aspiration. Endocr Pathol 2011, 22(4):178-183.
3.Alexander EK, Kennedy GC, Baloch ZW, Cibas ES, Chudova D, Diggans J, Friedman L, Kloos RT, LiVolsi VA, Mandel SJ et al: Preoperative diagnosis of benign thyroid nodules with indeterminate cytology. N Engl J Med 2012, 367(8):705-715.
4.Sun Y, Selvarajan S, Zang Z, Liu W, Zhu Y, Zhang H, Chen W, Chen H, Li L, Cai X et al: Artificial intelligence defines protein-based classification of thyroid nodules. Cell Discov 2022, 8(1):85.
5.Sun Y, Li L, Zhou Y, Ge W, Wang H, Wu R, Liu W, Chen H, Xiao Q, Cai X et al: Stratification of follicular thyroid tumours using data-independent acquisition proteomics and a comprehensive thyroid tissue spectral library. Mol Oncol 2022, 16(8):1611-1624.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


