Cancer Res: M6A RNA甲基化调节组蛋白泛素化促进肿瘤生长和进展
来源:本站原创 2022-03-27 16:40
骨肉瘤是儿童和青少年中最常见的骨恶性肿瘤,在50岁以上的人群中发病率第二高。大多数骨肉瘤(80%-90%)是高级别肿瘤,病因知之甚少。不幸的是,转移性或复发性骨肉瘤患者的存活率在过去30年中几乎没有变化,总体5年存活率约为20%。由于缺乏有效的化疗替代方案,这一比率没有改善。
骨肉瘤是儿童和青少年中最常见的骨恶性肿瘤,在50岁以上的人群中发病率第二高。大多数骨肉瘤(80%-90%)是高级别肿瘤,病因知之甚少。不幸的是,转移性或复发性骨肉瘤患者的存活率在过去30年中几乎没有变化,总体5年存活率约为20%。由于缺乏有效的化疗替代方案,这一比率没有改善。
此外,存活的患者由于在生命早期接受大剂量化疗而产生的衰弱副作用,严重影响了生活质量。在过去的三十年里,几乎没有一种药物被批准用于治疗骨肉瘤。这在一定程度上是因为骨肉瘤的基因组高度混乱,而且还没有发现可以靶向的反复突变。这些事实强调了确定新的靶点和机制的重要性,这些靶点和机制可以帮助更好地理解骨肉瘤的发病机制。
图片来源: https://pubmed.ncbi.nlm.nih.gov/35303054/
近日,格里希儿童癌症研究所的研究人员在Cancer Res杂志上发表了题为“M6A RNA Methylation Regulates Histone Ubiquitination to Support
Cancer Growth and Progression”的文章,该研究直接将ALKBH5活性增加与癌症中USP22/RNF40和组蛋白泛素化的失调联系起来。更广泛地说,这些结果表明,m6A
RNA甲基化与其他表观遗传机制协同工作,以控制癌症的生长。
在本研究中,研究者报告了通过mRNA甲基化的表观遗传学变化对于更好地了解骨肉瘤生长的机制和开发靶向治疗具有很大的前景。在骨肉瘤患者中,RNA去甲基酶ALKBH5基因扩增,且高表达与拷贝数变化相关。
ALKBH5是促进骨肉瘤生长和转移的关键因素,但对于正常细胞的生存却是必不可少的。ME-RIP-Seq分析和功能研究表明,ALKBH5通过调节组蛋白脱泛素酶USP22和泛素连接酶RNF40的m6A水平来介导其促肿瘤功能。
ALKBH5介导的骨肉瘤M6A缺失导致USP22和RNF40表达增加,从而抑制组蛋白H2A的单泛素化,诱导关键的促肿瘤基因,从而驱动不受抑制的细胞周期进展,持续复制和DNA修复。RNF40通过与基于DDB1-CUL4的泛素E3连接酶复合体相互作用并影响其稳定性,抑制了肿瘤中H2A的泛素化。
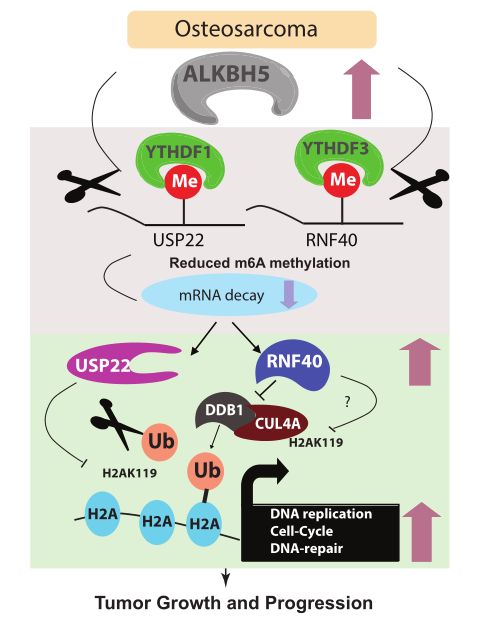
ALKBH5促进骨肉瘤生长和进展机制
图片来源: https://pubmed.ncbi.nlm.nih.gov/35303054/
总而言之,本研究有几个关键的观察结果。首先,研究者证明了m6A RNA甲基化对于维持组蛋白去泛素酶和泛素连接酶的最佳比例以控制H2A泛素化至关重要。其次,研究者展示了一个先前未明确的机制,即组蛋白去泛素酶USP22和泛素连接酶RNF40在癌症中的表达受到调控。这一发现意义重大,因为人们对组蛋白在癌症中普遍存在的调控知之甚少。
此外,揭示导致USP22在癌症中过度表达的机制将阐明其功能,并可能为靶向其致癌作用的方法提供信息。第三,该研究首次表明RNF40-DDB1-CUL4A在调节H2AK119泛素化中的作用。最后,研究者表明针对ALKBH5的方法将具有巨大的翻译潜力来治疗依赖于ALKBH5致癌信号的癌症。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



