代谢废物也是宝!3篇高分文献解析乳酸化在炎症和免疫领域研究中的应用!
来源:网络 2024-07-30 10:00
乳酸化是最近发现的乳酸条件炎症的贡献者,也是潜在的治疗靶点。乳酸化对免疫的调节作用也被称为“乳酸时钟”,基于时间模式将代谢和基因调控联系起来。
为助推研究者更好地利用奥斯卡DIA乳酸化组产品进行相关研究,现中科新生命和杭州微米生物联合推出“乳酸化组学百万支持计划”!该活动面向国内研究者征集乳酸化组学检测意向,并给予总额百万的项目支持。

传统上,乳酸被认为是细胞代谢的“废物”。最近的研究结果表明,乳酸是一种在各种生理细胞功能中发挥着不可或缺的作用的物质,有助于免疫和炎症反应过程中的能量代谢和信号转导。乳酰化的发现进一步揭示了乳酸在调节炎症过程中的作用。在剧烈运动或肿瘤、炎症、感染和缺血等疾病的条件下,当耗氧量或身体组织和细胞的氧气供应不足时,TCA循环受到抑制,有氧糖酵解途径被激活,以弥补氧化磷酸化产生ATP的不足。作为一种重要的信号分子,乳酸在调节免疫反应方面也起着至关重要的作用,从而影响免疫监视和逃逸相关行为。
大多数免疫细胞在稳定状态下相对静止,但当身体受到微生物感染、组织损伤或细胞应激时,免疫细胞可以迅速做出反应,激活炎症反应的代谢途径,帮助身体消除威胁并恢复体内平衡。转录因子缺氧诱导因子1α(HIF-1α)易位到细胞核并与糖酵解调节基因结合,诱导“Warburg 效应”和乳酸的产生。
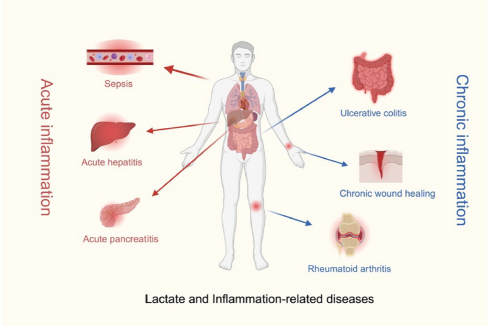
接下来小编将用3篇高分文献和大家探讨乳酸化在炎症和免疫的应用潜力。
1. 乳酸化与急性炎症疾病
脓毒症通常被视为一种压倒性的全身炎症,脓毒症相关急性肺损伤(sepsis-associated acute lung injury,ALI)是脓毒症患者的常见并发症,与高死亡率密切相关。大量临床证据表明,血清乳酸水平升高可作为脓毒症的预测生物标志物,乳酸水平升高与死亡率增加相关。此外,研究人员还发现,在ALI/ARDS患者中,局部肺乳酸水平与肺损伤程度呈正相关。
2024年5月复旦大学附属中山医院麻醉科缪长虹教授团队联合美国俄亥俄州立大学在Redox Biology杂志在线发表了题为“Histone lactylation-regulated METTL3 promotes ferroptosis via m6A-modification on ACSL4 in sepsis-associated lung injury”的研究性文章,探讨了乳酸在脓毒症相关急性肺损伤(ALI)期间肺泡上皮细胞铁死亡过程中的作用。

摘要
乳酸水平升高是脓毒症的重要生物标志物,与脓毒症相关死亡率呈正相关。脓毒症相关肺损伤(ALI)是临床患者预后不良的主要原因。然而,乳酸参与脓毒症相关 ALI 的潜在机制尚不清楚。在这项研究中,作者证明乳酸通过促进p300介导的 H3K18la 与 METTL3 启动子位点的结合来调节 N6-甲基腺苷(m6A)修饰水平。METTL3介导m6A修饰在ACSL4中富集,其mRNA稳定性通过YTHDC1依赖性通路进行调控。此外,短期乳酸刺激上调 ACSL4,从而促进线粒体相关的铁死亡。通过敲低或靶向抑制METTL3可有效抑制脓毒症高乳酸诱导的肺泡上皮细胞铁死亡,减轻脓毒症小鼠肺损伤。我们的研究结果表明,在脓毒症相关的ALI 期间,乳酸通过 GPR81/H3K18la/METTL3/ACSL4 轴在肺泡上皮细胞中诱导铁死亡。这些结果揭示了组蛋白乳酸化驱动的机制通过METTL3介导的m6A修饰诱导铁死亡。靶向 METTL3 对于脓毒症相关 ALI 患者来说是一种很有前途的治疗策略。
研究思路:

2. 乳酸化与自身免疫病相关疾病
在自身免疫病中,例如类风湿性关节炎和系统性红斑狼疮,免疫系统错误地攻击身体自身组织,导致慢性炎症和组织损伤。研究发现,乳酸化修饰可以影响关键的免疫调节分子的功能,如核苷酸结合寡聚化激活因子(NLRP3)和T细胞受体(TCR),从而改变免疫细胞的活性和自身免疫反应的强度。因此,理解乳酸化在自身免疫病发生和发展中的作用,有助于开发新的治疗策略和药物靶点,为患者提供更有效的治疗选择。
2020年12月德国海德堡大学医院团队在Arthritis & Rheumatology 杂志上发表了题为“Effect of Increased Lactate Dehydrogenase A Activity and Aerobic Glycolysis on the Proinflammatory Profile of Autoimmune CD8+ T Cells in Rheumatoid Arthritis”的研究性论文,通过研究类风湿性关节炎(RA)患者外周血和滑膜中的CD8+ T细胞,探讨了它们在代谢水平上的特征。

摘要
CD8+ T 细胞通过释放促炎和细胞溶解介质来导致类风湿性关节炎 (RA),即使在具有挑战性的缺氧和营养不良的微环境(如滑膜)中也是如此。本研究旨在探讨 CD8+ T细胞在 RA 患者血液和滑膜中满足其代谢需求的机制。本文使用来自 RA 患者、银屑病关节炎(PsA)患者和脊柱关节炎(SpA)患者以及健康对照受试者的纯化血液的CD8+ T细胞和来自RA滑膜的CD8+ T细胞。在mRNA和蛋白质水平上评估代谢酶、转录因子和免疫效应分子的表达,进行CD8+ T细胞功能研究。在所有RA CD8 T细胞亚群中,乳酸脱氢酶A(LDHA)在mRNA水平(P < 0.03 vs 对照组;n = 6/组)和蛋白水平(P < 0.05 vs 对照组;n = 17 名 RA 患者,n = 9 名对照组)过表达。在RA血液中,用FX11抑制LDHA导致CD8+ T细胞的脂肪生成、迁移和增殖以及CD8+ T细胞效应功能降低,而活性氧的产生增加了1.5倍(P<0.03与对照组相比)。通过靶向 LDHA 活性重塑 RA CD8+ T 细胞中的葡萄糖和谷氨酰胺代谢可以减少这些细胞对自身免疫发展的有害炎症和细胞溶解作用。
研究思路:
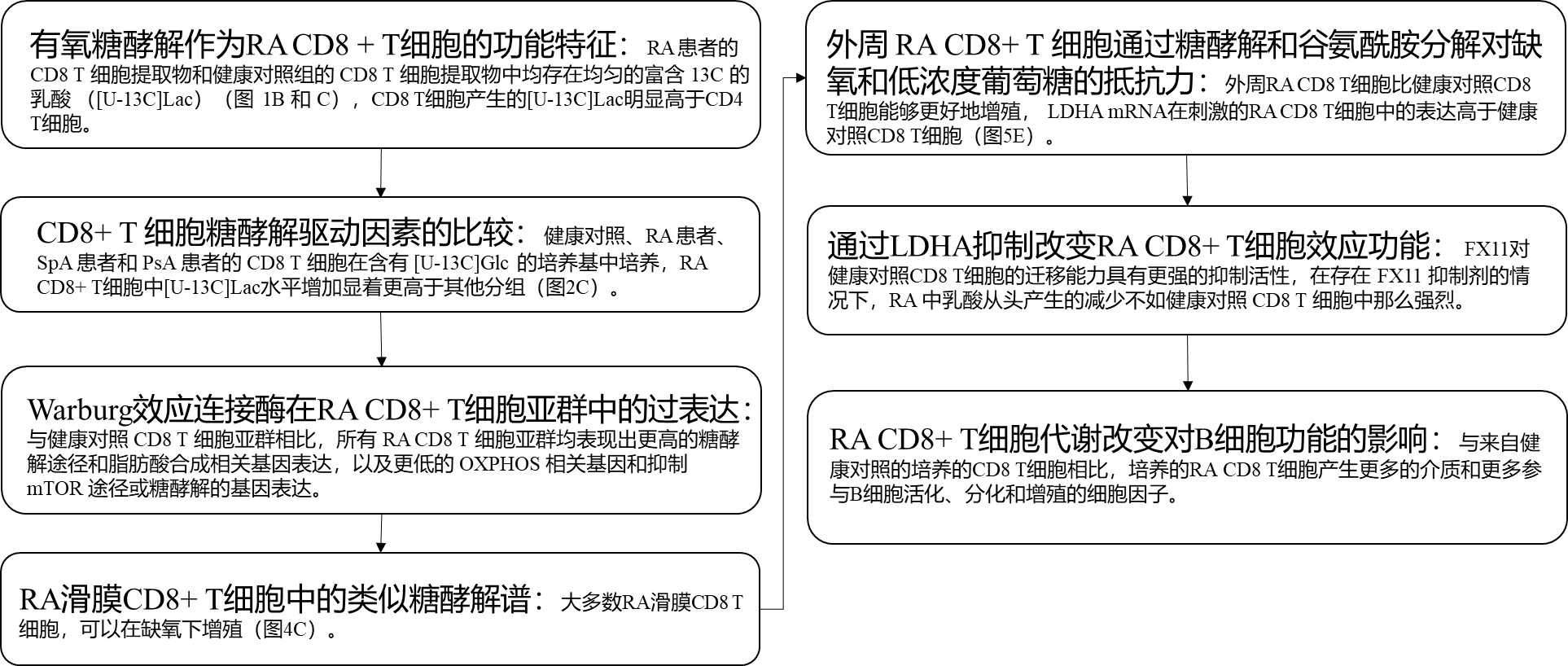
3. 乳酸化与巨噬细胞免疫
巨噬细胞是高度可塑性的免疫细胞,可据不同的微环境信号可表现出促炎或修复表型。乳酸化修饰可以调节多种关键蛋白,如炎症因子和调节免疫反应的信号分子,从而影响巨噬细胞的活性。研究显示,乳酸作为一种代谢产物,不仅影响巨噬细胞的能量代谢途径,还通过改变细胞内的代谢状态,促进巨噬细胞从促炎向修复的转变。深入理解乳酸化在巨噬细胞免疫中的作用机制,对于治疗炎症性疾病和促进组织修复具有重要的临床意义。
2022年10月来自上海交通大学医学院附属瑞金医院的章雄和刘琰团队在International Journal of Biological Sciences杂志上发表了题为“Lactylation of PKM2 Suppresses Inflammatory MetabolicAdaptation in Pro-inflammatory Macrophages”的研究性论文,探讨了乳酸和乳酸化对丙酮酸激酶 M2(PKM2)的调节作用,并进一步研究了乳酸在促炎巨噬细胞代谢适应和表型转变中的潜在作用。

摘要
新出现的证据表明,代谢适应是巨噬细胞表型转变的重要标志和先决条件。丙酮酸激酶M2(PKM2)是促炎巨噬细胞代谢适应的重要分子决定簇。翻译后修饰在PKM2的调控中起着核心作用。然而,对于PKM2中是否存在乳酸化以及乳酸化如何调节PKM2的功能仍然存在疑问。我们的研究首次报告说,乳酸通过激活PKM2来抑制Warburg效应,促进促炎巨噬细胞向修复表型的转变。我们将PKM2 鉴定为乳酸化底物,并确认乳酸化主要发生在K62位点。我们发现乳酸增加了PKM2的乳酸化水平,从而抑制了其四聚体到二聚体的转变,促进了其丙酮酸激酶活性并减少了核分布。简而言之,我们的研究报告了PKM2中一种新的翻译后修饰类型,并阐明了其在调节促炎巨噬细胞炎症代谢适应方面的潜在作用。
研究思路:
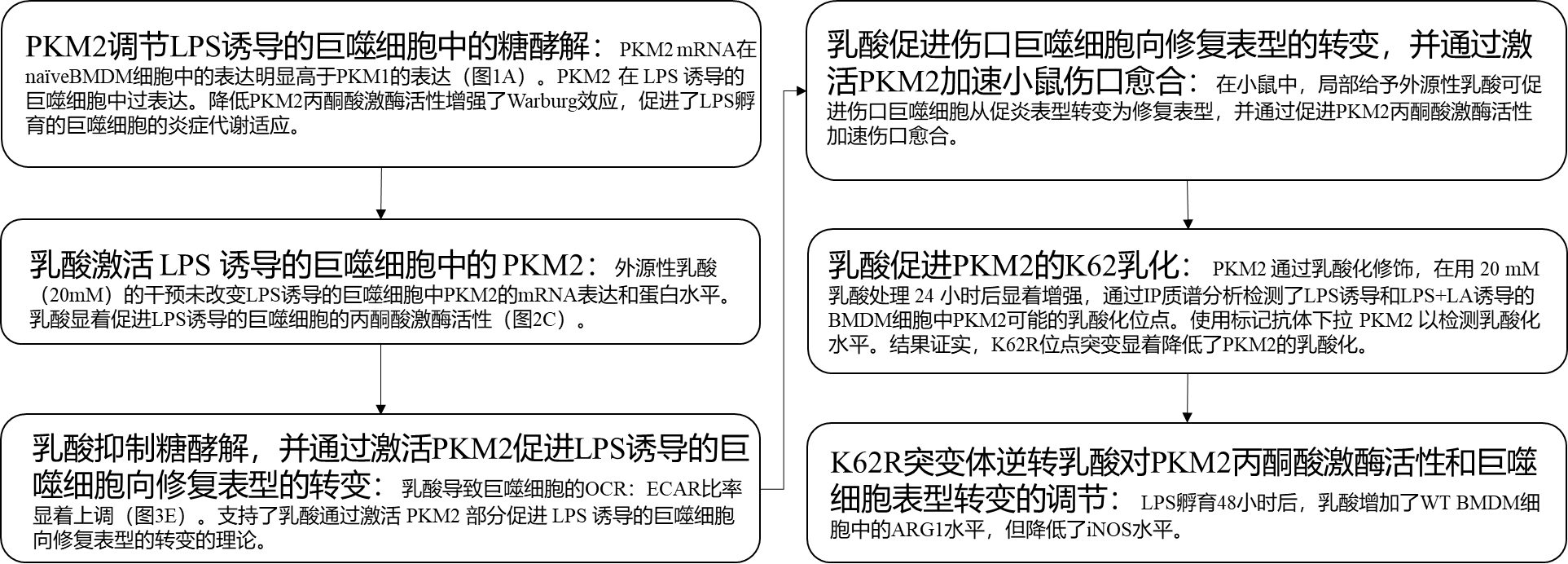
总结
乳酸在炎症疾病中的作用已在各个疾病方向有所开放,但根本矛盾机制仍需探索。乳酸化是最近发现的乳酸条件炎症的贡献者,也是潜在的治疗靶点。乳酸化对免疫的调节作用也被称为“乳酸时钟”,基于时间模式将代谢和基因调控联系起来。总之,乳酸化可能为预防和治疗炎症疾病提供新的思路和方法。
参考文献:
1.Wu D, Spencer CB, Ortoga L, et al. Histone lactylation-regulated METTL3 promotes ferroptosis via m6A-modification on ACSL4 in sepsis-associated lung injury. Redox Biol. 2024;74:103194.
2. Souto-Carneiro MM, Klika KD, Abreu MT, et al. Effect of Increased Lactate Dehydrogenase A Activity and Aerobic Glycolysis on the Proinflammatory Profile of Autoimmune CD8+ T Cells in Rheumatoid Arthritis. Arthritis Rheumatol. 2020;72(12):2050-2064.
3. Wang J, Yang P, Yu T, et al. Lactylation of PKM2 Suppresses Inflammatory Metabolic Adaptation in Pro-inflammatory Macrophages. Int J Biol Sci. 2022;18(16):6210-6225. Published 2022 Oct 24.
关于中科新生命
上海中科新生命生物科技有限公司(APTBIO)成立于2004年,前身是原中国科学院上海生命科学研究院蛋白质组研究分析中心的对外服务平台。企业通过与国内外高等研究机构的技术合作和自有研发团队的创新能力组建了企业创新研究院,建立了大队列多组学研究技术平台、生物药物早研及临床前CMC研究分析平台、生物药及药械注册报批平台、AI大数据算法四大技术平台,布局科技服务、生物医药及大健康消费医疗CRO服务三大业务板块,构建了AI大数据结合质谱多组学技术应用的生命科学大健康商业版图。
作为大健康产业链上游创新引擎的科技服务事业部,以蛋白质组、修饰组、代谢及脂质组等质谱服务为核心,并延伸打造微生物、转录组等基因组以及单细胞蛋白、单细胞测序、空间转录组、空间代谢、空间蛋白等单细胞/空间多组学服务,已搭建出完整的创新型多组学平台。科技服务事业部在上海、浙江义乌两地设有近10000平方米的实验室,多年来连续引进ThermoFisher、SCIEX、Bruker、10X等最先进的仪器设备近100台,秉承“创新为本,诚信为先、务实为要“的价值观,已助力全国上千所科研院校和医院客户发表3000+高水平SCI文章,累计影响因子20000+,为生命科学的发展提供坚实、专业、前沿的基础性研究。
联系我们
服务电话:021-54665263 400-066-6761
网址:www.aptbiotech.com
邮箱:marketing@aptbiotech.com.
联系地址:上海市闵行区园美路58号1号楼15 楼
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


