Cell子刊:宋尔卫院士团队揭示T细胞抑制乳腺癌转移的新机制
来源:生物世界 2025-08-29 10:22
这项研究表明了适应性免疫系统能够远程部署以保护远端器官免受肿瘤转移的侵害,突显了重建效应免疫细胞布控(EICD)在癌症治疗中的潜在疗效。
肿瘤抗原特异性 CD8+ T 细胞(细胞毒性 T 淋巴细胞)是抗肿瘤免疫的主要效应免疫细胞,但其在对抗癌症转移时的全身性分布情况,目前仍不明确。
2025 年 8 月 27 日,中山大学孙逸仙纪念医院宋尔卫院士、黄迪博士作为共同通讯作者,在 Cell 子刊 Developmental Cell 上发表了题为:Long-range deployment of tumor-antigen-specific cytotoxic T lymphocytes inhibits lung metastasis of breast cancer 的研究论文。
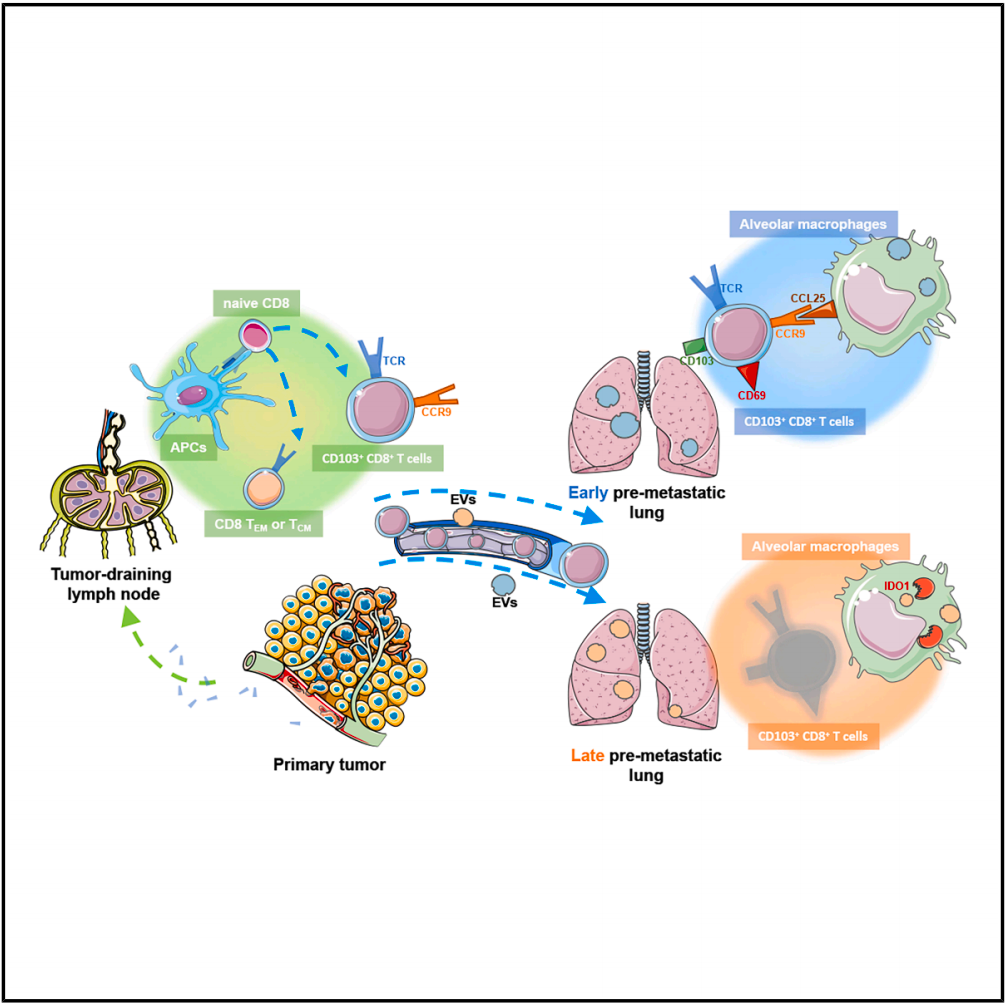
该研究揭示了肿瘤抗原特异性细胞毒性 T 淋巴细胞(CD103+ CD8+ T 细胞)的远程部署,可抑制乳腺癌的肺转移。

免疫检查点阻断(ICB)通过重新激活效应免疫细胞,在癌症治疗方面取得了巨大成功。表现出免疫“热肿瘤”表型的患者,其特征为效应免疫细胞的广泛浸润,可能从免疫检查点阻断治疗中获益。然而,原发肿瘤细胞与炎性浸润细胞之间的相互作用可能会减少效应 T 细胞的浸润,从而导致对免疫检查点阻断无反应的免疫“冷肿瘤”表型。
2022 年,宋尔卫院士团队提出了效应免疫细胞布控(Effector Immune Cell Deployment,EICD)的新概念,EICD 指的是效应免疫细胞在淋巴结、外周血和肿瘤微环境中的启动、激活、循环、募集、浸润和生存,其在免疫监视中至关重要,而 EICD 缺陷可能导致免疫逃逸。
远端器官炎性微环境的变化可能会显著影响前转移免疫重塑,导致促肿瘤或抗肿瘤的先天免疫细胞在前转移微环境中浸润。这些相互矛盾的证据表明了先天免疫在肿瘤转移防护中的双刃剑效应。然而,原发性肿瘤所引发的适应性免疫在控制肿瘤转移方面的作用,以及适应性免疫细胞的远程部署,却很少受到研究。
近期,新出现的证据表明,具有驻留记忆表型的 CD103+ CD8+ T 细胞存在于包括皮肤、肺、肠道和生殖道在内的非淋巴组织屏障中,在黏膜免疫反应中发挥着关键作用。在人体肺组织中,CD69+ CD103+ CD8+ T 细胞的数量是循环系统中同类细胞的 2-3 倍,它们能迅速唤起适应性免疫反应,并在呼吸道感染中保持长期的保护性记忆。
在包括非小细胞肺癌、乳腺癌和卵巢癌在内的多种实体瘤中,CD103+ CD8+ T 细胞的高度浸润与良好的临床预后相关,因为 CD103+ CD8+ T 细胞比其 CD103− 对应细胞能更有效地杀伤肿瘤细胞。然而,CD103+CD8+ T 细胞在肿瘤转移中的作用尚不清楚。
在这项最新研究中,研究团队发现,肿瘤引流淋巴结(TDLN)中肿瘤特异性 CD103+ CD8+T 细胞的丰度与乳腺癌患者的肺转移无病生存期延长有关。
研究团队进一步在小鼠癌症模型中发现,CD103+ CD8+ T 细胞在肿瘤引流淋巴结(TDLN)中被激活,并通过 CCL25/CCR9 信号转导,招募至肺部,通过抗原特异性免疫来抑制肿瘤转移。此外,来自肿瘤早期和晚期的细胞外囊泡(EV)分别使肺泡巨噬细胞极化,从而释放 CCL25 和 IDO1,而后者会抑制肺部 CD103+ CD8+ T 细胞的部署,从而促进肺转移。有效耗竭 IDO1 可恢复 CD103+ CD8+ T 细胞介导的对肺转移的保护作用。
该研究的核心发现:
抗原特异性 CD103+CD8+ T 细胞在肿瘤引流淋巴结中被激活,并迁移至肺部;
肺泡巨噬细胞通过 CCL25 招募 CD103+CD8+T 细胞,但通过 IDO1 触发 T 细胞死亡;
肿瘤细胞外囊泡货物在转移的不同阶段动态塑造肺泡巨噬细胞极化;
增强 CD103+CD8+T 细胞的募集或阻断 IDO1 可遏制肿瘤的肺转移。
总的来说,这项研究表明了适应性免疫系统能够远程部署以保护远端器官免受肿瘤转移的侵害,突显了重建效应免疫细胞布控(EICD)在癌症治疗中的潜在疗效。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


