Cell:David Baker团队从头设计可口服的迷你抗体,治疗自身炎症性疾病
来源:生物世界 2024-10-11 13:36
研究表明,口服给药的从头设计的微型结合剂能够穿过肠道上皮屏障到达治疗靶点,具有高效能、胃肠道稳定性和易于制造的特点。
近日,人工设计蛋白领域先驱 David Baker 教授团队在国际顶尖学术期刊 Cell 上发表了题为:Preclinical proof of principle for orally delivered Th17 antagonist miniproteins 的研究论文。
该研究利用计算设计从头生成了靶向IL-23R和IL-17的迷你蛋白,其具有抗体样结构、亚皮摩尔级别的亲和力,且具有极强的稳定性足以通过口服给药,在体外和体内实验中,该迷你蛋白显示出对结肠炎优异的治疗效果。

白细胞介素(IL)-23细胞因子由抗原呈递细胞产生,促进辅助性T细胞17(TH17细胞)的分化和表型维持。IL-23刺激循环TH17细胞以及组织内固有淋巴样细胞(ILC)和γδT细胞中促炎细胞因子IL-17的产生。
IL-23和IL-17是在基因和临床中得到验证的治疗靶点,用于治疗几种TH17细胞介导的自身炎症性疾病,包括炎症性肠病(IBD)和银屑病(俗称牛皮癣)。然而,现有的抗体疗法有一些局限性。在接受乌司奴单抗(ustekinumab,强生公司开发的全人源双靶向IL-12和IL-23抑制剂)治疗的IBD患者中,只有约30%的患者获得缓解,约20%的初始应答者由于产生抗药物抗体而随着时间的推移失去应答。此外,全身免疫抑制还会使患者患恶性肿瘤和严重感染的风险增加。
由于抗体药分子大,渗透性差,不能口服,只能通过静脉滴注或皮下注射给药,这也给患者带来不便和压力。全身给药的抗体通常表现出较差的组织外显率,全身给药后仅达到目标组织血清浓度的5%-10%。
此外,抗体药的制造和分销成本很高,因为它们通常是在哺乳动物表达系统中产生的,需要复杂的纯化过程才能达到适合肠外给药的纯度,并且需要冷藏才能储存和运输。
目前,已有许多口服和局部给药的蛋白质、肽类和小分子正在研发中,作为系统性施用抗体药的方便、免疫原性更低且价格更低廉的替代品。
一些已获批的TNF-α抗体的口服版本有望在具有相同细胞效力的情况下提供更大的用药便利性,但需要专有配方才能完整到达作用部位,这进一步增加了抗体药本身已经很高的成本。口服的JAK抑制剂已被批准用于包括炎症性肠病(IBD)在内的许多慢性炎症病症,但严重的副作用限制了其广泛应用。
目前正在研发的治疗炎症性肠病和银屑病的口服肽类药物,需要使用非规范氨基酸和交联来赋予其对胃肠道中蛋白酶的抗性,需要通过化学合成这种昂贵的生产方式。而正在研发的治疗银屑病的口服小分子药物,其与作用靶点IL-17A的结合亲和力仅为低微摩尔级别,并且需要每天服用两次相对较高的剂量才能达到适度的临床效果。
上述药物或疗法虽然比系统性给药的单克隆抗体更方便,但它们的安全风险、高昂的生产成本和有限的疗效仍是有待解决的显著缺点。
在这项研究中,研究团队展示了从头设计的迷你蛋白,这些微型结合剂具有抗体样结构、低皮摩尔级别的亲和力,能够靶向抑制IL-23R和IL-17A,且分子大小较小。
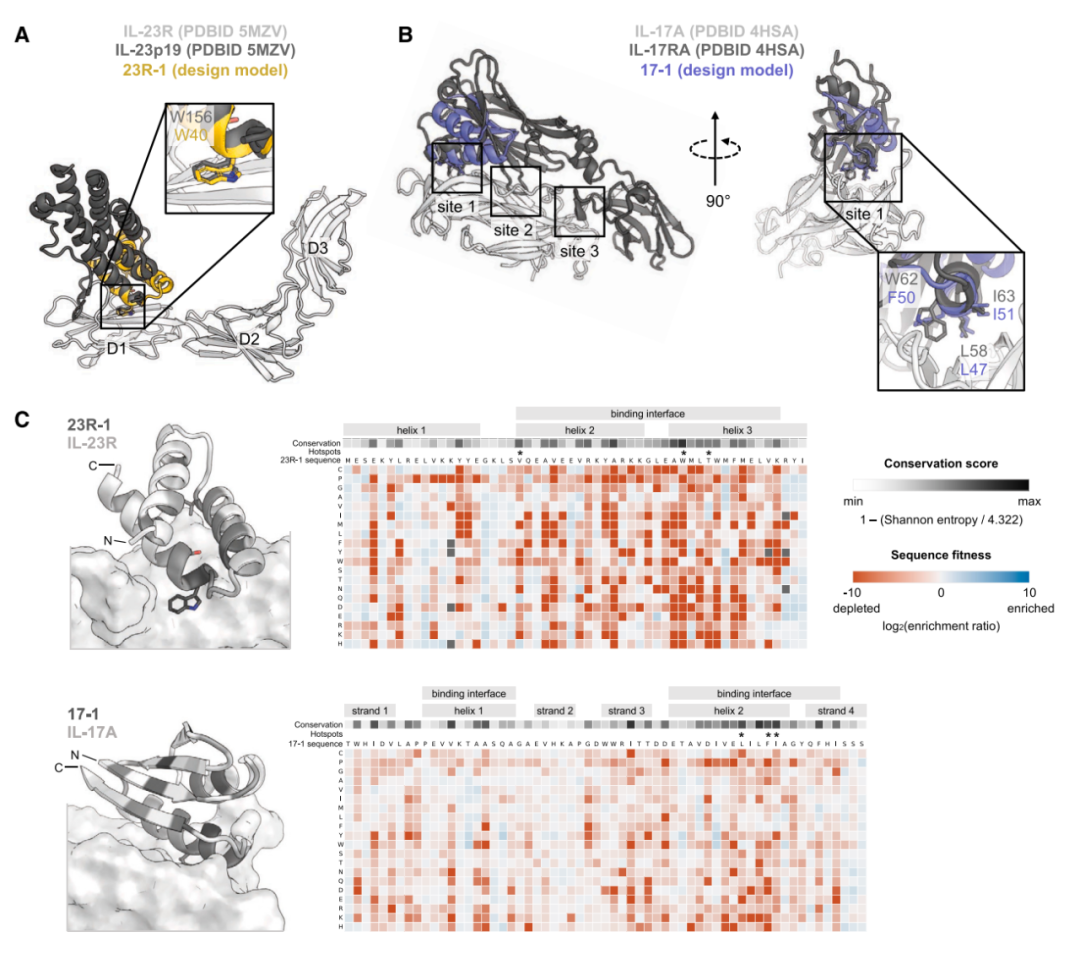
IL-23R和IL-17A迷你结合剂的计算设计
这些迷你结合剂在体外实验(原代细胞以及人类器官)中能有效阻断细胞信号转导,并且极其稳定,能够口服给药,且成本低廉。口服的IL-23R迷你结合剂在小鼠结肠炎中的疗效优于临床使用的抗IL-23抗体,并在大鼠中具有良好的药代动力学和生物分布特征。
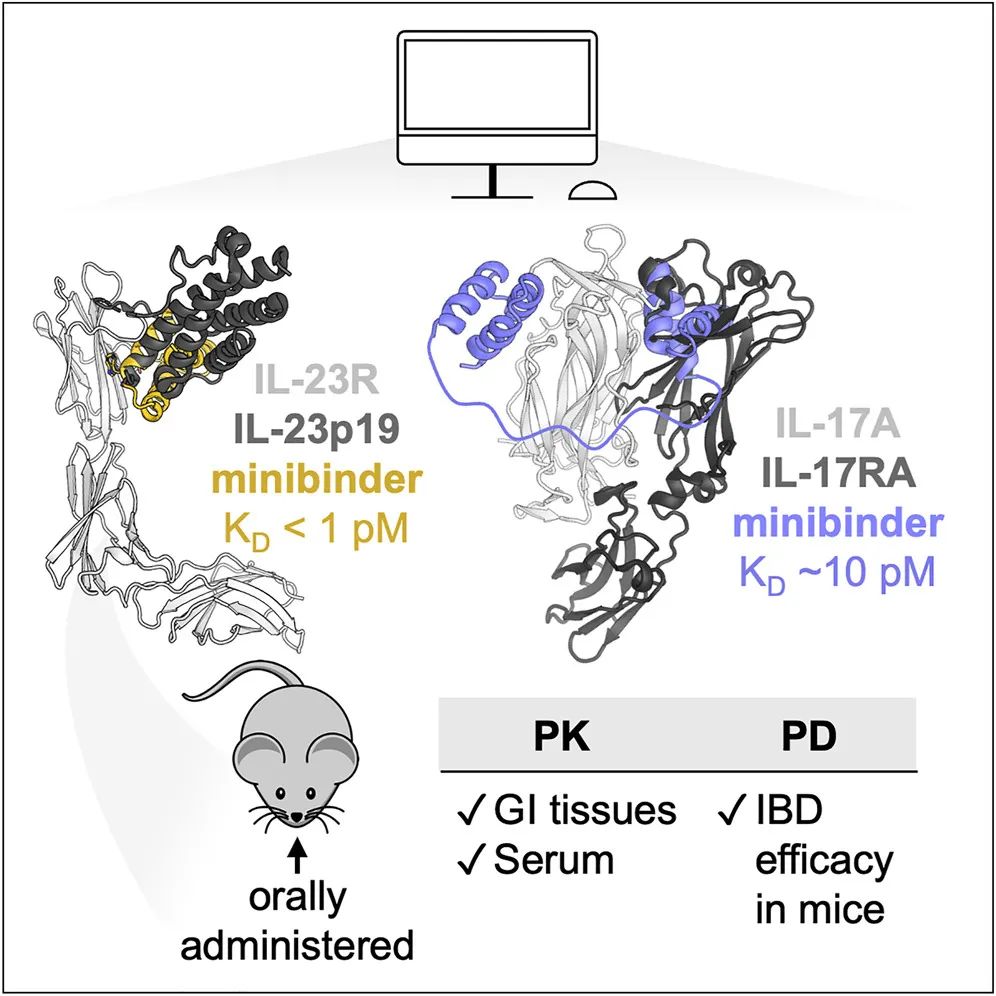
这项研究表明,口服给药的从头设计的微型结合剂能够穿过肠道上皮屏障到达治疗靶点,具有高效能、胃肠道稳定性和易于制造的特点,因此,从头设计的微型结合剂是口服生物制剂的一种有前途的形式。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


