Cancer Res:FOXP4是YAP1促进胃癌干性和转移的直接靶点
来源:生物谷原创 2024-08-30 12:43
本研究表明FOXP4在促进Yap1驱动的胃癌的进展中起到致癌基因的作用,从机制上讲,FOXP4作为YAP1的中介提高SOX12的表达并维持GC的干性。
癌变是癌症的标志之一,它指的是癌细胞表现出干细胞样特性的能力,如自我更新、分化成多种细胞类型的能力以及休眠。肿瘤干细胞(CSCs),也被称为肿瘤起始细胞,代表肿瘤内的一个细胞分支,被认为在各种类型的癌症中负责致瘤性、转移、复发和治疗抵抗。
CSCs通过驱动肿瘤生长和异质性、逃避免疫监视和响应环境信号来促进生存、增殖和维持干细胞特性。根据CD44、CD24、CD29、CD90和CD133等表面标记物的表达,可以从多种肿瘤和细胞系中分离出csc。
由于大多数CSCs具有遗传和表观遗传改变,导致信号通路失调,如TP53突变,β-连环蛋白过度激活或DNA甲基化。一些研究还表明,癌症的干细胞性可以通过异常激活或抑制正常干细胞通路来调节,如Wnt、NF-κB、Notch、Hedgehog、JAK-STA T、PI3K/AKT/mTOR以及Hippo-YAP1信号通路。
Hippo通路,也被称为Hippo- yAP1信号通路,最初是通过突变筛选在果蝇中发现的。它是一个进化上高度保守的信号级联,是器官大小、发育和细胞接触抑制的主要控制因子,也维持细胞增殖、凋亡和组织稳态之间的平衡。此外,hpo - yap1通路的失调已被证明可以增强几个重要的癌症特征,如控制细胞增殖、增殖、抵抗癌细胞死亡和赋予癌症干细胞特征。
它与各种人类癌症的发展有关,包括胃癌、乳腺癌、结肠直肠癌、肝癌和食道癌。在此之前,研究者已经揭示了Hippo-YAP1信号通路在胃癌发生中的驱动作用,在该通路的核心,YAP1作为转录共激活因子,主要与TEAD转录因子家族结合促进细胞增殖,并在GC中发挥致癌作用。研究者还总结了Hippo-Y AP1信号失调在GC中的功能作用。在机制上,Hippo-Y AP1通路调节数千个促进肿瘤发生的靶基因。然而,在GC中具有干性特性的YAP1直接靶基因尚未被发现。

图片来源:https://pubmed.ncbi.nlm.nih.gov/39047223/
近日,来自中国科学院解剖与细胞病理学研究室的研究者们在Cancer Res杂志上发表了题为“FOXP4 is a Direct YAP1 Target that Promotes Gastric Cancer Stemness and Drives Metastasis”的文章,该研究揭示了FOXP4作为一种新的干性标志物,通过调节YAP1信号在胃癌中促进肿瘤发生。
Hippo-YAP1通路是一个进化保守的信号级联,控制器官大小和组织再生,Hippo-YAP1信号的失调促进了包括胃癌(GC)在内的几种癌症的发生和发展。由于Hippo-Y AP1通路调节数千种基因的表达,因此确定哪些靶基因参与YAP1驱动的致癌程序以确定规避该程序的策略非常重要。
在这里,研究者发现FOXP4通过维持干性和促进腹膜转移在Yap1驱动的胃癌发生中发挥重要作用。FOXP4的缺失损害了GC球状体的形成并降低了干细胞标记物的表达,而FOXP4的上调则增强了癌细胞的干细胞性。RNA-seq分析显示SOX12是FOXP4的下游靶点,功能研究证实SOX12在Y AP1诱导的癌变中支持干性。

生成MNNG诱导GC模型的工作流程图
图片来源:https://pubmed.ncbi.nlm.nih.gov/39047223/
小分子筛选发现42-(2- Tetrazolyl)雷帕霉素是FOXP4抑制剂,在体内靶向FOXP4可抑制GC肿瘤生长,增强5-FU化疗的疗效。
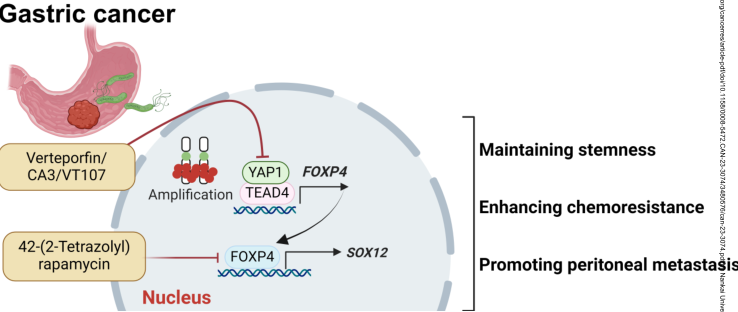
YAP1-FOXP4-SOX12轴在胃癌中的总体示意图
图片来源:https://pubmed.ncbi.nlm.nih.gov/39047223/
综上所述,本研究表明FOXP4在促进Yap1驱动的胃癌的进展中起到致癌基因的作用,从机制上讲,FOXP4作为YAP1的中介提高SOX12的表达并维持GC的干性。此外,研究者发现一种名为42-(2-Tetrazolyl)雷帕霉素的小分子抑制FOXP4与5-FU(一线化疗)联合使用具有更强的抗肿瘤作用,这表明通过添加5-FU靶向FOXP4可能是一种治疗GC的前瞻性方法。此外,本研究为Y ap1驱动的GC的茎干维持提供了新的见解。YAP1-FOXP4-SOX12轴的异常激活是GC的一个有希望的治疗靶点。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


