阿司匹林为何能预防癌症?蒋晖等人揭示阿司匹林促进DNA修复新机制
来源:生物世界 2023-03-07 09:22
阿司匹林抑制炎症通路并通过同源重组(HR)促进DSB修复的能力强调了其在炎症和基因组不稳定驱动的健康疾病管理中的潜力。
阿司匹林(Aspirin,乙酰水杨酸),1898年上市以来,至今已有超过百年的临床应用,成为医药史上三大经典药物之一。至今仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂。
近年来,阿司匹林被发现在多种疾病中有效,甚至对神经退行性疾病、心血管疾病、癌症等重大疾病也有着一定的预防和治疗效用。
近日,蒋晖(现为哈尔滨工业大学研究员)等人在 Cell Research 期刊发表了题为:Aspirin protects against genotoxicity by promoting genome repair 的研究论文。
该研究表明,阿司匹林除了其广为人知的抗炎作用外,还具有良好的对抗辐射的作用,通过对组蛋白H4K16的乙酰化,增强了染色质解压缩,从而增强DNA损伤部位招募修复因子进行同源重组(HR)修复。
阿司匹林作为染色质结构和修复的调节剂这一发现提供了一种新的机制,可以解释其许多备受赞誉的健康益处,包括预防癌症。

第二次世界大战中核爆炸产生的巨大破坏让人们开始寻找对抗辐射的措施,此后,切尔诺贝利核电站、福岛核电站泄露事件进一步加深了人们对辐射危害性的认知。实际上,在辐射源附近的工作人员、飞行员和宇航员,以及长期接受放疗的患者,也需要预防辐射危害。然而,尽管已经研究了几十年,现在仍然没有一种安全、高效、经济的辐射保护工具。
在癌症治疗中,骨髓衰竭是放疗后死亡的主要原因。因此,保护骨髓是开发辐射对策的主要目标。炎症是辐射引起的组织损伤的关键结果和驱动因素,考虑到阿司匹林的抗炎作用,研究团队探索了使用阿司匹林来预防辐射危害。
在这项研究中,研究团队发现,在小鼠体内和骨髓源性单核细胞中,阿司匹林可防止辐射诱导的骨髓消融,并抑制辐射对炎症基因(包括Ifnb1、Mx1和Tnfa)的诱导。
模式识别受体(PRR),包括Toll样受体(TLR)、RIG-I样受体(RLR)和胞质DNA感受器(CDS)是炎症和细胞死亡的起始中枢。为了评估阿司匹林的辐射保护是否是由于抑制PRR驱动的炎症,研究团队将野生型(WT)小鼠与PRR信号传导缺陷小鼠进行了比较。与WT小鼠类似类似,阿司匹林可以保护TLR和RLR通路均有缺陷或CDS缺陷的基因敲除小鼠的骨髓对抗辐射,并抑制炎症基因的表达。这意味着实验中观察到的骨髓抑制与PRR驱动的炎症无关,阿司匹林的辐射保护作用也与其抗炎作用无关。
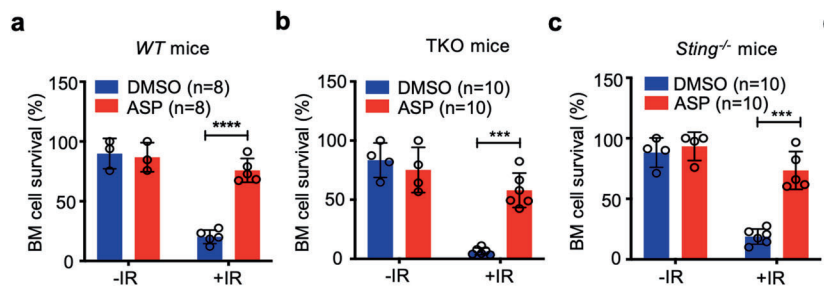
DNA双链断裂(DSB)是辐射最有害的结果,其可能导致细胞的染色体畸形,形成微核(Micronuclei),HEK293细胞在PRR信号传导方面存在缺陷,缺乏前列腺素过氧化物合酶(COX1和COX2),这是炎症和疼痛的关键介质,也是阿司匹林最著名的靶标。阿司匹林能够抑制辐射诱导的HEK293细胞形成微核,这表明这种作用不依赖于其抗炎活性。当辐射在冰上低温培养的HEK293细胞(防止其自发DNA修复),然后从冰上转移到37°C以允许DNA修复时,阿司匹林预处理的细胞能够更快地修复DNA双链断裂。此外,阿司匹林也加速了由抗癌药物阿霉素诱导的DNA双链断裂的修复。
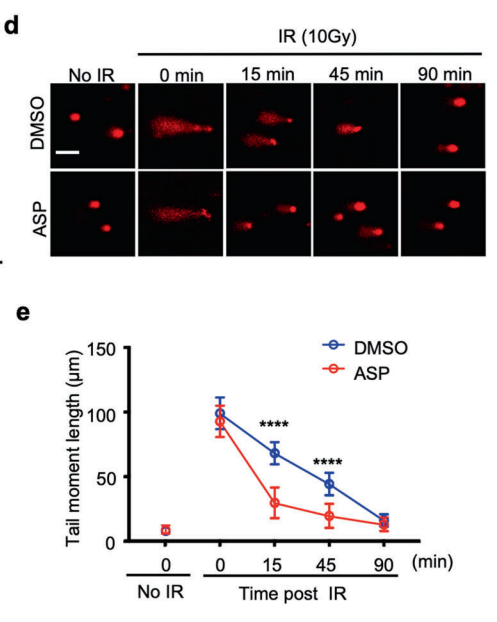
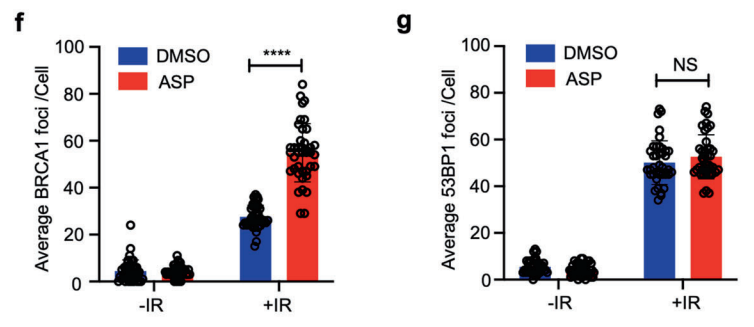
DNA双链断裂(DSB)后通过同源重组(HR)和非同源末端连接(NHEJ)进行修复。基于绿色荧光蛋白(GFP)报告系统的结果显示,阿司匹林促进HR修复,但不促进NHEJ修复。BRCA1和53BP1分别是HR和NHEJ修复的关键检查点蛋白。阿司匹林增强了对BRCA1的招募,而NHEJ修复蛋白53BP1没有被招募到DNA损伤位点。因此,BRCA1的缺失显著减缓了阿司匹林对DSB修复的加速作用。
染色质解压缩对于损伤部位的DNA修复机制的招募至关重要。组蛋白H4的N端尾是核小体间相互作用的中心,组蛋白H4第16位赖氨酸的乙酰化(Ac-H4K16)对于减少核小体-核小体堆叠和染色质压缩至关重要,以允许修复蛋白的募集。而阿司匹林能够促进Ac-H4K16。
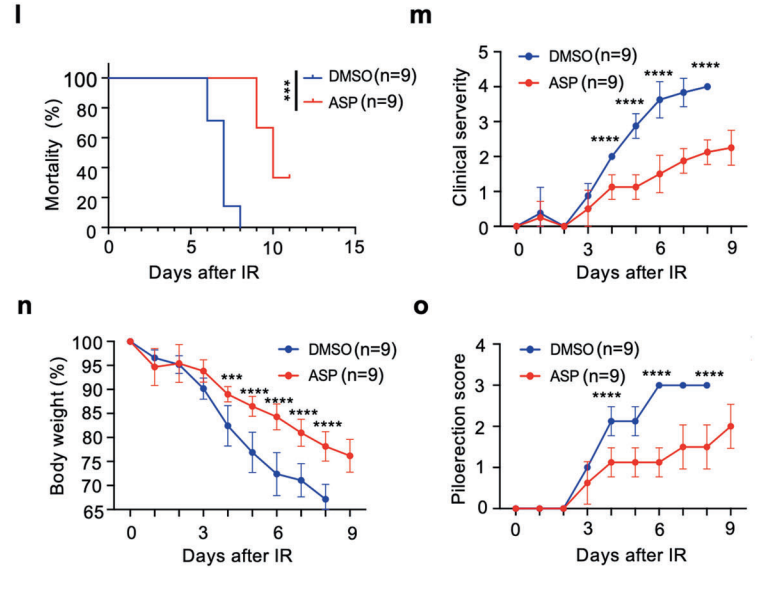
研究团队进一步从小鼠骨髓细胞中分离出染色质,与体内加速DNA断裂修复的能力一致,阿斯匹林治疗的小鼠Ac-H4K16升高,辐射后γ-H2A水平下降,γ-H2A是DNA损伤的标志。当进一步监测时,阿司匹林治疗小鼠的生存期延长,并表现出相对更轻的辐射症状。
阿司匹林的治疗效果被认为是由于它有抑制炎症的能力,在机制上,阿司匹林最初被报道通过抑制COX1和COX2来实现这一效果。而这项最新研究发现,虽然阿司匹林也通过阻断多种PRR通路来抑制炎症,但除了其抗炎作用外,阿司匹林还是基于同源重组(HR)的DNA双链断裂(DSB)修复的有效放大器。具体来说,阿司匹林通过对组蛋白H4K16的乙酰化,增强了染色质解压缩,从而增强了DNA损伤部位招募修复因子进行同源重组(HR)修复。
DNA双链断裂(DSB)对健康有害,它除了可能引发细胞死亡外,如果没有修复或修复错误,还会导致染色体缺失和易位,从而导致长期危害,包括癌症和遗传性疾病。此外,DSB也是炎症的原因,而炎症是辐射/化疗诱导的组织损伤的关键驱动因素。除了加速DSB的修复外,阿司匹林还可能通过抑制炎症诱导的DNA损伤间接促进基因组保护。
因此,阿司匹林抑制炎症通路并通过同源重组(HR)促进DSB修复的能力强调了其在炎症和基因组不稳定驱动的健康疾病管理中的潜力。此外,阿司匹林是染色质结构和修复的调节剂这一发现提供了一种新的机制,可以解释其许多备受赞誉的健康益处,包括预防癌症。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


