研究人员发展免疫邻近标记技术高分辨解析神经元轴突起始段蛋白质组
来源:网络 2024-01-02 14:40
该研究发展了基于免疫邻近化学标记的新技术,提供了高空间特异性的神经元AIS蛋白质组数据,并描绘了在神经元发育过程中AIS蛋白质组分的动态变化。
大脑神经环路的活动依赖于神经元动作电位的产生和传播。轴突起始段(Axon Initial Segment,AIS)是一个位于轴突上靠近胞体的亚细胞结构,长度一般在20至60µm之间,是神经元动作电位起始的地方。AIS结构组分、长度或位置的改变均可以影响神经元的兴奋性,其结构的完整性对于神经元极性的建立和维持也至关重要。例如:AIS结构被破坏可导致神经元轴突获得树突特性。已有研究表明,在许多神经系统疾病中存在AIS结构异常现象,包括自闭症、阿尔茨海默病、中风、双相情感障碍、精神分裂症和肌萎缩侧索硬化症等。在小鼠模型中,恢复AIS结构和功能可以帮助改善阿尔茨海默症和天使综合征的神经缺陷。然而,人们目前对于AIS组分的了解依然有限,这阻碍了在生理和病理情况下我们对AIS结构和功能调控的理解。
传统鉴定AIS组分的方法主要依靠抗体染色或药理学筛选。这些方法受制于抗体或药物的特异性和商业化程度,不仅成本较高,而且通量很低。此外,AIS区域由于结构致密而导致可溶性差,使用传统的生物化学方法(如免疫共沉淀)分离其中的蛋白质组分效果不理想。近年来,基于生物素连接酶BioID/TurboID或过氧化物酶APEX/HRP的邻近标记方法被建立起来,成为解析亚微米-纳米尺度下细胞结构蛋白质组学的重要研究工具。然而,这些方法需要将融合了诱饵蛋白的邻近标记酶通过转染或病毒侵染等手段导入到细胞,而这种外源表达方法可能会导致诱饵蛋白的错误定位。例如,BioID技术被用于鉴定体外培养海马体神经元AIS蛋白质组分,由于诱饵蛋白出现了在AIS以外的错误定位,所获得数据的空间特异性较低。鉴于目前AIS组分研究中面临的通量低或数据质量差等问题,迫切需要开发一种针对内源诱饵蛋白开展邻近标记的技术。

论文截图
近日,北京大学化学与分子工程学院、北大-清华生命科学联合中心、北大IDG/麦戈文脑科学研究所邹鹏研究员课题组和美国贝勒医学院神经科学系Matthew N. Rasband教授课题组合作在Nature Communications上发表了题为“Immunoproximitybiotinylation reveals the axon initial segment proteome”的论文。该研究发展了基于免疫邻近化学标记的新技术,提供了高空间特异性的神经元AIS蛋白质组数据,并描绘了在神经元发育过程中AIS蛋白质组分的动态变化。该工作鉴定到了新的AIS组分如SCRIB,并利用超分辨荧光成像、生物化学等手段对其定位和蛋白质-蛋白质相互作用进行了详细的表征。这些研究为阐明AIS结构和功能的调控机制提供了丰富的数据资源。
首先,作者建立了针对AIS的免疫邻近标记技术IPL(immuno-proximity labeling)。利用针对AIS蛋白质组分NF186的抗体,将过氧化物酶HRP靶向至AIS处,实现针对内源蛋白质的靶向,避免了遗传学操作。进一步,利用HRP在过氧化氢的触发下催化产生生物素苯酚自由基,以100nm的扩散半径对NF186邻近的蛋白质分子进行共价标记,实现对AIS组分的有效覆盖。免疫荧光成像和免疫印迹分析均证明了IPL方法具有高空间分辨能力。
随后,作者以多个神经元亚细胞结构(包括细胞体、树突、轴突等)作为空间参照,通过10重TMT肽段标签并结合定量比率蛋白质组学扣除背景信号和参照信号,最终获得了高质量AIS蛋白组数据。数据分析表明,捕获到的1403个蛋白质几乎涵盖了所有已报到的AIS分子(图1),包括胞外基质蛋白、AIS膜蛋白及各种电压门控离子通道蛋白和细胞骨架相关蛋白等。其中,目前已知的AIS高表达分子AnkG、TRIM46、NFASC、Nav1.2和βIV-spectrin处在数据列表前5的位置。至此,作者获得了成熟神经元AIS高覆盖度的蛋白质数据列表。
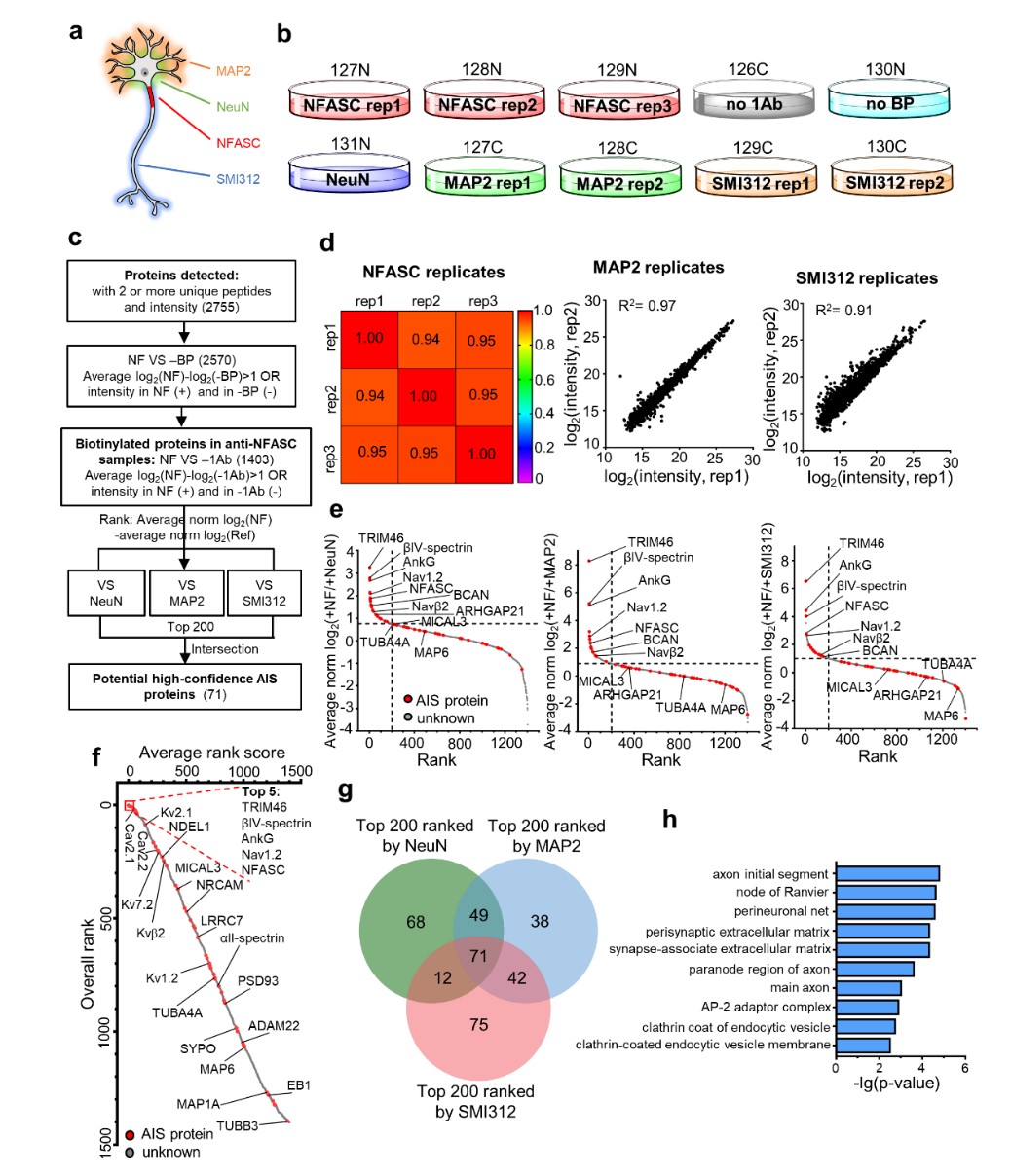
图1. DIV14神经元轴突起始段AIS蛋白组
为探讨AIS发育过程中组分的动态变化,作者选取了AIS发育初期DIV7、成熟期DIV14和完全成熟期DIV21三个时间点,通过IPL策略分别给出了各时期的AIS数据集。对发育过程中AIS潜在核心组分的分析,揭示了AIS组分的动态变化:绝大多数蛋白质随着AIS的发育表达量增加,如AnkG和Nav1.2;而少数蛋白质如参与神经元早期极性建立的TRIM46却呈现出显著性降低。至此,作者获得了神经元发育过程中与AIS生理功能匹配的蛋白质组分动态图谱。
最后,作者以DIV14的蛋白质组学数据作为指导,对排名前三且在AIS中没有任何研究的蛋白质进行了表征(图2a)。通过CRISPR/Cas9依赖的HiUGE基因敲入策略对感兴趣蛋白质添加内源性标签。成像结果显示,这三个蛋白质在AIS处有着不同程度的表达,其中支架蛋白SCRIB在AIS处呈现高度的极化(图2b和c)。随后作者通过体内外基因标签敲入策略和抗体标记实验进一步证实了SCRIB在AIS的极化分布。通过CRISPR/Cas9依赖的基因敲除策略和免疫共沉淀实验,揭示了SCRIB在AIS的富集受AIS核心组分AnkG的征募,且SCRIB N-端结构域参与了与AnkG的互作。
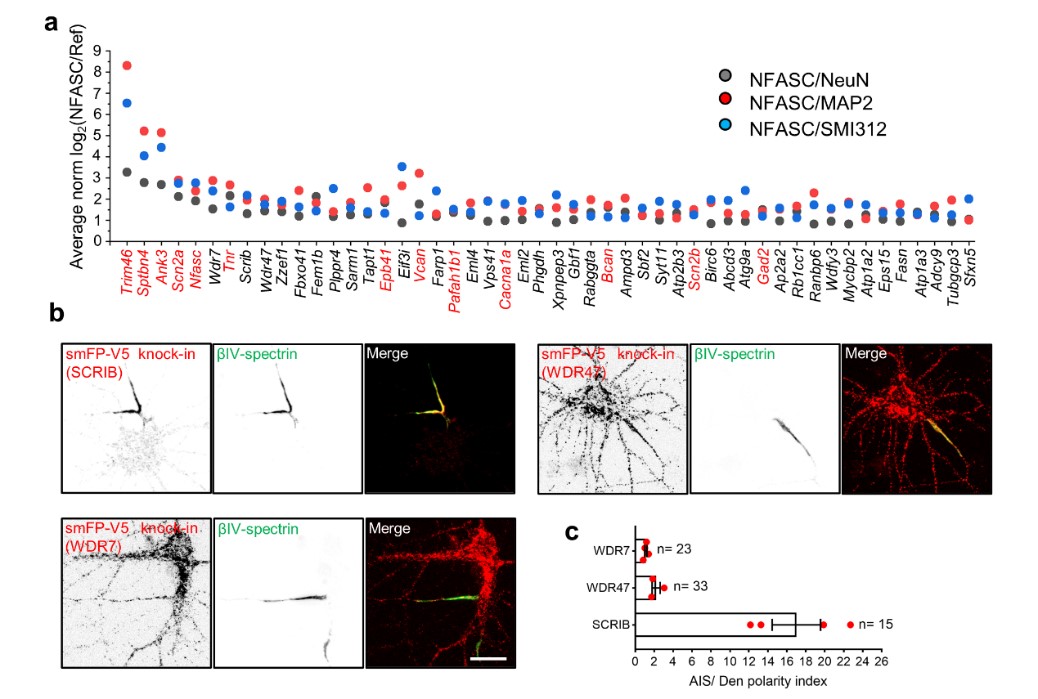
图2. 通过标记内源基因筛选AIS分子
综上,该研究发展了可用于标记神经元亚细胞结构AIS的免疫邻近标记技术,揭示了AIS在神经元发育过程中的蛋白质组动态变化。该蛋白质组数据有助于指导后续针对AIS组分的研究,对深入理解AIS调控神经元兴奋性和引发病理缺陷的机制奠定了基础。
邹鹏和Matthew N. Rasband为该论文的共同通讯作者,北京大学化学与分子工程学院、北大-清华生命科学联合中心已出站博士后张伟博士为该论文的第一作者。该工作得到了国家自然科学基金委、科技部、北京分子科学国家研究中心、生物有机与分子工程教育部重点实验室、北京脑科学与类脑研究所、National Institutes of Neurological Disorders and Stroke和Dr. Miriam and Sheldon G. Adelson Medical Research Foundation的支持。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


