Genome Biology:染色质lncRNA Platr10控制干细胞多能性
来源:本站原创 2021-09-07 13:27
核心干细胞因子基因的特定三维染色体内结构需要将体细胞重编程为多能性。
核心干细胞因子基因的特定三维染色体内结构需要将体细胞重编程为多能性。由于对协调这种结构重塑的表观遗传阅读器知之甚少,作者使用了一种新的染色质RNA原位逆转录测序(CRIST-SEQ)方法来分析Oct4启动子中的长非编码RNA(LncRNAs)。在本研究中发现Platr10作为一种新的染色质RNA分子,通过调节染色质结构和调节核心干细胞因子网络中的DNA甲基化来控制反式作用的多能性。
图片来源:https://doi.org/10.1186/s13059-021-02444-6
通过使用干细胞转录因子Oct4-Sox2-Klf4-c-Myc (OSKM)、小化合物或核转移,终末分化细胞可以重编程进入多能阶段,称为诱导多能干细胞(ipsCs)。然而,这些重新编程的过程极其低效和耗时,阻碍了ipscs在再生医学方面的潜在临床应用。
现在很清楚,在细胞实现完全多能性之前,必须克服强大的表观遗传障碍。细胞重编程向多能性的启动需要核心干细胞因子网络的适当表达。围绕着关键的多能性基因位点的特殊染色质结构,如Oct4,sox2,a n d
Nanog,是参与细胞重塑调节的关键表观遗传步骤的顶峰。多能干细胞的自我更新还需要形成一种特殊的长距离染色体间和染色体内相互作用网络。
为了探索重编程的机制,作者比较了已经完成重编程的ipscs和我们称之为“非ipscs”的细胞(表达慢病毒OSKM因子,但未能完成重编程)之间的启动子dna结合和染色质结构。作者发现病毒表达的OSKM因子在两组细胞中都与它们的目标基因结合。然而,在非ipscs中,靶基因不能被激活以实现多能性,部分原因是缺乏启动子-增强子染色体内环结构。
这种染色体内环的形成是诱导多能性所必须克服的一个关键的表观遗传障碍。此外,维持多能性还需要一种特殊的、更高阶的基因组结构,该基因组结构由远距离染色质相互作用组成。然而,协调这种多能性特异性染色体内网络的分子因素仍未确定。
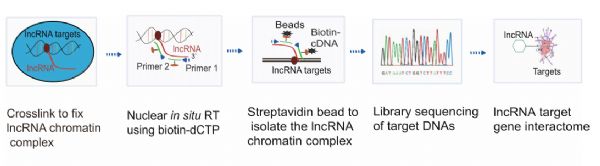
RNA逆转录相关陷阱测序(RAT-seq)示意图
图片来源:https://doi.org/10.1186/s13059-021-02444-6
最近的研究表明,长非编码rna(lncRNAs)是三维核结构的重要结构组成部分。在nu- cleus中,lncrna可以通过多种表观遗传机制在顺式或反式的不同功能步骤调控基因转录,包括与调控元件(启动子和增强子)的结合、染色体间和染色体内的相互作用、组蛋白修饰、DNA甲基化、染色质重塑、以及转录后蛋白质泛素化和降解。最近作者使用染色质RNA原位逆转录测序(CRIST-seq)方法在关键干性基因的调控元件内定位lncRNA网络。
在这篇报告中,作者着重于Platr10在重编程中的作用的机制。作者证明Platr10主要位于细胞核中,通过与多种干细胞核心因子(包括Oct4,Sox2,Klf4和cMyc)结合来调节多能性,这四个因子已用于诱导多能重编程。突变分析表明,Platr10包含Oct4结合元件和TET1结合元件,这两者都是调节干细胞多能性和重编程所必需的。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。