Nature:利用CELLFIE平台有望改善CAR-T细胞疗法
来源:生物谷原创 2025-10-01 09:29
新研究引入了CELLFIE——一个CAR T细胞工程化及高内涵CRISPR筛选平台,使研究人员能够系统化改造CAR T细胞并评估其治疗潜力。
CAR T细胞是源自患者、经过基因工程改造的免疫细胞。它们作为"活体药物",堪称现代医学的里程碑。通过为免疫系统的关键细胞类型——T细胞装备"嵌合抗原受体(CAR)",使其能够特异性识别并攻击癌细胞。
CAR T细胞疗法已通过治愈其他方法无法治疗的血癌患者证明了其潜力。但它对大多数患者仍然无效,这通常源于T细胞固有的功能障碍。为了解决当前局限并从根本上增强CAR T细胞,奥地利科学院分子医学研究中心和维也纳医科大学的科学家开发了一种系统性发现CAR T细胞功能遗传增强因子的新方法。

这项发表于《自然》杂志的新研究引入了CELLFIE——一个CAR T细胞工程化及高内涵CRISPR筛选平台,使研究人员能够系统化改造CAR T细胞并评估其治疗潜力。
少即是多:RHOG基因敲除的CAR T细胞在小鼠模型中击败白血病
"我们的CELLFIE平台可并行测试所有人类基因的敲除效果,并评估哪些基因能使CAR T细胞适应性更强、更持久或更不易耗竭,"该研究的第一作者兼共同指导者、现任美国加利福尼亚州Arc研究所组长的Paul Datlinger解释道。这导致了一个令人惊讶的遗传靶点的发现:在临床前模型中,敲除RHOG基因能显著增强CAR T细胞对抗白血病的效力。
与经过数百万年演化的天然T细胞不同,CAR T细胞通过基因工程获得新功能,但进化上并未对此进行优化。因此,在天然免疫中重要的基因反而可能削弱CAR T细胞功能。
"RHOG就是一个典型例子,"奥地利科学院分子医学研究中心联合第一作者、博士研究生Eugenia Pankevich表示。"它在我们的免疫系统中扮演关键角色,却会降低CAR T细胞的效力。通过CRISPR技术敲除该基因,我们显著提升了CAR T细胞的治疗潜力。"
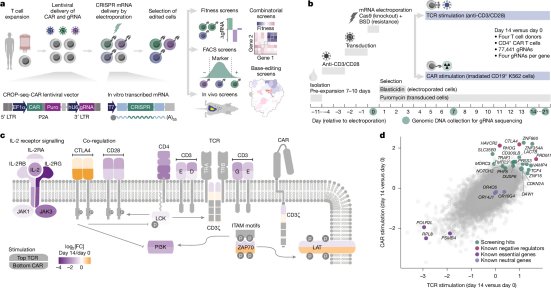
利用CELLFIE平台,研究人员设计并测试了CAR T细胞中数千种基因敲除效果。为了优先筛选最有希望的靶点,他们在临床前小鼠模型中开发了一种新颖的体内CRISPR筛选方法,并验证了多个对CAR T细胞有益的基因敲除。最值得注意的是,与标准CAR T细胞相比,RHOG敲除的CAR T细胞扩增能力更强、更能抵抗耗竭,并能更有效地控制白血病。
未来临床测试的强大组合策略
"我们发现了两个具有互补特性的基因敲除靶点。它们联合使用时效果更强,"奥地利科学院分子医学研究中心联合第一作者、高级NGS技术专家兼科学项目经理Cosmas Arnold解释道。"通过同时靶向RHOG和FAS,我们观察到显著的协同效应——经过基因编辑的CAR T细胞增殖更快、活性更持久、自相残杀现象减少,并能治愈患有侵袭性白血病的小鼠。"
CELLFIE平台为系统化增强细胞疗法提供了灵活框架。通过结合全基因组筛选、组合CRISPR筛选和碱基编辑技术,研究人员创建了一个多功能工具包,用于开发作为疗法的下一代免疫细胞。这种方法可加速发现具有更强持久性、更少副作用及更广适用性的CAR T细胞——不仅适用于血癌,还可能应用于实体瘤、自身免疫疾病和再生医学领域。
"我们的研究为未来临床验证某种特定血癌疗法提供了一个令人兴奋的候选方案,"CeMM首席研究员、维也纳医科大学教授Christoph Bock强调。"同时我们创建了一种广泛适用的方法,用于系统化增强基于细胞的免疫疗法。我们正在学习如何编程细胞,使其成为有效的癌症治疗剂以及针对多种疾病的'活体药物'。"(生物谷Bioon.com)
参考文献:
Paul Datlinger et al, Systematic discovery of CRISPR-boosted CAR T cell immunotherapies, Nature (2025). DOI: 10.1038/s41586-025-09507-9.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


