《自然》:生酮饮食防治肠癌的机制打通了!宾大科学家发现,生酮饮食产生的β-羟丁酸能抑制肠癌的形成和发展
来源: 奇点糕 2022-04-30 08:48
生酮饮食防治肠癌的分子通路终于打通了!
生酮饮食防治肠癌的分子通路终于打通了!
近日,宾夕法尼亚大学的Christoph A. Thaiss和Maayan Levy教授领衔的团队在《自然》发表重要研究成果,破解了生酮饮食抑制肠癌的分子机制[1]。
他们发现生酮饮食的代谢产物β-羟丁酸(BHB,脂肪酸代谢后产生的酮体)可通过与细胞表面受体Hcar2结合,诱导转录调节因子Hopx表达增加,从而抑制肿瘤细胞增殖。
这一发现提示BHB或可作为结直肠癌预防和治疗的补充手段,或可与手术、化疗或免疫治疗起到协同作用,并开启“代谢疗法”的新篇章。

文章首页截图
结直肠癌(CRC)约占到全世界每年确诊癌症人数的10%,是女性的第二大常见癌症,男性的第三大常见癌症,且发病率仍在逐年攀升[2]。
除了遗传因素外,多种特定饮食习惯已被报道与结直肠癌风险增加相关,如西方饮食[3, 4]、高糖饮食[5]和过量摄入动物蛋白(尤其是红肉)[2]等。相比之下,对于是否有饮食习惯能预防或治疗CRC,我们知之甚少。
生酮饮食(极低碳水,高脂肪)是近年来炙手可热的一种饮食方式,多个研究表明其具有抗癌的作用,其抗癌机制包括:促进人体糖代谢产生的细胞毒性物质甲基乙二醛降解(脂肪酸代谢后产生的酮体乙酰乙酸介导)[6]、增加肿瘤抑制蛋白P53的表达(BHB介导)[7],以及改善PI3K抑制剂的抗癌效果[8]等。
作为与饮食最相关的癌症之一,生酮饮食在CRC中对起到什么作用呢?
带着这个问题,Christoph A. Thaiss和Maayan Levy教授团队首先给小鼠准备了6种不同的饮食(蛋白质含量恒定,脂肪/碳水化合物比例不同),其中包括两种生酮饮食,并通过注射偶氮甲烷(AOM)和葡聚糖硫酸钠(DSS)来构建CRC小鼠模型(AOM/DSS诱导CRC小鼠模型)。
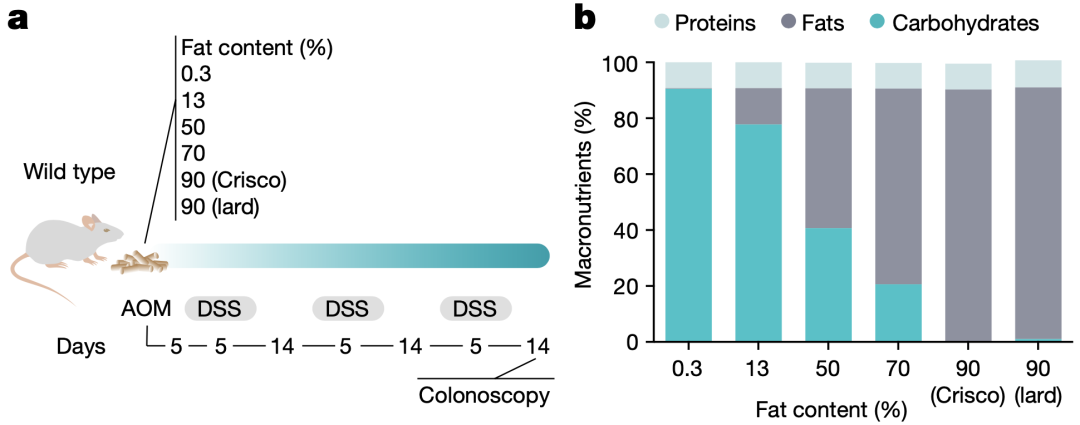
为CRC小鼠模型喂食6种不同的饮食
研究人员发现,随着脂肪/碳水化合物比例的增加,小鼠形成的CRC肿瘤数目减少,体积也更小。并在另一CRC小鼠模型(Cdx2creERTApcfl/fl基因编辑自发CRC小鼠模型)中发现了同样的现象。以上研究初步表明,生酮饮食可抑制肿瘤的发生。
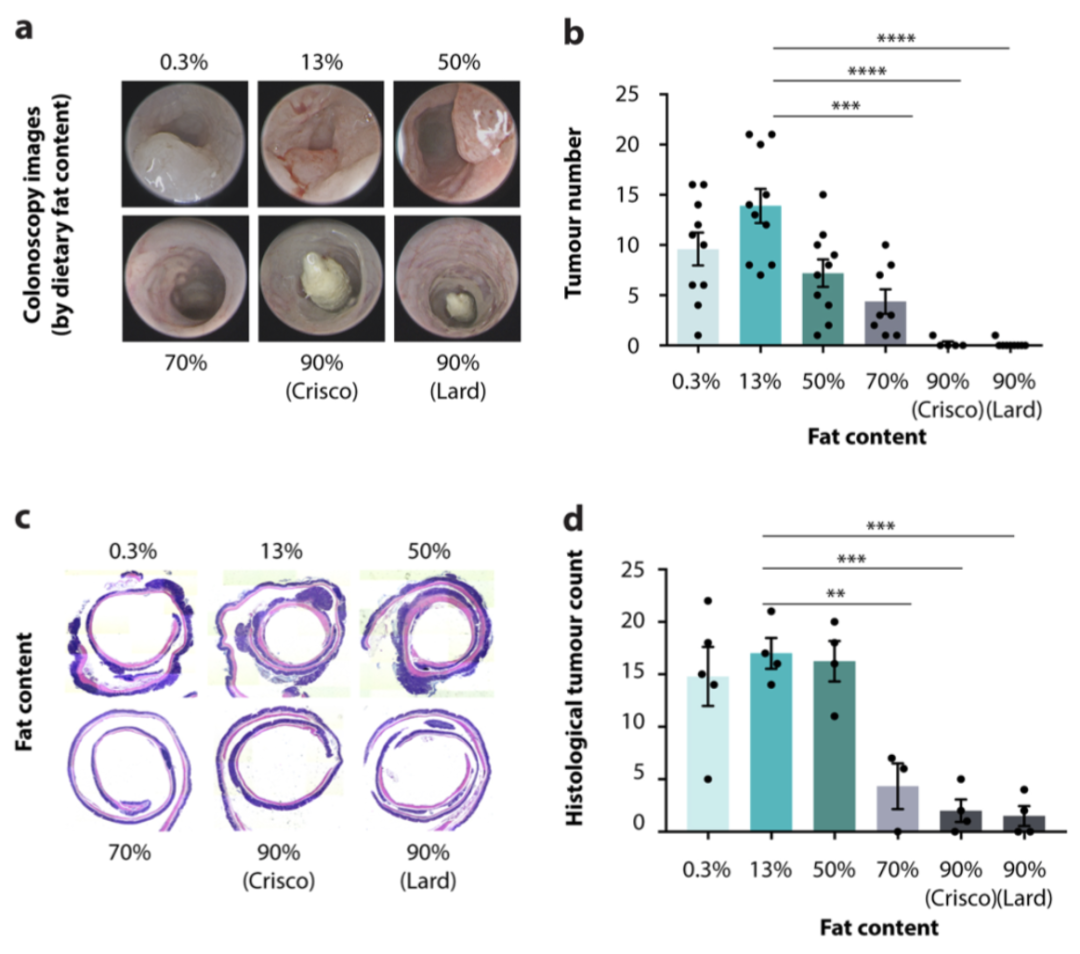
生酮饮食可抑制肿瘤发生
除了抑制肿瘤发生,研究人员发现生酮饮食还可以抑制肿瘤发展。给已形成CRC肿瘤的小鼠喂食生酮饮食后,肿瘤生长明显被抑制,而中断生酮饮食后,肿瘤很快又复发。
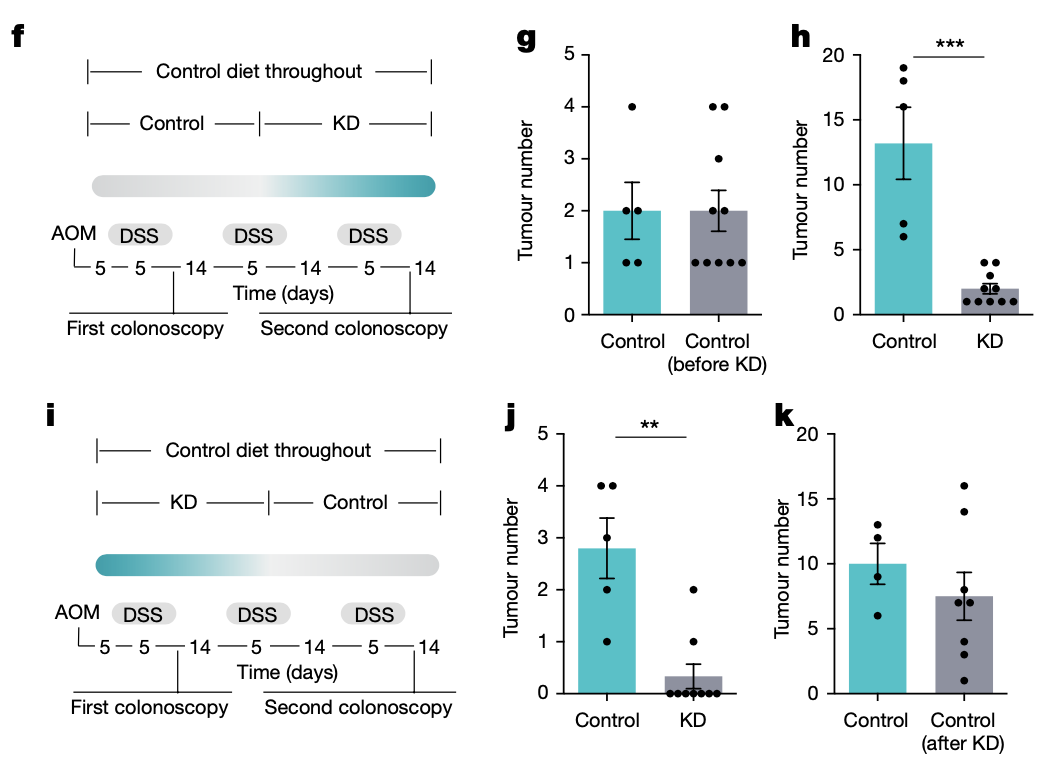
生酮饮食可抑制肿瘤发展
新问题又产生了,生酮饮食是如何抑制肿瘤发生、发展的呢?
研究人员注意到,生酮饮食喂养的小鼠,在正常肠道和长肿瘤的肠道中,肠上皮细胞增殖水平都显著降低,且上皮细胞的凋亡也明显减少。
这表明上皮细胞的更替明显变慢,而上皮细胞的更替是由位于肠隐窝底部的Lgr5+干细胞调节,因此生酮饮食很可能影响到了肠道干细胞的功能。
为了验证这一点,研究人员构建了肠道类器官,并发现来自生酮饮食喂养小鼠的肠道干细胞构建的类器官长的明显不如对照组,这一结果佐证了生酮饮食影响了肠道干细胞的功能这一猜想。
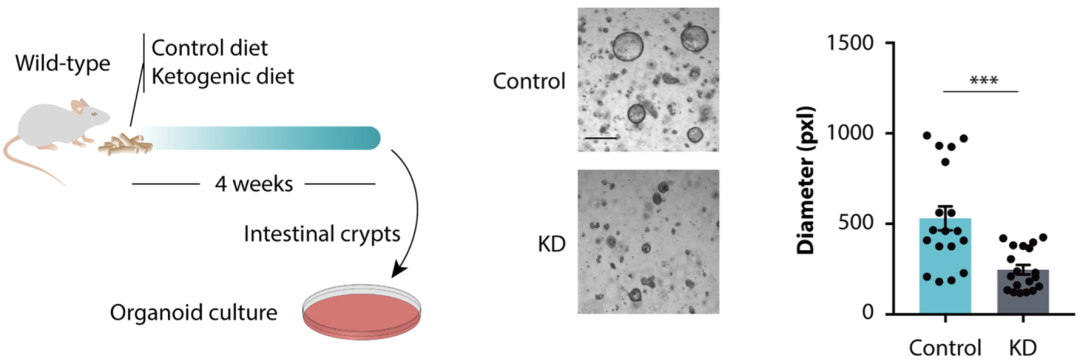
来自生酮饮食喂养小鼠的肠道干细胞构建的类器官长的明显不如对照组
在先前的研究中,生酮饮食的各种功能往往都是由脂肪酸氧化产生的酮体,如乙酰乙酸和BHB介导,因此研究人员首先怀疑生酮饮食对CRC的抑制是由酮体介导。
在培养的肠道类器官中分别添加乙酰乙酸和BHB,添加乙酰乙酸的肠道类器官生长未有变化,而添加BHB的肠道类器官生长受到抑制(BHB达到与生酮饮食喂养小鼠肠道内相似的浓度),同时在CRC类器官中也发现了BHB对肿瘤生长的抑制作用,这表明生酮饮食代谢物BHB很可能是抑制肿瘤生长的关键。
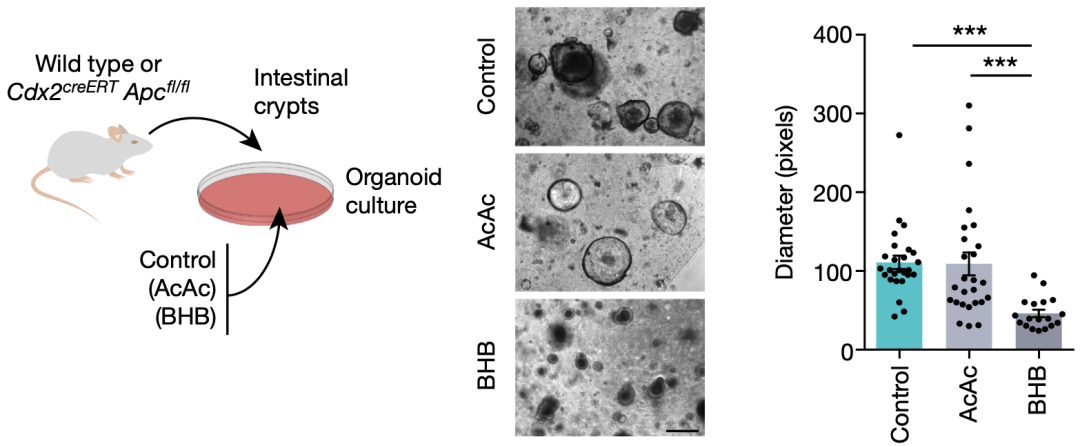
添加BHB的肠道类器官生长受到抑制
在体内实验中,给多种CRC小鼠模型喂食BHB,使其体内浓度达到与生酮饮食小鼠相似的程度,同样可以抑制肿瘤的生长,而喂食乙酰乙酸并不能达到这一效果。这下子板上钉钉了,生酮饮食就是通过BHB来发挥抑癌作用。
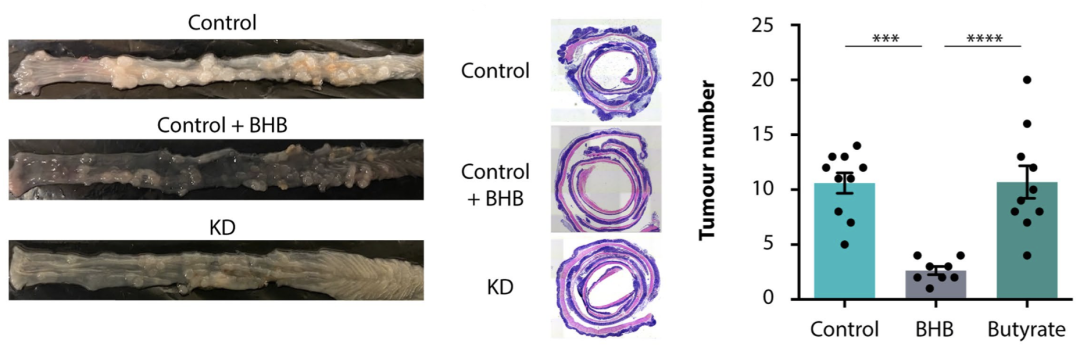
给CRC小鼠喂食BHB同样可以抑制肿瘤的生长
为了寻找下游机制,研究人员对BHB处理后的肠道类器官和对照进行RNA测序,发现BHB处理使得编码抑癌蛋白Hopx的基因表达显著上调。
结合BHB对Hopx功能缺失小鼠来源的肠道类器官缺乏抑制作用,且将肠道类器官中Hopx过表达同样能够达到抑制肠道类器官生长的作用,研究人员猜想BHB的抑癌作用很可能是由Hopx介导的。
为了明确BHB的肿瘤抑制作用是否由Hopx介导,研究人员用生酮饮食喂养长有CRC的Hopx功能缺失小鼠和野生型小鼠,发现野生型小鼠肿瘤受到明显抑制,而Hopx功能缺失小鼠肿瘤则无明显变化。对这两组小鼠的肠道结肠组织进行RNA测序后发现,Hopx功能缺失小鼠肠道组织中增殖相关基因明显上调。
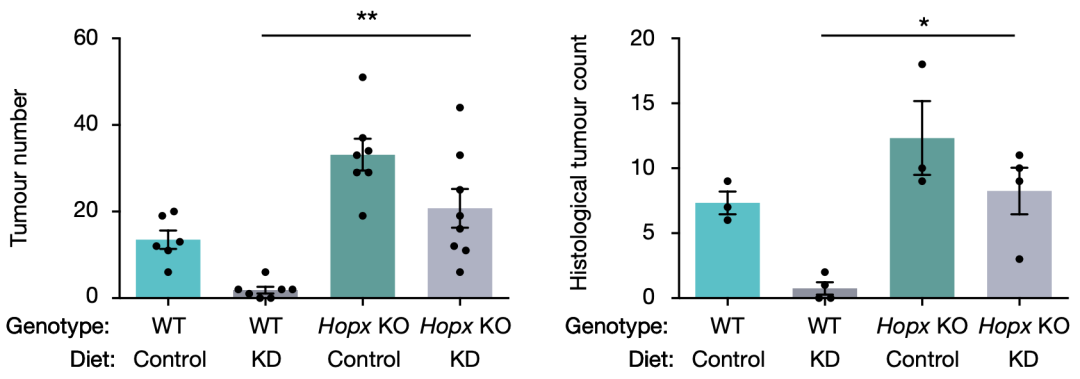
生酮饮食对Hopx功能缺失小鼠肿瘤无明显抑癌效果
这些发现都表明,生酮饮食(或BHB)诱导的Hopx表达增加抑制了肿瘤的生长。那BHB是如何诱导Hopx表达增加呢?
为了寻找BHB与Hopx之间的“桥梁”,研究人员通过CRISPR技术在类器官中筛选BHB的下游基因,包括BHB受体Hcar2和Ffar3,同时还包括受BHB调控的几个基因。
经过实验后发现,BHB对Hcar2功能缺陷类器官的生长无抑制作用,且Hcar2功能缺陷使得BHB上调Hopx基因表达的作用消失。这些结果表明,BHB是通过细胞表面受体Hcar2,诱导Hopx表达来抑制肿瘤的生长。
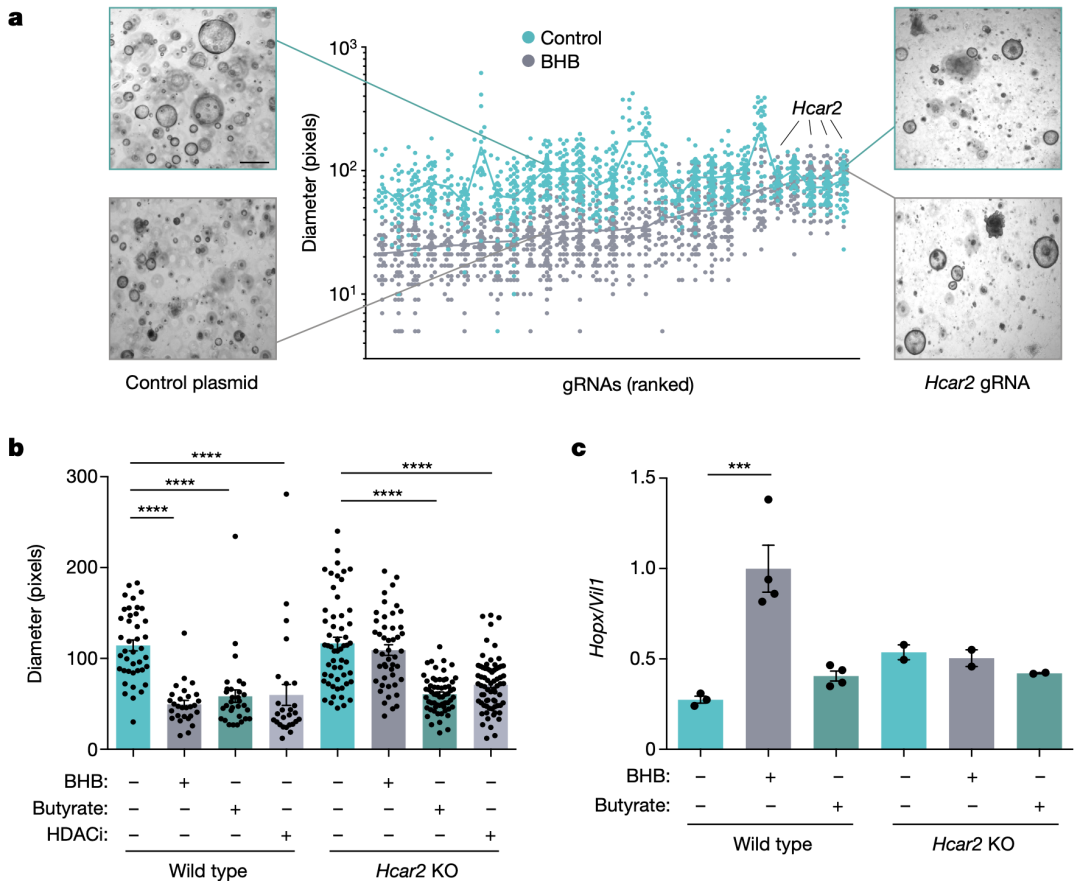
BHB是通过细胞表面受体Hcar2诱导Hopx表达来起到抑制肿瘤生长的作用
最后,研究人员探究了BHB-Hcar2-Hopx通路是否同样能够抑制人肠上皮增生。实验结果表明,BHB可抑制健康人群和CRC患者来源的肠道类器官的生长。
此外,对9名血清BHB水平不同患者的肿瘤和正常结肠组织进行的单细胞RNA测序结果也显示,CRC患者血清中BHB含量与结肠中Hopx表达水平呈正相关,与细胞周期进展呈负相关。这些数据表明,BHB对人肠上皮细胞的增殖同样可起到抑制作用。
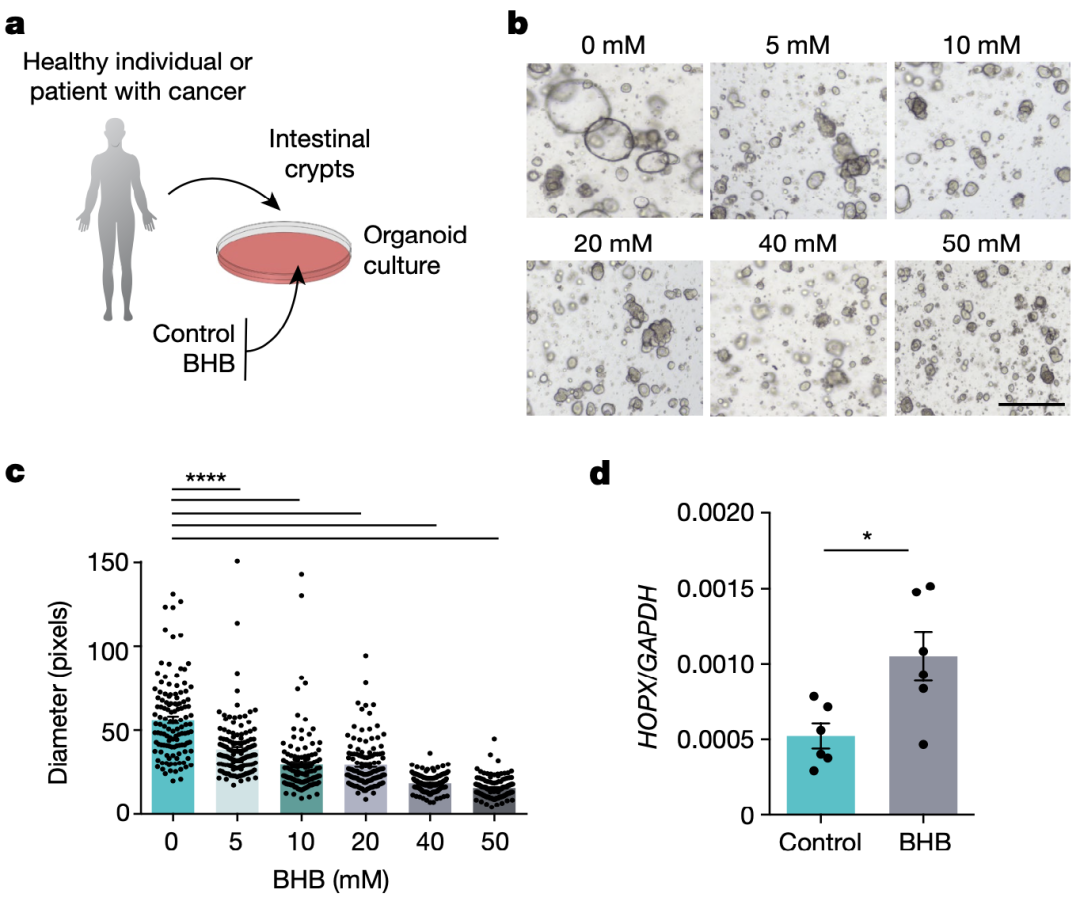
BHB可抑制健康人群和CRC患者来源的肠道类器官的生长
总的来说,研究人员发现了生酮饮食可抑制CRC的发生发展,并阐明了其内在机制:生酮饮食通过BHB-Hcar2-Hopx信号通路抑制肠道肿瘤生长。
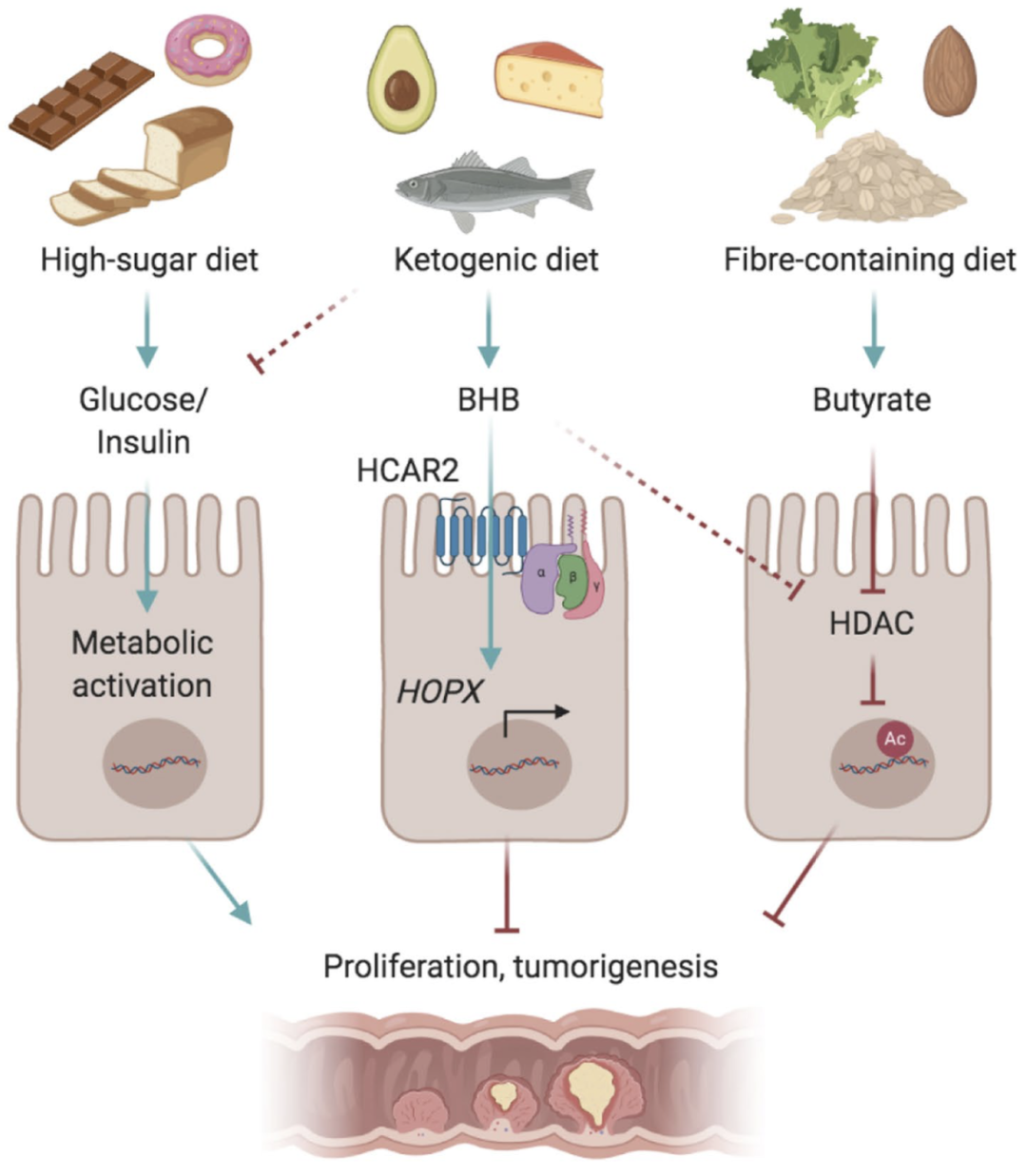
机制示意图
BHB在癌症中的作用目前其实还是不明确的,其作用多种多样,甚至有报道表明BHB具有促进癌症发展的作用[9]。因此,探究不同浓度BHB在不同组织中的作用十分关键,同时也需要进行临床试验来验证这一些临床前研究的结果。
该研究的亮点在于明确了特定的饮食模式可对肿瘤起到抑制作用,尤其是胃肠道肿瘤,其与饮食的关系应该是最密切的,因此该研究的切入点选的很好,证明了病不仅可从口入,还可从口治。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


