Nat Commun:蛋白酶体在氨基酸缺乏时组装在一起诱导癌细胞自杀
来源:本站原创 2021-12-07 10:03
如今,在一项新的研究中,来自加拿大蒙特利尔大学等研究机构的研究人员揭示了负责消除废物的细胞系统的一种新的作用机制。相关研究结果于2021年11月30日发表在Nature Communications期刊上,论文
2021年12月7日讯/生物谷BIOON/---控制细胞产生的废物是人体的一项基本功能,因为这种废物消除机制存在的任何缺陷都可能导致癌症和神经退行性疾病。如今,在一项新的研究中,来自加拿大蒙特利尔大学等研究机构的研究人员揭示了负责消除废物的细胞系统的一种新的作用机制。相关研究结果于2021年11月30日发表在Nature Communications期刊上,论文标题为“Starvation-induced proteasome assemblies in the nucleus link amino acid supply to apoptosis”。论文通讯作者为蒙特利尔大学医学教授El Bachir Affar博士。

Affar及其团队研究了一种叫做蛋白酶体(proteasome)的微型生物机器,它存在于人体的每个细胞中。该微型生物机器负责分解和清除不需要的、有缺陷的或多余的蛋白,这是细胞增殖和正常运作的一个重要过程。此外,这个过程确保了氨基酸的循环利用,而氨基酸是细胞用来制造新蛋白的基本组成部分。然而,人们对蛋白酶体正常功能的确切机制仍然知之甚少。
一种细胞自杀机制
在实验室里,Affar团队发现,在氨基酸缺乏时,蛋白酶体分子会聚集在一起形成一种大型结构,所形成的大型结构通过一种称为细胞凋亡的细胞自杀机制诱导细胞死亡,从而获得新功能。这种机制似乎对维持组织和器官的正常功能很重要。此外,他们发现,这一过程在肿瘤细胞中变得异常,这就证明了它在预防癌症产生方面的重要性。因此,这项新研究为了解正常细胞和癌细胞的运作开辟了许多前景。
具体而言,他们发现哺乳动物的蛋白酶体在氨基酸缺乏时会在细胞核内经历液-液相分离,从而形成蛋白酶体凝聚物。他们把这些蛋白酶体凝聚物称为SIPAN(Starvation-Induced Proteasome Assemblies in the Nucleus, 饥饿诱导的蛋白酶体在细胞核中的组装体),并表明这是哺乳动物细胞对氨基酸缺乏的一种常见反应。SIPAN经历融合事件,迅速与周围环境交换蛋白酶体颗粒,并在氨基酸补充后迅速溶解。
他们进一步发现:(i) SIPAN含有与K48位点偶联的泛素;(ii) 抑制蛋白酶体可加快SIPAN形成;(iii) 抑制去泛素酶可阻止SIPAN溶解;(iv) RAD23B蛋白酶体穿梭因子是SIPAN形成所必需的。
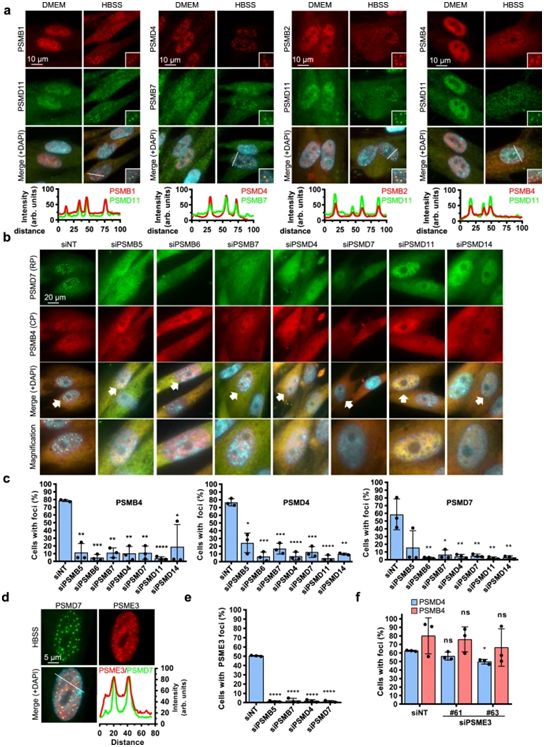
在营养物缺乏时,蛋白酶体的完整性是SIPAN形成所必需的。图片来自Nature Communications, 2021, doi:10.1038/s41467-021-27306-4。
最后,SIPAN的形成与细胞存活率下降和p53介导的细胞凋亡有关,这可能有助于在不同的病理生理条件下的组织适应。
加拿大梅桑那芙-罗斯蒙医院(Maisonneuve-Rosemont hospital)肿学者Pierre Dubé博士说,“这一发现非常令人兴奋。Affar博士和他的团队已经发现了一个新的过程,当它出现问题时,就可以促进癌症产生。这为一个新的研究领域开辟了道路,并可能确定用于癌症治疗的分子靶标。”
利用最近从加拿大卫生研究院获得的资助,Affar计划确定蛋白酶体为何以及如何协调它们自己组装成SIPAN。他的团队将使用最先进的工具和方法来了解SIPAN的生物功能和作用机制。
Affar团队的研究将有助于提高科学家们对正常细胞中蛋白酶体功能机制的认识。他说,通过强调导致蛋白酶体在疾病中出现功能异常的缺陷,可以为治疗癌症的临床干预措施找到更好的治疗靶标。(生物谷 Bioon.com)
参考资料:
Maxime Uriarte et al. Starvation-induced proteasome assemblies in the nucleus link amino acid supply to apoptosis. Nature Communications, 2021, doi:10.1038/s41467-021-27306-4.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


