Gut | 再添益处!南方医科大学李壮团队发现葛根素缓解动脉粥样硬化的潜在机理
来源:生物探索 2024-06-05 09:37
研究表明,通过干预减少TMAO的产生可导致动物和人类AS症状的减轻。
南方医科大学李壮团队在Gut(IF 25)在线发表题为“Puerarin alleviates atherosclerosis via the inhibition of Prevotella copri and its trimethylamine production”的研究论文,该研究发现葛根素通过抑制Prevotella copri 及其三甲胺的产生来缓解动脉粥样硬化。PU通过调节肠道微生物群来缓解AS,这可以从PU处理的小鼠到饲喂HFD的ApoE-/-小鼠的FMT后肠道微生物群组成的改变和AS的改善中得到证明。
具体来说,PU降低了P. copri 的丰度,通过产生三甲胺(TMA)加剧了AS。长时间的单定殖P. copri 破坏了PU对AS的有益作用。在临床中,AS患者的斑块评分与P. copri 丰度和血浆氧化三甲胺(TMAO)水平呈正相关。为期1周的口服PU干预有效降低颈动脉斑块患者P. copri 水平和TMAO浓度。因此,PU可能通过靶向P. copri及其TMA的产生来治疗AS。

心血管疾病(CVD)构成了重大的全球公共卫生挑战,其中动脉粥样硬化(AS)是主要诱因尽管取得了显著的医学进展,但仍然需要有效地解决AS的治疗策略。食用和药用植物由于其固有的天然和安全特性,作为预防和管理包括AS在内的慢性疾病的一种新方法,引起了人们的广泛关注。
葛根素(PU)是在葛根中发现的一种天然化合物,自20世纪50年代末以来一直被认为是最重要的活性化合物之一,具有公认的心血管益处,其抗动脉粥样硬化的特性已通过减少炎症和改善血脂水平得到证实。然而,PU在水和脂质中的溶解度有限,导致生物利用率低,阻碍了对这些效应背后机制的清晰理解。
AS的持续高发病率可归因于多种因素,包括遗传和高脂肪饮食(HFD)等环境影响肠道微生物组越来越被认为是理解HFD对AS影响的关键因素。特别是,针对肠道微生物群的治疗干预已被证明具有增强与HFD相关的代谢健康的潜力。
所有这些证据表明,肠道微生物群在介导与HFD相关的心脏代谢健康中起着关键作用。通常,肠道微生物群的复杂生态系统会对HFD做出反应,并通过各种过程积极参与人体代谢健康的调节,包括营养吸收、生长发育、生物屏障的维持、免疫调节和代谢。
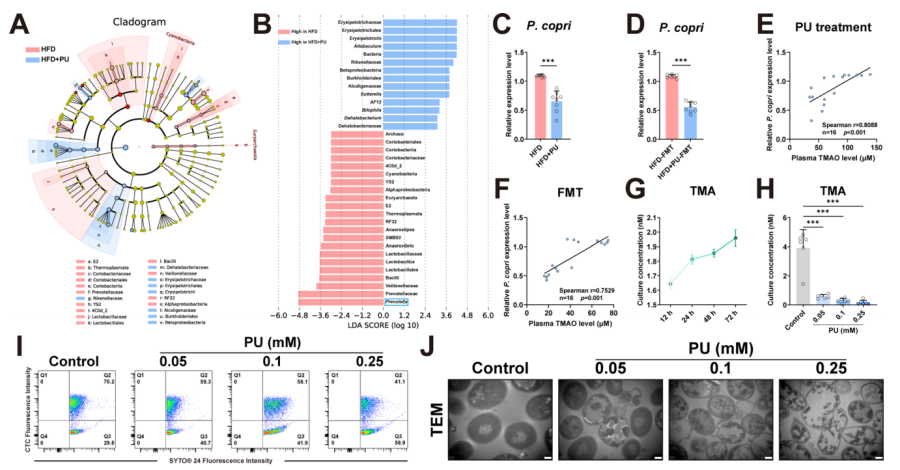
PU降低了P. copri的丰度和TMA的产量(Credit: Gut)
肠道菌群有规律地分泌代谢物,包括短链脂肪酸和次级胆汁酸,对心血管有益。相反,三甲胺(TMA)由肠道微生物群产生,被吸收到血液中,随后被运送到肝脏,在那里它被氧化形成三甲胺N-氧化物(TMAO)。氧化三甲胺通过直接刺激炎症和干扰胆固醇的反向运输,参与加速动脉粥样硬化病变的发展。该化合物已被确定为AS的独立预测因子和促进因子。研究表明,通过干预减少TMAO的产生可导致动物和人类AS症状的减轻。因此,针对TMAO治疗AS的治疗策略的探索正在获得动力。
该研究确定P. copri 是一种重要的细菌物种,通过促进TMAO在小鼠和人类中的积累而加重AS。PU的干预已经显示出通过抑制P. copri 降低TMAO水平的有希望的结果。该研究阐明了PU通过抑制ApoE−/−小鼠和颈动脉斑块患者的P. copri 及其TMA的产生来缓解AS的作用,强调了其在临床实践中对抗AS的新治疗潜力。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


