Nature:IL-27——肿瘤免疫治疗的新突破,增强T细胞活力的关键因子!
来源:生物探索 2025-02-09 10:15
IL-27作为一种具有独特免疫学优势的调节因子,未来在肿瘤免疫治疗中的应用前景广阔。
肿瘤免疫治疗已是癌症治疗的重要方向,尤其是免疫检查点抑制剂(如PD-1/PD-L1抑制剂)的成功应用,使得癌症治疗迎来了新的曙光。然而,即使这些治疗方法在部分患者中表现出显著疗效,仍有大量患者未能得到有效的治疗。这种现象背后,隐藏着肿瘤免疫逃逸和免疫耐受的复杂机制。因此,如何激发和维持抗肿瘤免疫反应,尤其是增强肿瘤特异性CD8+ T细胞(CTLs)的功能,成为了肿瘤免疫治疗研究中的关键课题。
在这一背景下,2月5日Nature的研究报道“IL-27 elicits a cytotoxic CD8+ T cell program to enforce tumour control”,研究人员发现IL-27(白细胞介素-27)作为一种重要的免疫细胞因子,具有调节免疫反应的潜力。IL-27不仅在调节T细胞的生长和分化中扮演着至关重要的角色,它还能在肿瘤微环境中促进CD8+ T细胞的持久性和效能,从而增强其对肿瘤的免疫攻击作用。IL-27的作用特别引人注目,因为它不仅能提高抗肿瘤T细胞的效能,还能在与其他免疫检查点抑制剂联合应用时,产生协同作用,进一步提高治疗效果。
该研究深入探讨了IL-27在小鼠肿瘤模型中的作用,发现IL-27通过直接作用于肿瘤特异性CD8+ T细胞,显著提升了它们的抗肿瘤功能和持续性。通过过表达IL-27或使用半衰期延长的IL-27蛋白,研究人员成功地诱导了肿瘤的消退,同时未出现明显的免疫相关毒性。此外,IL-27与PD-L1抑制剂的联合使用,进一步验证了它在免疫治疗中的潜力。这些发现不仅为肿瘤免疫治疗提供了新的思路,也为未来开发更加有效的免疫治疗策略奠定了基础。
通过该研究,IL-27被重新定义为一种具有强大潜力的免疫调节因子,不仅为肿瘤免疫治疗提供了新的希望,也为其他免疫相关疾病的治疗开辟了新的方向。在未来,IL-27的临床应用可能会成为癌症免疫治疗领域的重要突破,特别是在那些对现有治疗反应不佳的患者中。

肿瘤免疫治疗的新曙光
肿瘤免疫治疗已经成为现代癌症治疗的重要组成部分。通过激活患者自身的免疫系统,特别是调动T细胞等免疫细胞对抗肿瘤,免疫治疗为许多癌症患者带来了新的生机。尤其是免疫检查点抑制剂(如PD-1/PD-L1抑制剂)在多种癌症中展现了显著的疗效,改变了传统的治疗模式,为癌症患者带来了突破性的进展。
然而,尽管免疫治疗取得了令人瞩目的成就,但仍有大量患者未能从中获益。临床实践中,免疫治疗并非对所有患者有效,这背后隐藏着许多复杂的机制。一项关键原因在于肿瘤免疫微环境(TME)的复杂性,肿瘤细胞往往能够通过免疫逃逸机制避免免疫系统的攻击。例如,肿瘤微环境中的免疫抑制性细胞和分子,尤其是免疫检查点分子(如PD-1和CTLA-4),通过阻止T细胞的激活和效能,使得免疫系统在肿瘤面前失去战斗力。
即便如此,免疫检查点抑制剂仍然是目前免疫治疗中最常见的策略。然而,只有部分患者能够从中获得持续的治疗效果。根据最新的研究数据,尽管PD-1/PD-L1抑制剂在一些肿瘤类型中产生了令人瞩目的反应,但大约70%的患者对这种治疗没有明显的反应。这一现象表明,免疫治疗的效果并不仅仅取决于肿瘤的类型,更受到个体免疫反应的差异性、肿瘤免疫逃逸机制以及肿瘤微环境等多重因素的影响。
此外,免疫治疗的副作用也是一个不可忽视的问题。尽管相比传统化疗,免疫治疗的副作用较小,但它仍可能引起免疫系统过度激活,导致免疫相关的毒性反应,甚至危及患者的生命。因此,寻找新的免疫调节因子和治疗方法,能够增强免疫治疗效果并减少毒性,成为当前肿瘤免疫治疗研究的焦点之一。
CD8+ T细胞:肿瘤免疫中的关键角色
CD8+ T细胞,作为免疫系统中的“杀手细胞”,在抗肿瘤免疫中扮演着至关重要的角色。它们通过识别并杀伤肿瘤细胞,直接执行肿瘤的免疫清除任务。具体来说,CD8+ T细胞通过其T细胞受体(TCR)识别肿瘤细胞表面特有的抗原,启动细胞毒性反应,释放细胞毒性分子如穿孔素和格朗津B(GZMB),这些分子能够有效杀死肿瘤细胞,从而抑制肿瘤的生长。
尽管CD8+ T细胞在肿瘤免疫中发挥着至关重要的作用,但它们面临着肿瘤微环境(TME)中的重重挑战。在肿瘤的免疫逃逸过程中,肿瘤细胞通过一系列复杂的机制抑制CD8+ T细胞的功能和持久性。研究表明,肿瘤微环境往往充斥着免疫抑制分子,这些分子能通过调节免疫检查点(如PD-1和CTLA-4)降低CD8+ T细胞的活性。此外,肿瘤细胞通过分泌免疫抑制性细胞因子,改变TME中的细胞组成,使得CD8+ T细胞的功能进一步受到抑制,甚至引发免疫耐受。
更令人担忧的是,肿瘤中的CD8+ T细胞可能会逐渐进入“衰竭”状态。研究发现,在肿瘤免疫逃逸的过程中,CD8+ T细胞可能表现出一系列功能性缺陷,表现为细胞毒性分子如GZMB的表达下降以及免疫标记物如PD-1的上调,这使得这些T细胞无法有效清除肿瘤细胞。尤其是在持续的抗原刺激下,CD8+ T细胞逐渐出现功能衰竭现象,无法维持持久的抗肿瘤反应。这一现象是肿瘤免疫治疗面临的一个巨大难题。
IL-27:免疫调节因子的潜力
IL-27(白细胞介素-27)是一种由EBI3和p28亚基组成的异二聚体细胞因子,属于IL-6/IL-12细胞因子家族。它在免疫反应中的作用非常独特,不仅参与T细胞的活化与分化,还通过细胞内信号传导增强免疫系统对肿瘤的应答。IL-27的免疫学特性使其成为肿瘤免疫治疗的一个潜力巨大的靶点。
IL-27最初被认为在调节免疫反应中发挥多方面作用,特别是对CD4+ T细胞的影响。然而,最新的研究揭示,IL-27对CD8+ T细胞的功能也至关重要。在肿瘤免疫中,IL-27通过直接作用于肿瘤特异性CD8+ T细胞,促进这些细胞的活性和持久性,从而增强其抗肿瘤能力。研究数据表明,在小鼠模型中,IL-27的存在显著提升了肿瘤特异性CD8+ T细胞的数量和功能。具体来说,IL-27能够增强CD8+ T细胞的增殖,并通过增加GZMB等细胞毒性分子的表达,增强这些细胞的杀伤肿瘤细胞的能力。
IL-27在肿瘤免疫中发挥着至关重要的作用,特别是在促进CD8+ T细胞的激活、增殖和效能方面(Credit: Nature)
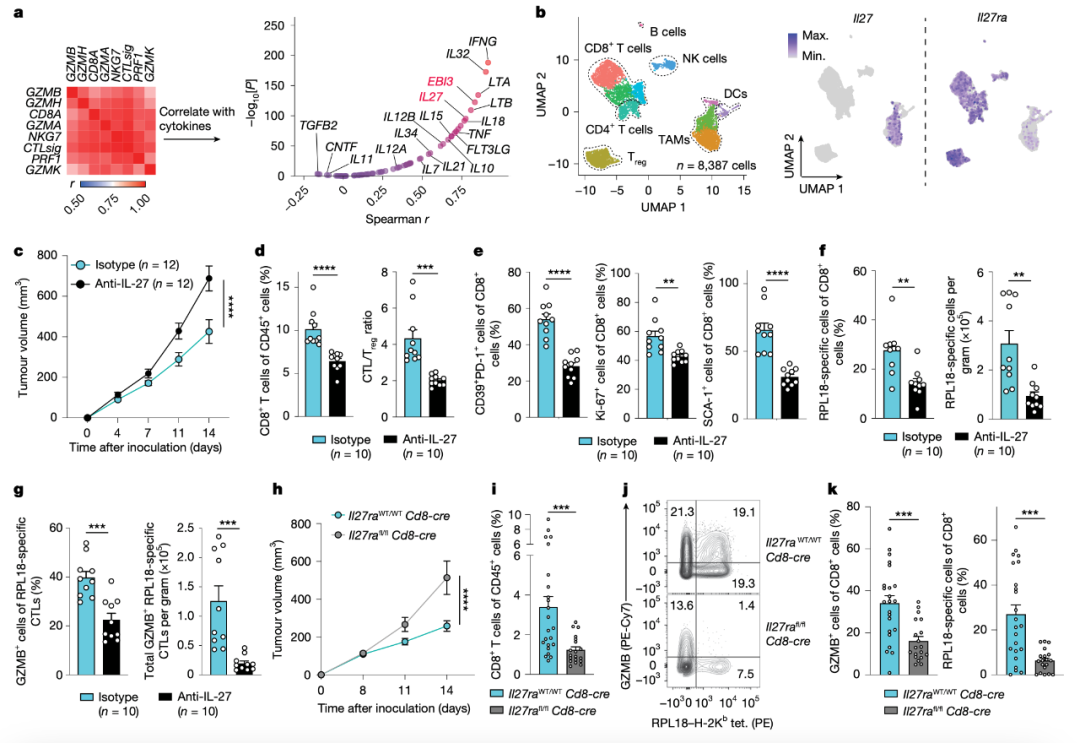
IL-27与CTLs在人体肿瘤中的相关性:在人体黑色素瘤的TCGA-SKCM数据库中,使用Spearman相关性分析,研究了75种免疫相关细胞因子与CD8+细胞毒性T细胞(CTLs)标志基因(CTLsig)表达的关系。结果显示,IL-27的表达与CTLsig呈显著正相关,表明IL-27可能在调节肿瘤免疫反应中起到关键作用。
MC38小鼠模型中的IL-27和IL-27RA表达情况:通过UMAP可视化分析,展示了MC38肿瘤模型中CD45+细胞的分布情况,并且分析了Il27和Il27ra的表达。结果表明,肿瘤相关巨噬细胞(TAMs)和T细胞中均表达IL-27和IL-27RA,提示IL-27在肿瘤免疫反应中的重要作用。
IL-27对肿瘤免疫反应的影响:在小鼠MC38肿瘤模型中,使用抗IL-27抗体进行治疗,结果显示:
肿瘤生长:IL-27治疗显著抑制了肿瘤生长
CTL频率和CD8+T细胞/Treg细胞比例:IL-27治疗组的CTL频率显著增加,CD8+T细胞与Treg细胞的比例也得到了改善,表明IL-27有助于促进有效的抗肿瘤免疫反应。
CTL激活标志物表达:IL-27治疗组CTLs的激活标志物表达显著提高,表明IL-27增强了CTLs的活性。
RPL18特异性CTL频率:IL-27治疗组中,RPL18特异性CTL的频率和绝对数目明显增多,表明IL-27对肿瘤特异性CTL的扩增具有重要作用。
GZMB表达:IL-27治疗组RPL18特异性CTL中GZMB的表达也显著增加,表明IL-27增强了CTL的细胞毒性功能。
IL-27对CD8+ T细胞的影响:在IL-27RA基因缺失的小鼠模型中(Il27rafl/fl Cd8-cre与Il27raWT/WT Cd8-cre小鼠),研究发现IL-27RA的缺失导致CD8+ T细胞在肿瘤中的频率和效应分子(如GZMB)的表达下降,肿瘤生长也加速。这进一步表明IL-27通过直接作用于CD8+ T细胞,是抗肿瘤免疫反应的重要调节因子。
IL-27的作用通过其在细胞内的信号传导途径实现,尤其是通过激活STAT1和STAT3这两种关键的转录因子。研究显示,IL-27通过其受体IL-27RA(白细胞介素-27受体α)与gp130(白细胞介素-6受体相关蛋白)结合后,启动JAK-STAT信号通路,特别是STAT1和STAT3的激活。这一过程促进了CD8+ T细胞的增殖、效应分子的产生(如GZMB和IFN-γ),并增强了这些细胞在肿瘤微环境中的持久性。此外,IL-27还能通过增强SCA-1等标记物的表达,促进CD8+ T细胞向具有更强记忆功能的效应细胞转化,从而提高其抗肿瘤的持续性和效率。
更重要的是,IL-27不仅通过增强CD8+ T细胞的直接抗肿瘤效应来发挥作用,它还能够抑制肿瘤微环境中免疫抑制因子的作用。研究显示,在IL-27的调节下,CD8+ T细胞的免疫逃逸标志物(如PD-1)的表达得到抑制,减少了CD8+ T细胞的“衰竭”现象,从而保持了它们的高效杀伤功能。这表明,IL-27通过促进CD8+ T细胞的效能,同时限制了肿瘤免疫逃逸的能力,增强了整体的抗肿瘤免疫反应。
临床前景:IL-27的免疫治疗潜力
随着肿瘤免疫治疗的不断进步,IL-27作为一种新兴的免疫调节因子,展现出了巨大的治疗潜力。IL-27不仅能增强肿瘤特异性CD8+ T细胞的抗肿瘤效能,还能够改善肿瘤微环境,降低免疫耐受的发生。基于这一特点,IL-27在癌症免疫治疗中的应用前景值得关注,并且与现有的免疫检查点抑制剂的协同作用,为提高免疫治疗的整体疗效提供了新的思路。
研究数据显示,IL-27在小鼠模型中的效果非常显著。当小鼠肿瘤达到一定大小时,应用IL-27治疗能够显著减少肿瘤体积,并促进肿瘤特异性CD8+ T细胞的增殖和效能。这些数据为IL-27在肿瘤免疫治疗中的应用奠定了基础。在实验中,IL-27的过表达或半衰期延长形式,能够在小鼠体内长期维持高水平的IL-27,从而持续增强抗肿瘤免疫反应。与此同时,IL-27的治疗不引起明显的免疫相关毒性,表明它在安全性方面具有潜在优势。
更为重要的是,IL-27与现有免疫检查点抑制剂(如PD-L1抑制剂)的联合使用,表现出了协同效应。研究中发现,IL-27的应用与PD-L1抑制剂结合使用时,能够显著提高抗肿瘤T细胞的数量和效能,增强肿瘤的控制效果。在小鼠模型中,IL-27与PD-L1抗体的联合治疗不仅促进了CD8+ T细胞的激活,还有效降低了肿瘤的生长速度,并提高了完全缓解的发生率。这一发现表明,IL-27不仅可以单独提升免疫反应,还能与免疫检查点抑制剂协同作用,从而克服单一治疗的局限性,提供更加全面的治疗方案。
此外,IL-27的协同效应不仅体现在其与PD-L1抑制剂的联合使用。研究还显示,IL-27与其他免疫治疗策略的组合(如抗-CTLA-4抗体)同样能产生协同效果,进一步增强了肿瘤的免疫控制能力。这些发现意味着,IL-27不仅可以单独作为免疫治疗的补充,还能作为联合治疗策略中的重要组成部分,为肿瘤患者提供更为多样化的治疗选择。
未来,随着对IL-27作用机制的深入理解和临床研究的不断推进,IL-27有望成为癌症免疫治疗的关键组成部分。特别是在联合免疫疗法中,IL-27的应用可能成为突破目前治疗瓶颈的关键因素,帮助那些对传统治疗反应不佳的患者获得更好的治疗效果。通过持续优化IL-27的临床应用方案,提升其安全性、有效性和耐受性,IL-27有望在癌症免疫治疗中实现突破,为全球癌症患者带来新的治疗选择和希望。
总的来说,IL-27作为一种具有独特免疫学优势的调节因子,未来在肿瘤免疫治疗中的应用前景广阔。随着对其作用机制的深入研究和临床试验的不断推进,IL-27有可能成为新一代免疫治疗的重要武器,推动癌症免疫治疗走向更加精准和高效的未来。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


