Cell子刊:王红阳院士团队发现肝癌的新型防护因子——LTA4H
来源:生物世界 2025-03-10 11:00
该研究表明,LTA4H 通过靶向 HNRNPA1/LTBP1/TGF-β 信号轴,改善肿瘤微环境并阻止肝细胞癌(HCC)进展。
肝细胞癌(HCC)是最常见的原发性肝癌,是全球第六大常见的癌症和第三大癌症相关死亡原因。许多患者确诊时已处于晚期,限制了根治性疗法的选择,导致预后不良,其特点是 5 年生存率低,手术后频繁复发。
肝细胞癌的固有异质性进一步复杂化了治疗策略。病毒性肝炎、酒精相关性肝病和非酒精性脂肪性肝病等因素导致的慢性肝损伤和炎症是肝细胞癌发病机制的基础,炎症介质严重影响肿瘤微环境(TME)并驱动肝细胞癌的进展。
2025年3月7日,复旦大学附属肿瘤医院/上海东方肝胆外科医院/国家肝癌科学中心王红阳院士、陈磊研究员等在 Cell 子刊 Cell Reports Medicine 上发表了题为:LTA4H improves the tumor microenvironment and prevents HCC progression via targeting the HNRNPA1/LTBP1/TGF-β axis 的研究论文。
该研究表明,LTA4H 通过靶向 HNRNPA1/LTBP1/TGF-β 信号轴,改善肿瘤微环境并阻止肝细胞癌(HCC)进展。

了解肿瘤微环境(TME)内的免疫逃逸机制对于改善肝细胞癌的免疫治疗效果至关重要。肿瘤相关巨噬细胞(TAM)在肝细胞癌中数量众多,通常呈现 M2 样巨噬细胞表型,是潜在的治疗靶点。TGF-β 和 CCL2 等趋化因子对于 TAM 的募集和功能重塑至关重要。通过趋化因子信号重编程 TAM 可能与免疫检查点抑制剂(ICI)产生协同作用,不过仍需进一步研究以优化组合并确定用于患者分层的预测性生物标志物。
有效的预测性生物标志物对于解决肝细胞癌患者反应的异质性至关重要。有研究证据表明,RNA 测序数据能够从肿瘤微环境中识别出治疗反应的预测性特征。然而,将这些特征转化为可通过免疫组织化学(IHC)测量的参数仍然具有挑战性,而这是推进临床应用所必需的。
白三烯 A4 水解酶(LTA4H)是一种具有多种功能的锌金属酶,具有环氧化物水解酶和氨肽酶活性。它催化白三烯 A4(LTA4)转化为白三烯 B4(LTB4),LTB4 是一种强效的炎症介质,通过白三烯 B4 受体 1(BLT1)和白三烯 B4 受体 2(BLT2)发挥作用。LTA4H 在包括食管癌、皮肤癌、卵巢癌和结直肠癌在内的多种恶性肿瘤中高表达,通过促进细胞增殖来推动肿瘤进展。然而,其在肝癌中的作用,尤其是在调节肿瘤微环境方面的作用,仍知之甚少。
在这项最新研究中,研究团队揭示了 LTA4H 在肝细胞癌(HCC)发生和发展过程中的保护作用。LTA4H 在人类肝细胞癌以及小鼠肝细胞癌肿瘤中表达下调。LTA4H 缺乏通过抑制 JNK 激活,加剧肝细胞损伤,并通过上调 LTBP1 表达以及下游 TGF-β 的分泌和活化促进 CD206+ 巨噬细胞极化。
从机制上来说,LTA4H 诱导异质性核核糖核蛋白 A1(HNRNPA1)磷酸化,增强它们之间的相互作用,从而导致 HNRNPA1 在调节核内 LTBP1 mRNA 成熟和加工方面的功能受到抑制。
该研究还发现,LTA4H 缺陷型肝细胞癌患者的预后不良且对免疫疗法有抗性。靶向 TGF-β 和 PD-1 的联合疗法,显著改善了 LTA4H 基因敲除的 Hepa1-6 肿瘤对免疫疗法的耐药性。
该研究的核心发现:
-
LTA4H 的低表达促进肝细胞癌的发生和发展;
-
LTA4H通过 LTBP1 介导的 TGF-β 激活促进 CD206+ 巨噬细胞的增殖;
-
LTA4H 以 HNRNPA1 依赖的方式阻止 LTBP1 mRNA 的成熟和加工;
-
TGF-β 阻断使 LTA4H 缺陷的肝细胞癌对免疫治疗增敏。
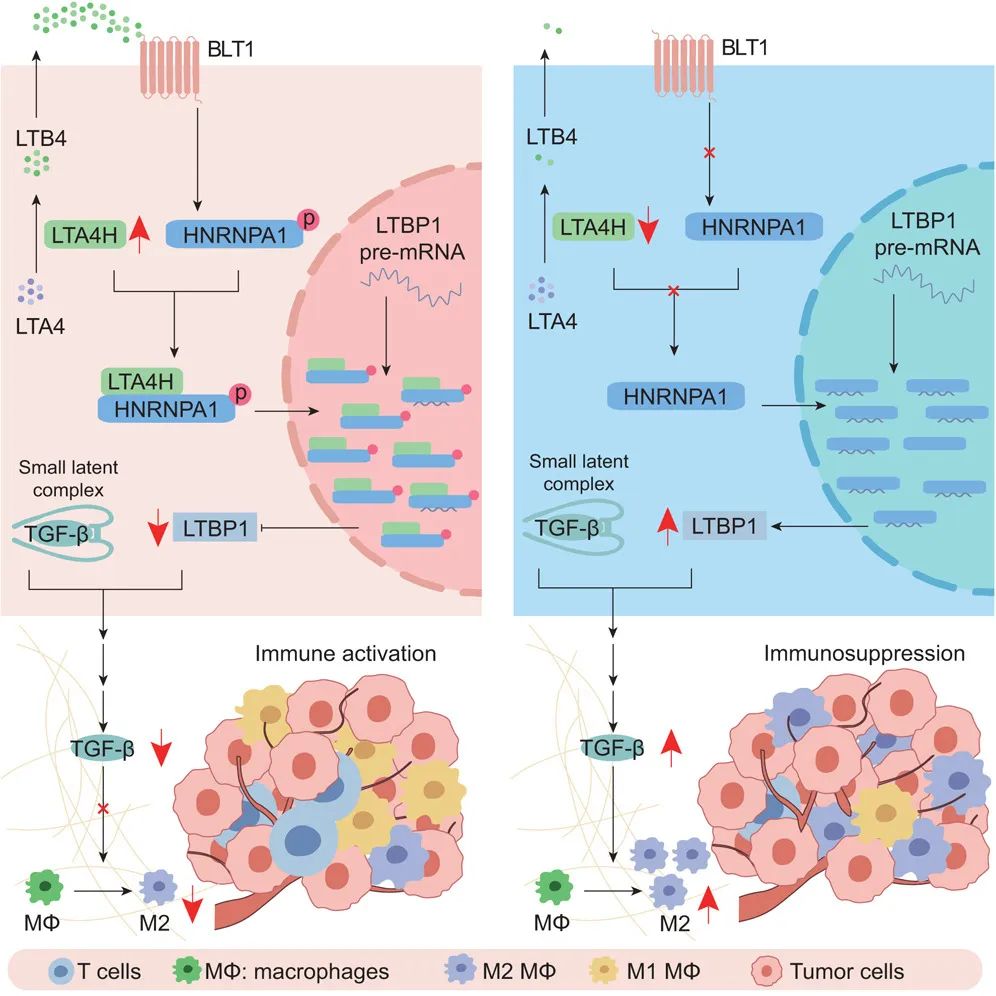
总的来说,这些研究结果揭示了 LTA4H 在调控肿瘤微环境方面此前未被报道的作用,并为 LTA4H 缺陷型肝细胞癌患者的潜在诊断和治疗策略提供了新见解。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


