2020年8月Science期刊不得不看的亮点研究
来源:本站原创 2020-08-31 22:12
2020年8月31日讯/生物谷BIOON/---2020年8月份即将结束了,8月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Science:新研究揭示细胞是走迷宫高手doi:10.1126/science.aay9792在一项新的研究中,来自英国多个研究机构的研究人员发现了细胞为何能够如此准确地在人体中迁移。相关研究结
2020年8月31日讯/生物谷BIOON/---2020年8月份即将结束了,8月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Science:新研究揭示细胞是走迷宫高手
doi:10.1126/science.aay9792
在一项新的研究中,来自英国多个研究机构的研究人员发现了细胞为何能够如此准确地在人体中迁移。相关研究结果发表在2020年8月28日的Science期刊上,论文标题为“Seeing around corners: Cells solve mazes and respond at a distance using attractant breakdown”。在这篇论文中,他们描述了他们开发的一种解释细胞定向运动(cell orienteering)的理论,以及他们如何使用迷宫对它进行测试。
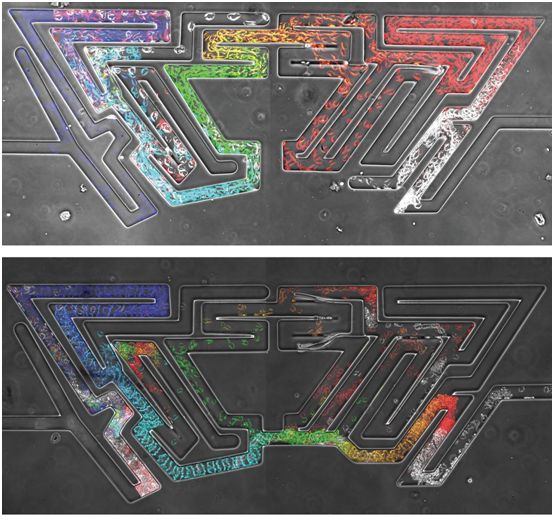
当身体受伤时,例如被针头戳伤,免疫系统的反应是派遣白细胞来杀死任何可能试图通过伤口进入体内的细菌。但是细胞通过什么方式找到伤口的呢?先前的研究已表明,细胞利用体内称为化学吸引剂(chemoattractant)的化学物来进行短距离导航。白细胞可以感知化学吸引剂并向它们移动---但是这仅在短距离内有效。在这项新的研究中,这些研究人员发现,细胞可以以不同的方式使用这样的化学吸引剂来导航更长和更复杂的途径。
这些研究人员推测,某些细胞通过分解接近它们的化疗吸引剂来进行导航。它们随后会感知化学吸引剂被补充的程度,最重要的是,在哪个方向进行补充。通过注意到新的化疗吸引剂的位置,它们就能向自己想要的目的地移动。举个例子,努力向伤口移动的白细胞在发现一个岔路口后,会选择分解了最多或最新的化学吸引剂的路径。
2.Science:详解先前的寨卡病毒感染可增加严重登革热病毒感染的风险
doi:10.1126/science.abb6143; doi:10.1126/science.abd5922
在一项新的研究中,来自美国和尼加拉瓜的研究人员发现感染蚊子传播的寨卡病毒会使人们以后更容易患上登革热病,而且当他们真地患上登革热病时,他们会遭受更严重的症状。相关研究结果发表在2020年8月28日的Science期刊上,论文标题为“Zika virus infection enhances future risk of severe dengue disease”。
这些研究结果证实了早先的猜测,即一些针对寨卡病毒的抗体,通常是为了保护身体免受感染,但实际上可能与登革热病毒相互作用,使得登革热病毒感染恶化。这种称为抗体依赖性增强作用(antibody-dependent enhancement)的相互作用,可能会使得人们更难设计出一种安全有效的在保护寨卡病毒的同时也不会增加登革热病毒感染风险的疫苗。
3.Science:重大进展!口服非核苷类STING激动剂MSA-2表现出显著的抗肿瘤活性
doi:10.1126/science.aba6098; doi:10.1126/science.abc6622
STING蛋白被它的天然配体---环鸟-腺二核苷酸(cyclic guanosine monophosphate-adenosine monophosphate, cGAMP)激活,引发信号转导反应,诱导I型干扰素和其他促炎细胞因子的释放。STING控制的干扰素产生参与抗病毒防御以及抗肿瘤免疫反应。利用药物激活STING被认为是一种很有前途的癌症治疗策略。
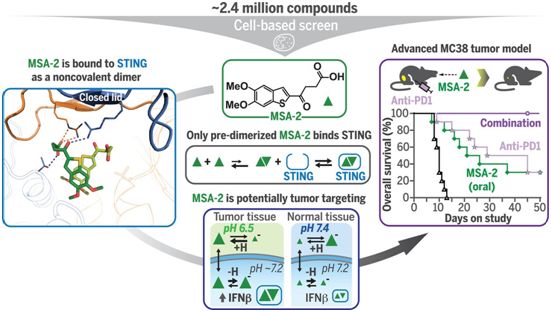
在一项新的研究中,来自美国默克公司的研究人员发现一种以前未知的化合物(MSA-2)可系统性给药,并通过它的独特作用机制优先靶向肿瘤。此外,MSA-2易于口服给药,由于方便和成本低,这是一种理想的给药途径。相关研究结果发表在2020年8月21的Science期刊上,论文标题为“An orally available non-nucleotide STING agonist with antitumor activity”。
4.Science:重大进展!小分子STING激活剂SR-717表现出显著的抗肿瘤活性
doi:10.1126/science.abb4255; doi:10.1126/science.abc6622
在一项新的研究中,来自美国斯克里普斯研究所的研究人员发现一种分子可以激活一种名为STING的免疫增强蛋白。这一发现标志着肿瘤学领域的一个关键进展,这是因为STING蛋白以其强大的抗肿瘤特性而闻名。相关研究结果发表在2020年8月21的Science期刊上,论文标题为“Antitumor activity of a systemic STING-activating non-nucleotide cGAMP mimetic”。
论文共同通讯作者、斯克里普斯研究所化学系副教授Luke Lairson博士说及其同事们发现,他们优化的STING激活剂(他们将它命名为SR-717)似乎以与其体内天然激活剂相同的方式激活STING蛋白。通过利用X射线衍射晶体分析法对原子尺度的相互作用进行成像,他们发现SR-717和一种已知的天然激活剂都与STING上的相同位点结合,并诱导这种蛋白发生相同的形状变化。
SR-717是一种非核苷类cGAMP模拟物。在侵袭性黑色素瘤的动物模型中,它能显著抑制肿瘤生长,阻止转移,诱导肿瘤分子呈现给免疫系统,并强力提升肿瘤周围CD8+ T细胞和NK细胞的水平---这两种细胞都是免疫系统中已知最强大的抗肿瘤武器之一。在有效剂量下,没有证据表明SR-717对动物有明显的不良副作用。
5.Science:重大进展!肠球菌噬菌体竟可增强癌症免疫治疗的疗效
doi:10.1126/science.aax0701
在一项新的研究中,来自法国、瑞典、中国、美国、加拿大、意大利、西班牙、丹麦、匈牙利和荷兰的研究人员发现一类称为肠球菌的肠道细菌携带着可调节免疫反应的噬菌体。噬菌体可整合到肠球菌的基因组中,称为原噬菌体(prophage)。他们报告了可能与肿瘤细胞相关抗原发生交叉反应的微生物抗原。相关研究结果发表在2020年8月21日的Science期刊上,论文标题为“Cross-reactivity between tumor MHC class I–restricted antigens and an enterococcal bacteriophage”。
进一步地,这些研究人员在海氏肠球菌(Enterococcus hirae)的原噬菌体(prophage)中鉴定出它的尾卷尺蛋白(TMP)存在着主要组织相容性复合体I类(MHC-I)结合表位:TSLARFANI(称为TMP1)。这种噬菌体TMP蛋白长1506个氨基酸,这个表位对应于它的氨基酸位点为187~197。携带含有原噬菌体的海氏肠球菌的小鼠在接受环磷酰胺或抗PD-1抗体免疫治疗时可产生TMP特异性的H-2Kb限制性CD8+ T淋巴细胞反应。给小鼠提供经过基因改造后表达这种TMP表位的细菌菌株可改善对它们的免疫治疗。
6.Science:揭示基因CIITA诱导人细胞抵抗埃博拉病毒和SARS样冠状病毒感染机制
doi:10.1126/science.abb3753
在一项新的研究中,来自美国弗吉尼亚梅森大学贝纳罗亚研究所、凯斯西储大学、波士顿大学医学院和MRIGlobal公司的研究人员发现了一种新的细胞保护途径,该途径靶向几种不同大流行病毒中的共同弱点。他们发现这种途径可以保护细胞免受埃博拉病毒和诸如SARS-CoV-2之类的冠状病毒感染。这些新发现使得人们更好地理解参与抵抗病毒感染的细胞机制,从而为治疗未来病毒性传染病提供参考。相关研究结果于2020年8月27日在线发表在Science期刊上,论文标题为“MHC class II transactivator CIITA induces cell resistance to Ebola virus and SARS-like coronaviruses”。
这项研究阐明了所发现的两个基因的全新作用,以及抑制病毒融合和进入人体细胞的独特方法,这使得我们离下一代抗病毒疗法更近了一步。这些研究人员利用转座子介导的基因激活筛选方法,寻找可以阻止埃博拉病毒感染的新基因。
这种新的筛选策略可作为发现针对其他危险病原体的抵抗机制的蓝本。利用这种策略,这些研究人员发现了基因CIITA(MHC class II transactivator,MHCII类反式激活蛋白)通过激活第二个基因CD74的表达,诱导人细胞系产生抵抗力。作为CD74的一种形式,p41破坏了称为组织蛋白酶(Cathepsin)的细胞蛋白酶对埃博拉病毒蛋白外壳上的蛋白的加工。这可以阻止这种病毒进入细胞和感染。p41还会阻断包括SARS-CoV-2在内的冠状病毒的组织蛋白酶依赖性进入途径。
7.Science:揭示富马酸盐阻断细胞焦亡机制
doi:10.1126/science.abb9818
在一项新的研究中,来自美国马萨诸塞大学、中国南京医科大学和南京中医药大学等研究机构的研究人员发现富马酸盐(fumarate,又称延胡索酸盐)是细胞焦亡的抑制剂。相关研究结果于2020年8月20日在线发表在Science期刊上,论文标题为“Succination inactivates gasdermin D and blocks pyroptosis”。他们发现递送到细胞中的富马酸二甲酯(dimethyl fumarate, DMF)或内源性富马酸盐在关键的半胱氨酸残基处与gasdermin D(GSDMD)反应,从而形成S-(2-琥珀酰)-半胱氨酸。GSDMD琥珀酰化(succination)阻止了它与caspase的相互作用,因而限制了它的加工、低聚化和诱导细胞死亡的能力。
在小鼠中,DMF给送通过靶向GSDMD,可保护它们免受脂多糖性休克(LPS shock),并减轻家族性地中海热(familial Mediterranean fever, FMF)和实验性自身免疫性脑炎(experimental autoimmune encephalitis, EAE)。
8.Science:线粒体或能促进大脑发育期间神经干细胞向神经元细胞的转变
doi:10.1126/science.aba9760
线粒体是能为机体每个细胞提供能量非常重要的小型细胞器,尤其是对于需要能量维持正常功能的大脑,近日,一项刊登在国际杂志Science上的研究报告中,来自Flanders生物技术研究所等机构的科学家们通过研究发现,线粒体或能在大脑发育期间调节关键的事件,即如何调节神经干细胞转变为神经细胞;线粒体会在这一精确的时期影响细胞的命运开关,人类这一关键时期的长度是小鼠的两倍,相关研究结果强调了线粒体的重要功能,其或有望帮助研究人员解释人类为何会在进化过程中发育出更大尺寸的大脑,以及线粒体的缺陷如何会诱发神经发育疾病的发生。
这项研究中,研究人员分析了在神经发生过程中线粒体的重塑是否以及如何与神经元的命运偶联,线粒体是一种高度动态化的细胞器,其能发生融合和分裂,因此研究者就想知道这些动态变化是否与多种干细胞的命运改变有关。研究者指出,干细胞分裂后不久,子代细胞中的会进行自我更新的线粒体就会发生融合,同时转变为神经元的子代细胞就会发生高水平的分裂。增加线粒体的分裂实际上会促进神经元细胞命运的分化,同时有丝分裂后线粒体的融合还会重新引导子代细胞走向自我更新的阶段。
因此,线粒体的动态变化对于转变成为神经元细胞非常重要,研究者Pierre Casimir说道,线粒体动态变化对细胞命运选择的影响或许会受限于特定的时间窗口,有意思的是,人类机体中受限制的时间窗口的长度是小鼠的两倍。此前研究重点分析了神经干细胞分裂之前的命运决策,本文研究结果表明,细胞命运能在一段较长的时间范围内被影响,即使是在神经干细胞分类后亦是如此;这或许对于当前细胞重编程研究领域具有重要的应用意义,即科学家们会尝试将非神经元细胞直接转换为用作治疗目的的神经元细胞。
9.Science:揭示蛋白酶体控制古生菌细胞分裂机制
doi:10.1126/science.aaz2532
真核生物很可能是由古生菌宿主和α-变形杆菌之间的共生伙伴关系产生的,后两者分别产生了细胞体和线粒体。正因为如此,一些控制真核细胞分裂周期中关键事件的蛋白都起源于古生菌。这其中包括ESCRT-III蛋白,它在许多真核生物中催化细胞分裂的最后一步,在古生菌嗜酸热硫化叶菌(Sulfolobus acidocaldarius)中也是如此。
然而,到目前为止,还没有发现任何一种古生菌有诸如周期蛋白依赖性激酶和周期蛋白之类的细胞周期调节因子的同源物,这些调节因子在所有真核生物中都能使得细胞周期事件有序进行。因此,古生菌细胞周期中的关键事件(包括细胞分裂)如何受到调控仍不清楚。
20S蛋白酶体是一个例外,它在古生菌和真核生物之间是保守的,它通过降解周期蛋白来调节真核生物的细胞周期。为了探究20S蛋白酶体在嗜酸热硫化叶菌中的功能,来自英国伦敦大学学院、剑桥大学、弗朗西斯-克里克研究所、兰卡斯特大学和瑞典斯德哥尔摩大学的研究人员在一项新的研究中,通过晶体学方法解析出它的三维结构,并且在体外在它受到抑制和没有受到抑制时,对它的活性进行了生化分析。相关研究结果发表在2020年8月7日的Science期刊上,论文标题为“The proteasome controls ESCRT-III–mediated cell division in an archaeon”。
10.Science:新方法可更快更廉价地合成治疗病毒感染和癌症的核苷类似物
doi:10.1126/science.abb3231; doi:10.1126/science.abd1283
在过去的50年里,科学家们利用人造的、合成的核苷类似物来开发药物,用于治疗涉及细胞分裂和/或受感染细胞中病毒增殖的疾病。这些疾病包括肝炎、单纯疱疹、HIV和癌症。但是,加拿大西蒙弗雷泽大学化学家Robert Britton教授说,“这个过程是密集的和具有挑战性的,限制和阻止了新药物疗法的发现。”
如今,在一项新的研究,Britton及其研究团队可以比以前的方法提前几个月构建出新的核苷类似物,这就为更快的药物发现铺平了道路。这也将使得人们更快更廉价地发现抗病毒药物和抗癌药物。相关研究结果发表在2020年8月7日的Science期刊上,论文标题为“A short de novo synthesis of nucleoside analogs”。
Britton教授说,“合成时间和成本的减少会有所不同,这取决于具体的核苷类似物,但是我们有例子表明,我们将一个20多个步骤的通常至少需要几个月才能完成的合成步骤减少到三四个步骤,这将只需要一周左右的时间。在治疗导致COVID-19疾病的新型冠状病毒SARS-CoV-2等新进化的病毒时,这显然是一个关键因素。”(生物谷 Bioon.com)
1.Science:新研究揭示细胞是走迷宫高手
doi:10.1126/science.aay9792
在一项新的研究中,来自英国多个研究机构的研究人员发现了细胞为何能够如此准确地在人体中迁移。相关研究结果发表在2020年8月28日的Science期刊上,论文标题为“Seeing around corners: Cells solve mazes and respond at a distance using attractant breakdown”。在这篇论文中,他们描述了他们开发的一种解释细胞定向运动(cell orienteering)的理论,以及他们如何使用迷宫对它进行测试。

图片来自Science, 2020, doi:10.1126/science.aay9792。
当身体受伤时,例如被针头戳伤,免疫系统的反应是派遣白细胞来杀死任何可能试图通过伤口进入体内的细菌。但是细胞通过什么方式找到伤口的呢?先前的研究已表明,细胞利用体内称为化学吸引剂(chemoattractant)的化学物来进行短距离导航。白细胞可以感知化学吸引剂并向它们移动---但是这仅在短距离内有效。在这项新的研究中,这些研究人员发现,细胞可以以不同的方式使用这样的化学吸引剂来导航更长和更复杂的途径。
这些研究人员推测,某些细胞通过分解接近它们的化疗吸引剂来进行导航。它们随后会感知化学吸引剂被补充的程度,最重要的是,在哪个方向进行补充。通过注意到新的化疗吸引剂的位置,它们就能向自己想要的目的地移动。举个例子,努力向伤口移动的白细胞在发现一个岔路口后,会选择分解了最多或最新的化学吸引剂的路径。
2.Science:详解先前的寨卡病毒感染可增加严重登革热病毒感染的风险
doi:10.1126/science.abb6143; doi:10.1126/science.abd5922
在一项新的研究中,来自美国和尼加拉瓜的研究人员发现感染蚊子传播的寨卡病毒会使人们以后更容易患上登革热病,而且当他们真地患上登革热病时,他们会遭受更严重的症状。相关研究结果发表在2020年8月28日的Science期刊上,论文标题为“Zika virus infection enhances future risk of severe dengue disease”。
这些研究结果证实了早先的猜测,即一些针对寨卡病毒的抗体,通常是为了保护身体免受感染,但实际上可能与登革热病毒相互作用,使得登革热病毒感染恶化。这种称为抗体依赖性增强作用(antibody-dependent enhancement)的相互作用,可能会使得人们更难设计出一种安全有效的在保护寨卡病毒的同时也不会增加登革热病毒感染风险的疫苗。
3.Science:重大进展!口服非核苷类STING激动剂MSA-2表现出显著的抗肿瘤活性
doi:10.1126/science.aba6098; doi:10.1126/science.abc6622
STING蛋白被它的天然配体---环鸟-腺二核苷酸(cyclic guanosine monophosphate-adenosine monophosphate, cGAMP)激活,引发信号转导反应,诱导I型干扰素和其他促炎细胞因子的释放。STING控制的干扰素产生参与抗病毒防御以及抗肿瘤免疫反应。利用药物激活STING被认为是一种很有前途的癌症治疗策略。

STING激动剂MSA-2,图片来自Science, 2020, doi:10.1126/science.aba6098。
在一项新的研究中,来自美国默克公司的研究人员发现一种以前未知的化合物(MSA-2)可系统性给药,并通过它的独特作用机制优先靶向肿瘤。此外,MSA-2易于口服给药,由于方便和成本低,这是一种理想的给药途径。相关研究结果发表在2020年8月21的Science期刊上,论文标题为“An orally available non-nucleotide STING agonist with antitumor activity”。
4.Science:重大进展!小分子STING激活剂SR-717表现出显著的抗肿瘤活性
doi:10.1126/science.abb4255; doi:10.1126/science.abc6622
在一项新的研究中,来自美国斯克里普斯研究所的研究人员发现一种分子可以激活一种名为STING的免疫增强蛋白。这一发现标志着肿瘤学领域的一个关键进展,这是因为STING蛋白以其强大的抗肿瘤特性而闻名。相关研究结果发表在2020年8月21的Science期刊上,论文标题为“Antitumor activity of a systemic STING-activating non-nucleotide cGAMP mimetic”。
论文共同通讯作者、斯克里普斯研究所化学系副教授Luke Lairson博士说及其同事们发现,他们优化的STING激活剂(他们将它命名为SR-717)似乎以与其体内天然激活剂相同的方式激活STING蛋白。通过利用X射线衍射晶体分析法对原子尺度的相互作用进行成像,他们发现SR-717和一种已知的天然激活剂都与STING上的相同位点结合,并诱导这种蛋白发生相同的形状变化。
SR-717是一种非核苷类cGAMP模拟物。在侵袭性黑色素瘤的动物模型中,它能显著抑制肿瘤生长,阻止转移,诱导肿瘤分子呈现给免疫系统,并强力提升肿瘤周围CD8+ T细胞和NK细胞的水平---这两种细胞都是免疫系统中已知最强大的抗肿瘤武器之一。在有效剂量下,没有证据表明SR-717对动物有明显的不良副作用。
5.Science:重大进展!肠球菌噬菌体竟可增强癌症免疫治疗的疗效
doi:10.1126/science.aax0701
在一项新的研究中,来自法国、瑞典、中国、美国、加拿大、意大利、西班牙、丹麦、匈牙利和荷兰的研究人员发现一类称为肠球菌的肠道细菌携带着可调节免疫反应的噬菌体。噬菌体可整合到肠球菌的基因组中,称为原噬菌体(prophage)。他们报告了可能与肿瘤细胞相关抗原发生交叉反应的微生物抗原。相关研究结果发表在2020年8月21日的Science期刊上,论文标题为“Cross-reactivity between tumor MHC class I–restricted antigens and an enterococcal bacteriophage”。
进一步地,这些研究人员在海氏肠球菌(Enterococcus hirae)的原噬菌体(prophage)中鉴定出它的尾卷尺蛋白(TMP)存在着主要组织相容性复合体I类(MHC-I)结合表位:TSLARFANI(称为TMP1)。这种噬菌体TMP蛋白长1506个氨基酸,这个表位对应于它的氨基酸位点为187~197。携带含有原噬菌体的海氏肠球菌的小鼠在接受环磷酰胺或抗PD-1抗体免疫治疗时可产生TMP特异性的H-2Kb限制性CD8+ T淋巴细胞反应。给小鼠提供经过基因改造后表达这种TMP表位的细菌菌株可改善对它们的免疫治疗。
6.Science:揭示基因CIITA诱导人细胞抵抗埃博拉病毒和SARS样冠状病毒感染机制
doi:10.1126/science.abb3753
在一项新的研究中,来自美国弗吉尼亚梅森大学贝纳罗亚研究所、凯斯西储大学、波士顿大学医学院和MRIGlobal公司的研究人员发现了一种新的细胞保护途径,该途径靶向几种不同大流行病毒中的共同弱点。他们发现这种途径可以保护细胞免受埃博拉病毒和诸如SARS-CoV-2之类的冠状病毒感染。这些新发现使得人们更好地理解参与抵抗病毒感染的细胞机制,从而为治疗未来病毒性传染病提供参考。相关研究结果于2020年8月27日在线发表在Science期刊上,论文标题为“MHC class II transactivator CIITA induces cell resistance to Ebola virus and SARS-like coronaviruses”。

图片来自Unsplash/CC0 Public Domain。
这项研究阐明了所发现的两个基因的全新作用,以及抑制病毒融合和进入人体细胞的独特方法,这使得我们离下一代抗病毒疗法更近了一步。这些研究人员利用转座子介导的基因激活筛选方法,寻找可以阻止埃博拉病毒感染的新基因。
这种新的筛选策略可作为发现针对其他危险病原体的抵抗机制的蓝本。利用这种策略,这些研究人员发现了基因CIITA(MHC class II transactivator,MHCII类反式激活蛋白)通过激活第二个基因CD74的表达,诱导人细胞系产生抵抗力。作为CD74的一种形式,p41破坏了称为组织蛋白酶(Cathepsin)的细胞蛋白酶对埃博拉病毒蛋白外壳上的蛋白的加工。这可以阻止这种病毒进入细胞和感染。p41还会阻断包括SARS-CoV-2在内的冠状病毒的组织蛋白酶依赖性进入途径。
7.Science:揭示富马酸盐阻断细胞焦亡机制
doi:10.1126/science.abb9818
在一项新的研究中,来自美国马萨诸塞大学、中国南京医科大学和南京中医药大学等研究机构的研究人员发现富马酸盐(fumarate,又称延胡索酸盐)是细胞焦亡的抑制剂。相关研究结果于2020年8月20日在线发表在Science期刊上,论文标题为“Succination inactivates gasdermin D and blocks pyroptosis”。他们发现递送到细胞中的富马酸二甲酯(dimethyl fumarate, DMF)或内源性富马酸盐在关键的半胱氨酸残基处与gasdermin D(GSDMD)反应,从而形成S-(2-琥珀酰)-半胱氨酸。GSDMD琥珀酰化(succination)阻止了它与caspase的相互作用,因而限制了它的加工、低聚化和诱导细胞死亡的能力。
在小鼠中,DMF给送通过靶向GSDMD,可保护它们免受脂多糖性休克(LPS shock),并减轻家族性地中海热(familial Mediterranean fever, FMF)和实验性自身免疫性脑炎(experimental autoimmune encephalitis, EAE)。
8.Science:线粒体或能促进大脑发育期间神经干细胞向神经元细胞的转变
doi:10.1126/science.aba9760
线粒体是能为机体每个细胞提供能量非常重要的小型细胞器,尤其是对于需要能量维持正常功能的大脑,近日,一项刊登在国际杂志Science上的研究报告中,来自Flanders生物技术研究所等机构的科学家们通过研究发现,线粒体或能在大脑发育期间调节关键的事件,即如何调节神经干细胞转变为神经细胞;线粒体会在这一精确的时期影响细胞的命运开关,人类这一关键时期的长度是小鼠的两倍,相关研究结果强调了线粒体的重要功能,其或有望帮助研究人员解释人类为何会在进化过程中发育出更大尺寸的大脑,以及线粒体的缺陷如何会诱发神经发育疾病的发生。
这项研究中,研究人员分析了在神经发生过程中线粒体的重塑是否以及如何与神经元的命运偶联,线粒体是一种高度动态化的细胞器,其能发生融合和分裂,因此研究者就想知道这些动态变化是否与多种干细胞的命运改变有关。研究者指出,干细胞分裂后不久,子代细胞中的会进行自我更新的线粒体就会发生融合,同时转变为神经元的子代细胞就会发生高水平的分裂。增加线粒体的分裂实际上会促进神经元细胞命运的分化,同时有丝分裂后线粒体的融合还会重新引导子代细胞走向自我更新的阶段。
因此,线粒体的动态变化对于转变成为神经元细胞非常重要,研究者Pierre Casimir说道,线粒体动态变化对细胞命运选择的影响或许会受限于特定的时间窗口,有意思的是,人类机体中受限制的时间窗口的长度是小鼠的两倍。此前研究重点分析了神经干细胞分裂之前的命运决策,本文研究结果表明,细胞命运能在一段较长的时间范围内被影响,即使是在神经干细胞分类后亦是如此;这或许对于当前细胞重编程研究领域具有重要的应用意义,即科学家们会尝试将非神经元细胞直接转换为用作治疗目的的神经元细胞。
9.Science:揭示蛋白酶体控制古生菌细胞分裂机制
doi:10.1126/science.aaz2532
真核生物很可能是由古生菌宿主和α-变形杆菌之间的共生伙伴关系产生的,后两者分别产生了细胞体和线粒体。正因为如此,一些控制真核细胞分裂周期中关键事件的蛋白都起源于古生菌。这其中包括ESCRT-III蛋白,它在许多真核生物中催化细胞分裂的最后一步,在古生菌嗜酸热硫化叶菌(Sulfolobus acidocaldarius)中也是如此。
然而,到目前为止,还没有发现任何一种古生菌有诸如周期蛋白依赖性激酶和周期蛋白之类的细胞周期调节因子的同源物,这些调节因子在所有真核生物中都能使得细胞周期事件有序进行。因此,古生菌细胞周期中的关键事件(包括细胞分裂)如何受到调控仍不清楚。

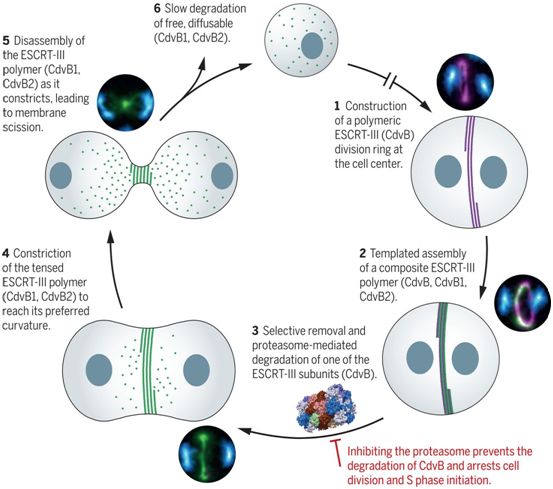
图片来自Science, 2020, doi:10.1126/science.aaz2532。
20S蛋白酶体是一个例外,它在古生菌和真核生物之间是保守的,它通过降解周期蛋白来调节真核生物的细胞周期。为了探究20S蛋白酶体在嗜酸热硫化叶菌中的功能,来自英国伦敦大学学院、剑桥大学、弗朗西斯-克里克研究所、兰卡斯特大学和瑞典斯德哥尔摩大学的研究人员在一项新的研究中,通过晶体学方法解析出它的三维结构,并且在体外在它受到抑制和没有受到抑制时,对它的活性进行了生化分析。相关研究结果发表在2020年8月7日的Science期刊上,论文标题为“The proteasome controls ESCRT-III–mediated cell division in an archaeon”。
10.Science:新方法可更快更廉价地合成治疗病毒感染和癌症的核苷类似物
doi:10.1126/science.abb3231; doi:10.1126/science.abd1283
在过去的50年里,科学家们利用人造的、合成的核苷类似物来开发药物,用于治疗涉及细胞分裂和/或受感染细胞中病毒增殖的疾病。这些疾病包括肝炎、单纯疱疹、HIV和癌症。但是,加拿大西蒙弗雷泽大学化学家Robert Britton教授说,“这个过程是密集的和具有挑战性的,限制和阻止了新药物疗法的发现。”
如今,在一项新的研究,Britton及其研究团队可以比以前的方法提前几个月构建出新的核苷类似物,这就为更快的药物发现铺平了道路。这也将使得人们更快更廉价地发现抗病毒药物和抗癌药物。相关研究结果发表在2020年8月7日的Science期刊上,论文标题为“A short de novo synthesis of nucleoside analogs”。
Britton教授说,“合成时间和成本的减少会有所不同,这取决于具体的核苷类似物,但是我们有例子表明,我们将一个20多个步骤的通常至少需要几个月才能完成的合成步骤减少到三四个步骤,这将只需要一周左右的时间。在治疗导致COVID-19疾病的新型冠状病毒SARS-CoV-2等新进化的病毒时,这显然是一个关键因素。”(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


