你知道吗?全球约有超过1000万人正在与被称为 “缓慢的时光小偷” 的帕金森病作斗争,这一数字较 1990 年增长了 274%。在中国,65 岁以上老年人的帕金森病患病率约为 1.7%,患者总数已超 300 万,且随着人口老龄化加剧,这一数据仍在持续攀升。
然而,现有的主流药物如左旋多巴,虽能暂时缓解颤抖、僵硬等症状,却无法阻止疾病的持续进展,长期使用还可能引发运动障碍、精神紊乱等并发症,约 34% 的患者会在四年后因无法耐受副作用而停药。面对这一困境,科学家们正在寻找一种既能 “治标” 又能 “治本” 的全新策略。
最近,发表在《Chinese Neurosurgical Journal》杂志上题为 “Synergy between stem cell therapy and brain-derived neurotrophic factor (BDNF) in Parkinson’s disease: a mini-review of combined neuroregenerative strategies” 的综述报告,为我们描绘了一幅充满希望的未来图景:将干细胞疗法与脑源性神经营养因子(BDNF)增强策略相结合,有望同时实现症状缓解与疾病修饰,为帕金森病的治疗带来革命性突破。

为什么传统疗法“力不从心”?
帕金森病的核心问题,在于大脑黑质致密部(SNpc)生产多巴胺的神经元逐渐凋亡,同时伴随 α- 突触核蛋白异常沉积。你可以把多巴胺想象成大脑内部的 “信号快递员”,它的减少直接导致运动指令传递失灵,从而出现手抖、动作迟缓、肌肉僵硬等症状。
左旋多巴作为多巴胺的 “前体”,能临时补充 “快递员” 数量,缓解症状,但它无法阻止神经元继续死亡,也无法修复已经受损的神经网络——这就好比给一个不断漏水的池子加水,而非修补漏洞。此外,多巴胺激动剂可能引发恶心、嗜睡等副作用,深部脑刺激等手术疗法虽有效,但费用高昂且伴随感染、出血等风险。因此,医学界迫切需要一种能从根源上保护神经元、替代丢失神经元、并修复神经回路的全新疗法。
强强联合
这篇综述聚焦的联合策略,巧妙地将两种前沿思路合二为一,实现 “1+1>2” 的协同效应。
一方面是干细胞负责 “种树”:干细胞,尤其是诱导多能干细胞(iPSCs)、胚胎干细胞(ESCs)和间充质干细胞(MSCs),拥有分化成各类细胞的潜力,就像一批 “预备役神经元”。移植到大脑后,它们能在 Nurr1、Pitx3、Lmx1a 等转录因子的调控下,定向分化成新的多巴胺能神经元,直接补充损失的细胞,替代左旋多巴的 “临时工” 角色,实现更根本的功能重建。临床前研究和早期临床试验已证实,这些分化后的神经元能成功整合到宿主神经回路,稳定分泌多巴胺。
另一方面是 BDNF 负责 “施肥”:BDNF 是一种对神经元生长、存活和功能至关重要的蛋白质,堪称神经细胞的 “超级营养液” 和 “生存信号”。它能与神经元表面的 TrkB 受体结合,激活 PI3K/Akt、MAPK/ERK、PLC-γ 等下游通路,这些通路就像 “保护开关”,既能抑制神经元凋亡、增强突触可塑性,又能调节神经炎症,为神经元提供良好的生存环境。更重要的是,BDNF 还能保护黑质区域的 γ- 氨基丁酸能神经元,减少兴奋性毒性损伤,这是单一干细胞疗法难以实现的。
然而,两者单独使用都有局限:干细胞移植后存活率和定向分化效率有待提高,且容易受到脑内炎症环境的影响;而 BDNF 本身分子量大,难以穿过血脑屏障,全身给药不仅效果不佳,还容易产生副作用。
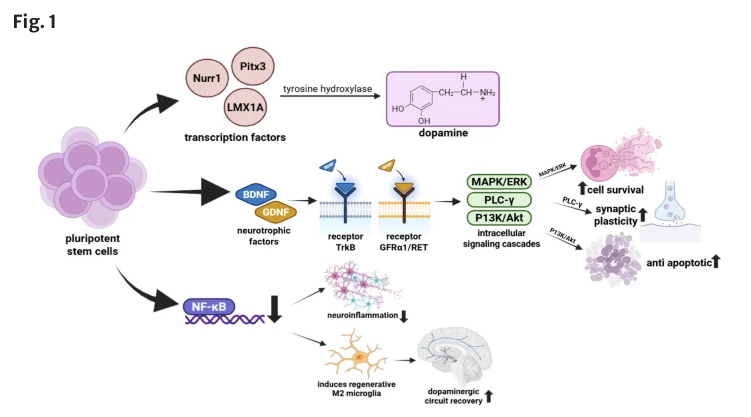
干细胞与脑源性神经营养因子的作用机制
“工程化细胞工厂” 的智能解决方案
研究的精华在于提出了一个智能方案:对干细胞进行基因改造,让它们变成可持续分泌 BDNF 的 “微型生物工厂”。经过改造的干细胞,移植后能发挥三重作用:
首先,BDNF 能促进自身更高效、更稳定地分化成多巴胺能神经元,提高移植成功率;
其次,它们持续分泌的 BDNF 会像 “甘霖” 一样,滋润周围残存的原生神经元和新生细胞,抑制凋亡、增强神经连接,形成一片健康的 “神经森林”;
最后,这种联合策略还能通过抑制 NF-κB 信号通路,减少促炎细胞因子释放,让小胶质细胞向抗炎的 M2 表型转化,为神经修复创造友好环境。
在帕金森病动物模型中,这一策略取得了鼓舞人心的成果:大脑内多巴胺水平显著回升,动物的旋转行为减少、运动功能得到实质性改善,且效果持续时间远超单一疗法。这标志着治疗不仅缓解了表面症状,更触达了疾病的核心病理环节。
从实验室到病床前,还有几步?
研究者 Jonny 博士表示,如果这种双重治疗策略成功转化,它将彻底改变帕金森病的治疗模式,实现长期症状缓解甚至改变疾病进程。当然,从美好的蓝图到普惠患者的疗法,仍有挑战需要攻克:如何通过 CRISPR/Cas9 等基因编辑工具,将 BDNF 精准插入干细胞的安全位点,避免插入突变风险;如何通过四环素响应启动子(Tet-On/Tet-Off)等诱导系统,精准调控 BDNF 的分泌量,防止过量引发兴奋性毒性;如何优化递送方式,确保干细胞精准定植于黑质 - 纹状体通路,提高整合效率;如何建立长期安全监控机制,通过 “自杀基因”(如 HSV-tk)等设计,应对可能的异常增殖。
尽管如此,随着细胞工程、递送技术和基因编辑工具的不断进步,这条 “干细胞搭载 BDNF” 的联合治疗之路正变得越来越清晰。Phase I/II 临床试验已证实,iPSC 来源的多巴胺能祖细胞移植后无致瘤性,且能有效改善患者运动功能;BDNF 修饰的间充质干细胞也在动物实验中展现出良好的安全性和有效性。它代表的不仅是一种新疗法,更是一种治疗理念的跃升——从被动缓解症状,转向主动修复与保护。
对于数百万帕金森病患者及其家庭而言,这意味着未来或许不再仅仅是与症状的漫长拉锯,而是一场有望逆转战局的修复之旅。科学的探索从未止步,而这束由 “再生” 与 “神经营养” 交汇而成的光芒,正照亮着通往更自由、更有质量生活的道路。或许不久的将来,这种联合疗法将走进临床,让帕金森病患者摆脱药物依赖,重新找回流畅的动作与生活的尊严。(生物谷Bioon.com)
参考文献:
Jonny, J., Larasati, A.D., Sunjaya, Q.A. et al. Synergy between stem cell therapy and brain-derived neurotrophic factor (BDNF) in Parkinson’s disease: a mini-review of combined neuroregenerative strategies. Chin Neurosurg Jl 11, 29 (2025).doi:10.1186/s41016-025-00415-5
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。




