《自然·癌症》:中国乳腺癌多组学研究重要成果发布!
来源:奇点糕 2024-02-21 10:22
该研究显示,与欧美乳腺癌患者相比,我国乳腺癌患者AKT1突变频率更高,更有可能从在研的AKT抑制剂治疗中获益。
近日,复旦大学附属肿瘤医院邵志敏、江一舟团队,复旦大学生命科学学院郑媛婷团队与上海市生物医药技术研究院黄薇团队就在《自然·癌症》期刊共同发表了对中国乳腺癌患者的综合多组学研究成果,对我国临床实践将有重要指导价值!
该研究显示,与欧美乳腺癌患者相比,我国乳腺癌患者AKT1突变频率更高,更有可能从在研的AKT抑制剂治疗中获益;同时,我国患者的HER2富集亚型比例更高,与既往临床研究中亚裔患者对抗HER2靶向治疗应答较好相吻合;而分型为基底样型(BLBC)的患者肿瘤脂质过氧化水平及铁死亡相关蛋白表达量更高,靶向铁死亡有望成为精准治疗新策略。

论文首页截图
此次研究基于复旦大学附属肿瘤医院2013-14年间收治的773例乳腺癌患者,即中国乳腺癌基因组图谱(CBCGA)队列进行,患者中位随访时间已接近7年(83.1个月),涵盖了全国范围、不同亚型的乳腺癌患者,多组学分析的维度则包括肿瘤基因组学(全外显子组测序、RNA测序)、转录组学、蛋白质组学、代谢组学、放射组学和数字病理学特征。
在完成上述分析后,研究者们首先对照了CBCGA患者队列和癌症基因组图谱计划(TCGA)白人乳腺癌患者的分子特征差异,发现我国患者的AKT1突变频率显著更高(6.4% vs. 2.5%, 伪发现率/FDR=0.032),且主要集中在Luminal A型患者(12.1% vs. 4.4%,FDR=0.025),突变类型绝大多数(90.9%)为E17K突变,可被现有AKT抑制剂(如capivasertib)针对。
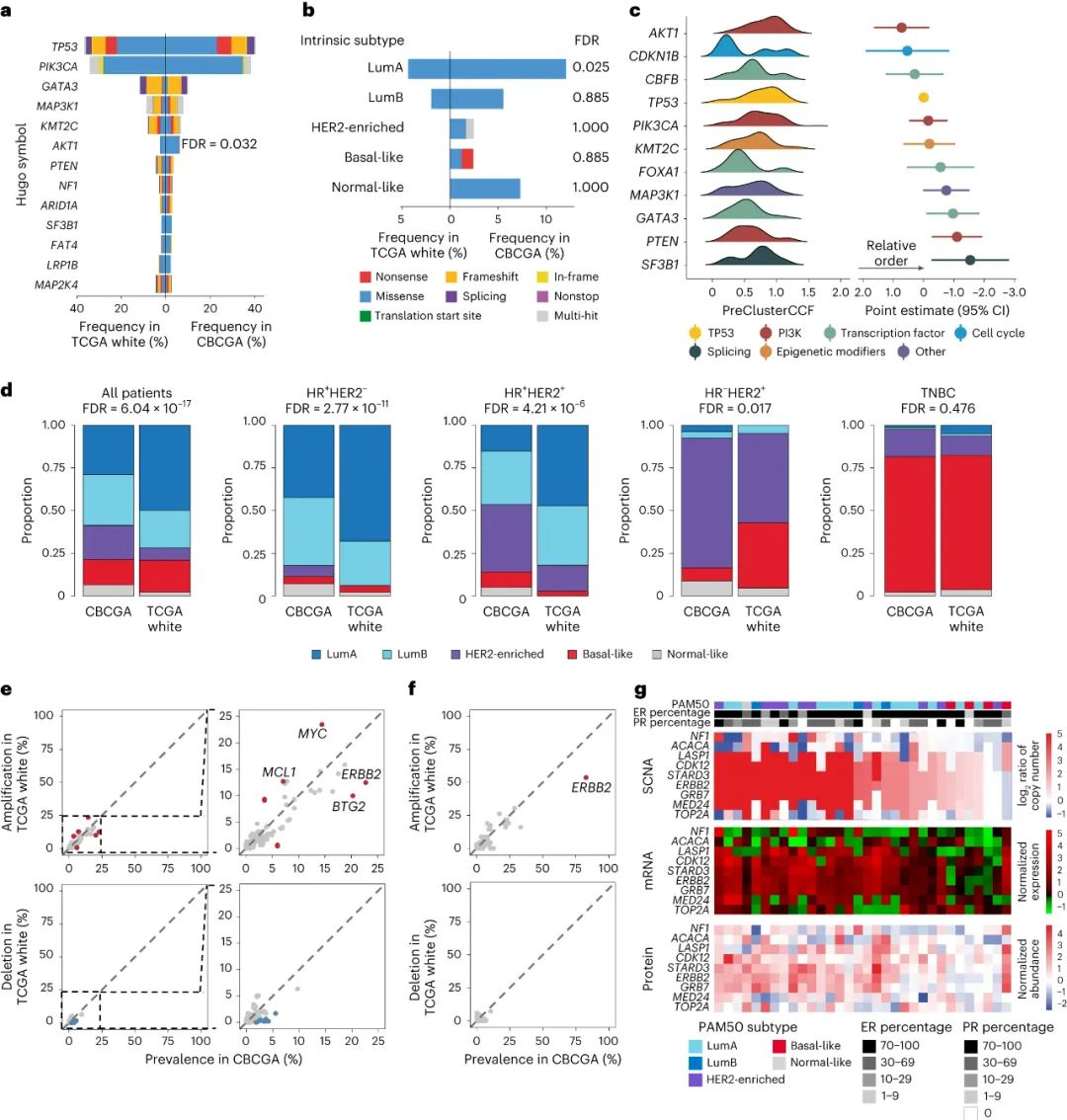
CBCGA患者队列与TCGA队列的分子特征差异对比
而按照乳腺癌分子分型的整体占比来看,CBCGA患者队列中的Luminal A型相对偏少(29.1% vs. 49.8%),HER2富集型偏多(20.0% vs. 7.1%),且HER2富集型中有约4成是激素受体阳性/HER2阳性型(HR+/HER2+),这可能解释了既往全球性临床研究中,亚裔患者对HER2靶向治疗应答更佳;如果患者存在HER2融合变异(研究共检出61个融合转录本),生存预后还会更好。
接下来通过蛋白组学分析和基因拷贝数变异(CNAs)分析,研究者们找到了又一种将乳腺癌患者分为4类亚型的分型方法,其中1型肿瘤存在明显的上皮-间质转化(EMT)基因特征,2型以雌激素通路激活为特征,3型为免疫激活型但患者既往预后不佳(HR+/HER2-患者尤为明显),可能需要提早使用免疫治疗,而4型则为快速增殖型。
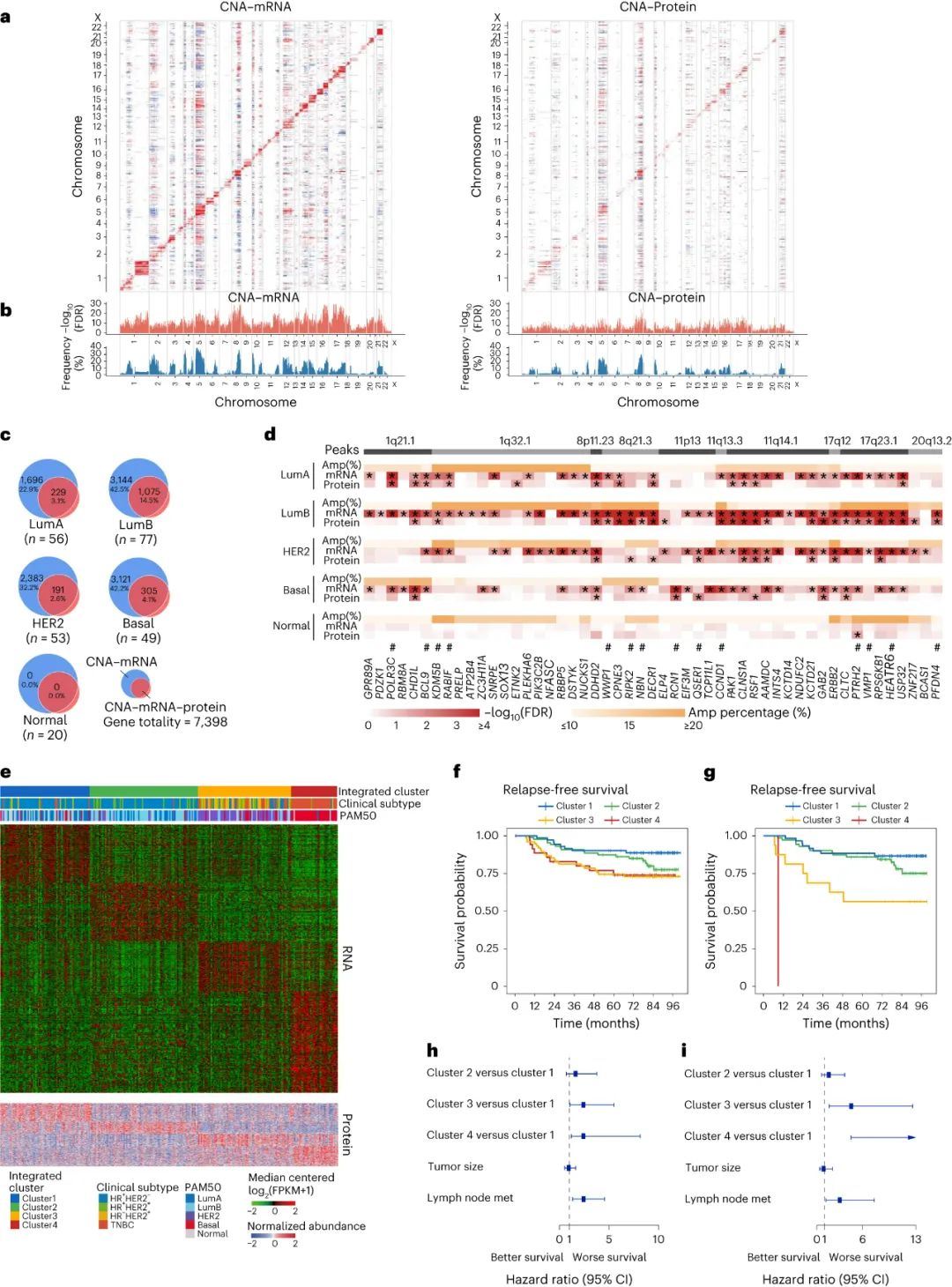
蛋白组学分析和CNAs分析提出的乳腺癌分型与患者预后有关
代谢组学分析则显示,不同亚型乳腺癌较正常乳腺组织的代谢失调也各有特点,例如基底样型乳腺癌中存在氧化磷脂的显著富集,研究团队就以此为线索,发现此类肿瘤中多个铁死亡关键蛋白(如ACSL4、TFRC)表达显著上调,对外界因素诱导的铁死亡更敏感,为将来的针对性精准治疗提供了可能性。
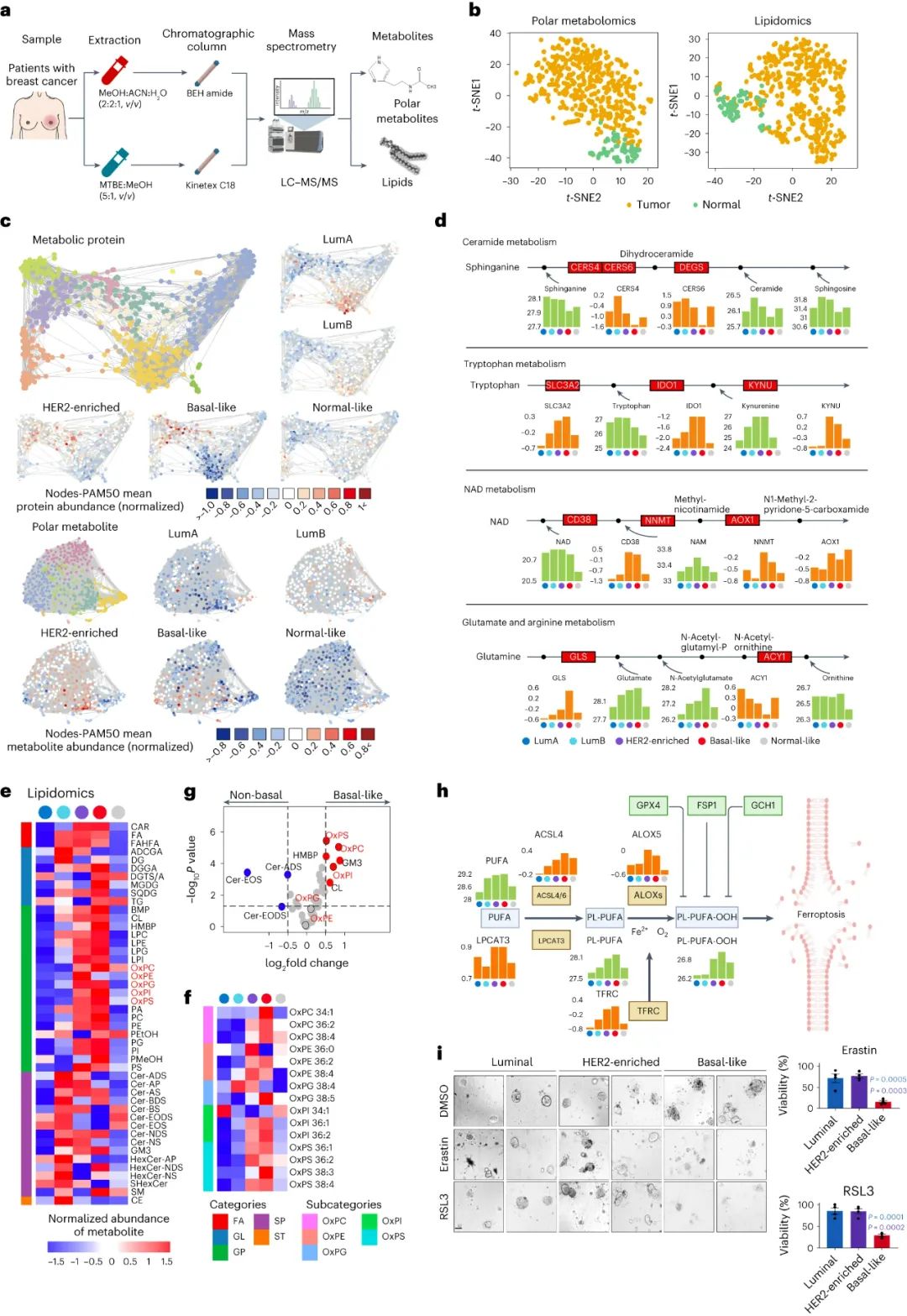
代谢组学分析提供的精准治疗线索
在免疫微环境方面,此次研究将乳腺癌免疫微环境分为了冷、中间、热三类,基底样型乳腺癌和HER2富集型过半都属于免疫热肿瘤,而Luminal型(A/B型)整体偏冷,但也有31.5%的Luminal B型肿瘤被定为热型;不同的免疫微环境不仅与适应性免疫有关,还与奇点糕们最近提到的固有免疫激活状态,例如“病毒模拟”等现象有关。
最后,基于本次研究获取的多组学特征和其它临床特征,研究者们基于机器学习构建了可预测我国乳腺癌患者复发风险的多模态风险分层模型,称为TMPIC模型,纳入因素包括:融合转录组(T)、代谢组(M)、数字病理(P)特征、免疫组化分型(I)和临床分期(C),在测试队列中的C指数(C-Index)达到0.78,提示了良好的预测效能。
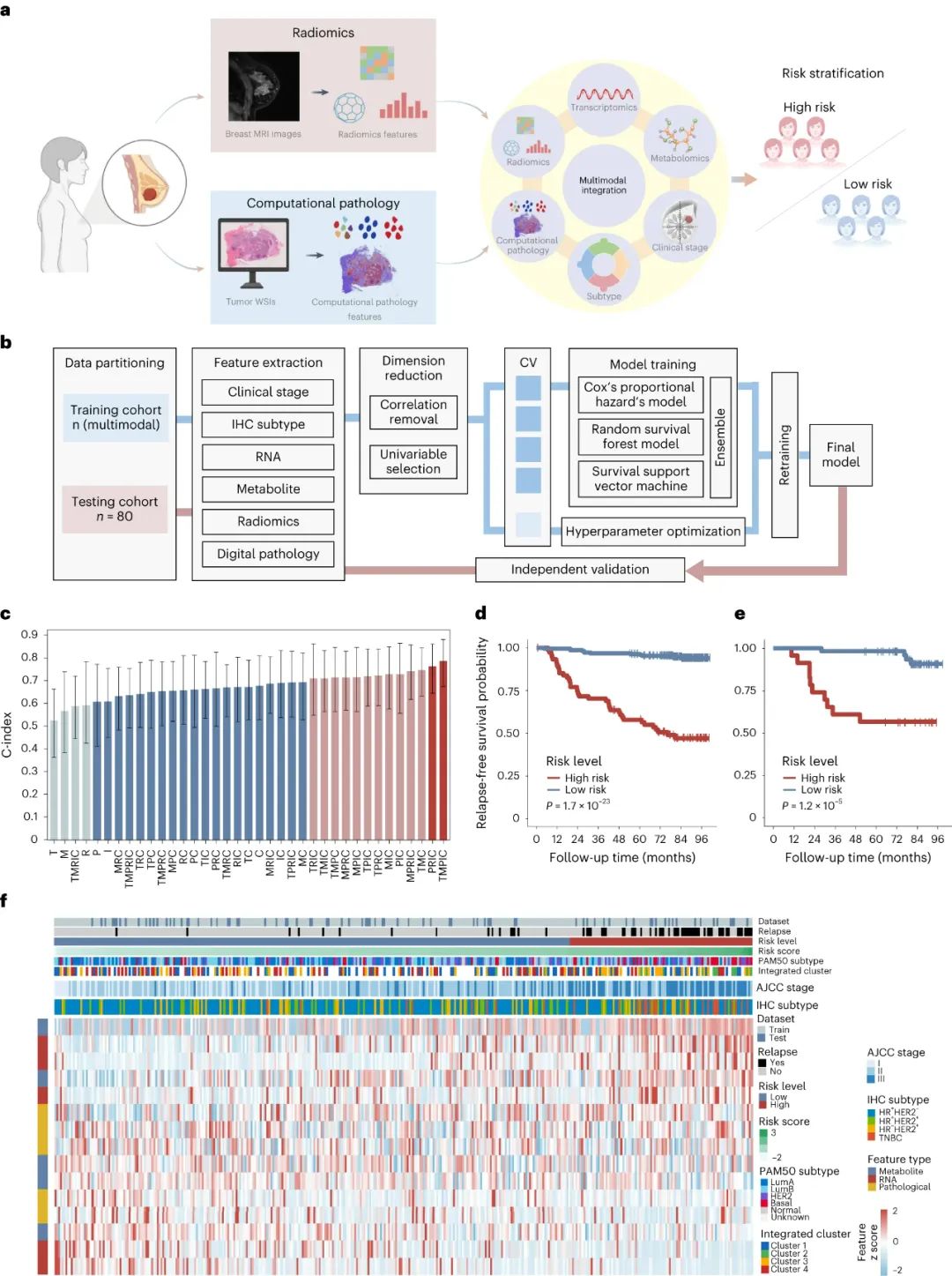
TMPIC模型的构建过程和在测试队列中的表现
相信在未来,CBCGA队列还可能为我国乳腺癌的精准治疗提供更多重要信息,奇点糕也期待同类研究能够覆盖到更多我国常见癌种,帮助中国医生和患者找到制胜之道~
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


