Cell Death Differ:结直肠癌治疗新突破!阻断HSF1-HSP90轴,激活p53或抑制CDK4/6助力抗癌
来源:生物谷原创 2025-05-09 10:39
本研究发现,p53激活剂或CDK4/6抑制剂与HSP90抑制剂联合使用,可阻断HSF1-HSR轴,协同抑制结直肠癌细胞生长、抑制肿瘤进展,为结直肠癌治疗提供新策略。
在全球范围内,癌症始终是威胁人类健康的重大疾病。其中,结直肠癌(CRC)在工业化国家的癌症相关死亡原因中位居第二,每年近100万人因此离世,新发病例和死亡人数占比可观,晚期患者5年生存率仅约15%。寻找更有效的治疗策略,成为医学领域亟待攻克的难题。
近期,一项发表于Cell Death Differ的研究Enhancement of colorectal cancer therapy through interruption of the HSF1-HSP90 axis by p53 activation or cell cycle inhibition,为结直肠癌治疗带来了新的希望。该研究聚焦于热休克蛋白90(HSP90)抑制剂在癌症治疗中的应用,虽然这类抑制剂在肿瘤治疗方面展现出高选择性,在小鼠实验中也能有效抑制肿瘤生长,但在临床试验中却屡屡受挫。主要原因在于,HSP90抑制剂会干扰热休克反应(HSR)中的负调节反馈回路,导致热休克因子1(HSF1)被激活,进而补偿性地合成应激诱导伴侣蛋白,稳定致癌蛋白,削弱治疗效果。

研究团队发现,野生型p53可通过p21-CDK4/6-MAPK-HSF1轴抑制HSF1,降低HSR活性。基于此,他们提出假设:在基于HSP90的治疗中,同时激活p53或直接抑制细胞周期,能否阻断有害的HSF1-HSR轴,提高HSP90抑制剂的疗效?
研究结果令人振奋。临床相关的p53激活剂Idasanutlin(RG-7388)与HSP90抑制剂Ganetespib联合使用时,在p53功能正常的结直肠癌细胞、小鼠肿瘤来源的类器官以及患者来源的类器官(PDOs)中,展现出显著的协同作用。联合治疗不仅显著降低细胞活力、加速细胞死亡,还能有效抑制HSF1-HSR活性,使HSF1靶基因表达下调,经典HSP90客户蛋白(如AKT和cRAF)更易降解。同时,p53相关通路、细胞凋亡和炎症通路显著上调。
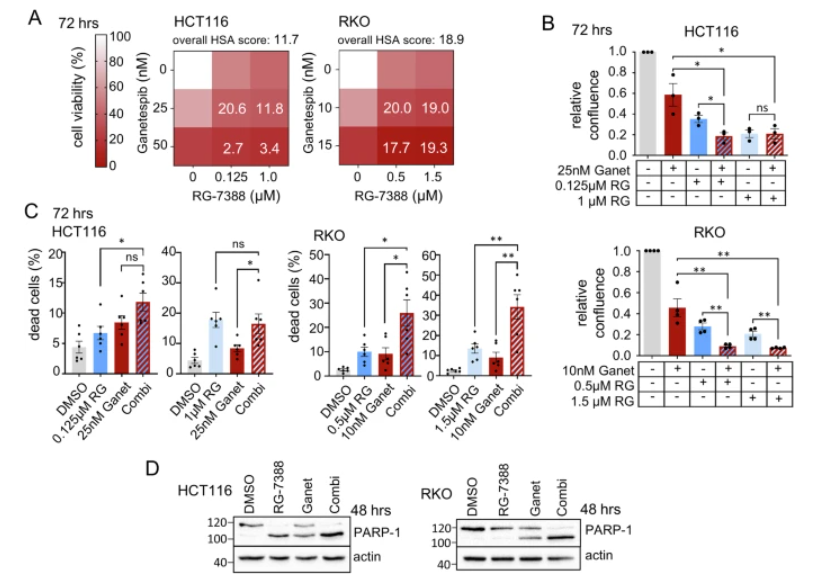
图 1:通过激活p53双抑制HSF1-HSP90协同抑制结直肠癌细胞生长
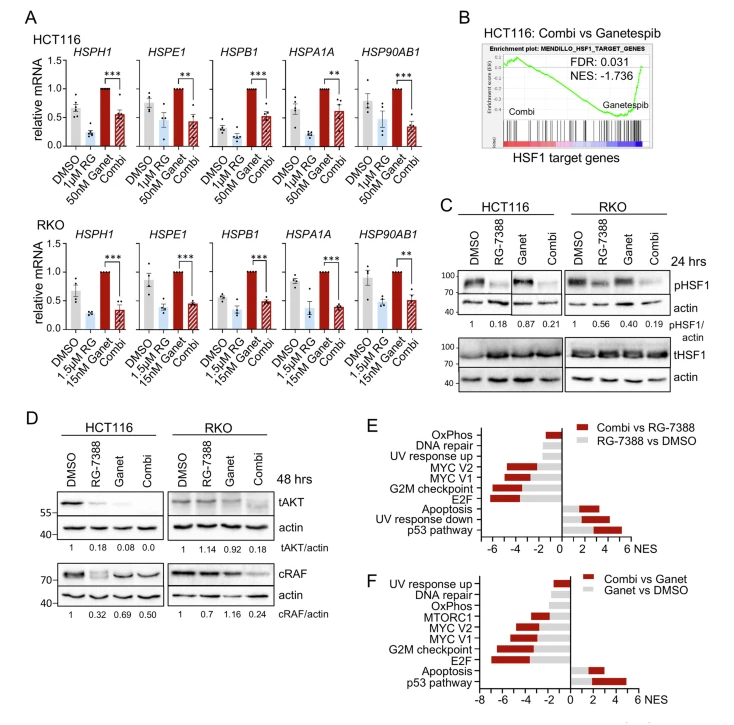
图 2:通过激活p53双抑制HSF1-HSP90消除HSF1介导的HSR并使HSP90客户蛋白不稳定
在小鼠模型实验中,这种联合治疗同样表现出色。它能显著抑制结肠肿瘤的生长,使肿瘤大小和数量明显减少,且未引起小鼠体重下降,表明其具有良好的耐受性。进一步研究发现,联合治疗会导致肿瘤组织中免疫细胞组成发生重塑,炎症通路被激活,肿瘤内中性粒细胞数量减少,免疫激活增强。
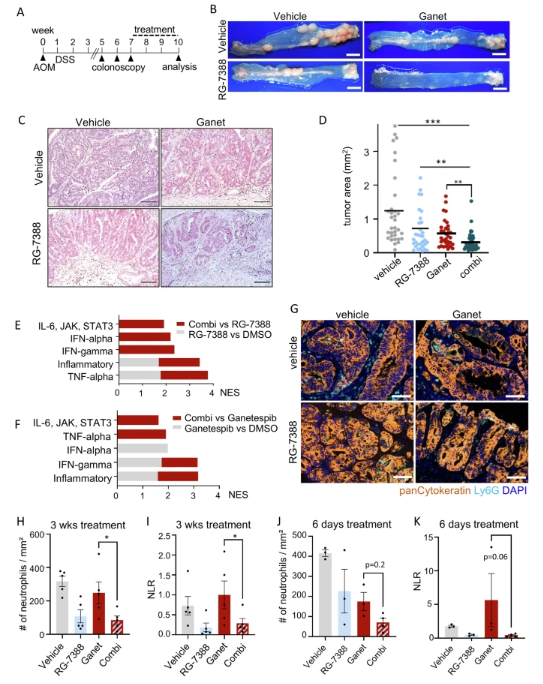
图 3:双抑制HSF1-HSP90通路通过重塑免疫系统减少小鼠模型中结肠肿瘤的进展
对于p53缺陷的结直肠癌细胞,研究也找到了有效的治疗策略。CDK4/6抑制剂Palbociclib与HSP90抑制剂联合使用时,在p53缺陷的细胞系、小鼠类器官以及患者来源的类器官中,同样能够抑制HSF1-HSR,降低癌细胞活力,减少肿瘤生长。这意味着,无论结直肠癌患者的p53状态如何,都有可能从这种联合治疗策略中获益。
这项研究为结直肠癌的治疗开辟了新方向。通过阻断HSF1-HSR轴,联合治疗显著提升了基于HSP90的治疗效果,且对正常组织和小鼠无明显毒性。未来,这一联合治疗策略有望进入临床试验,为广大结直肠癌患者带来更有效的治疗方案,提高患者的生存率和生活质量。医学研究人员也将继续深入探索,不断优化治疗方法,为攻克癌症这一难题持续努力。(生物谷Bioon.com)
参考文献:
Isermann T, Schneider KL, Wegwitz F, et al. Enhancement of colorectal cancer therapy through interruption of the HSF1-HSP90 axis by p53 activation or cell cycle inhibition. Cell Death Differ. Published online April 9, 2025. doi:10.1038/s41418-025-01502-x
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


