Science:针对BRCA2的新研究揭示了化疗耐药背后的新机制
来源:生物谷原创 2025-11-26 10:21
癌症治疗面临的最大挑战之一是化疗耐药性:原本对化疗反应良好的肿瘤会随着时间的推移产生耐药性。一旦发生这种情况,治疗选择往往非常有限。
由伊拉斯姆斯MC癌症中心分子遗传学系的Arnab Ray Chaudhuri领导的研究团队,现已揭示了BRCA2缺陷肿瘤产生这种耐药性的机制。蛋白质BRCA2和FIGNL1似乎具有与先前认知不同的功能。
Ray Chaudhuri表示:"这些发现改变了我们的思维范式。"该团队还找到了逆转或预防耐药性的方法。相关论文发表在《科学》杂志上。

化疗耐药性
BRCA2是一种通过名为"同源重组"的过程来修复毒性DNA双链断裂的关键蛋白质。在BRCA2突变的人群中,该修复机制无法正常运作,导致断裂无法修复,从而造成DNA损伤。其后果是患乳腺癌、卵巢癌或前列腺癌的风险显著增加。
为了治疗BRCA2突变肿瘤,通常采用靶向化疗药物,如PARP抑制剂。这类化疗会阻断另一种DNA修复机制:单链修复。由于缺乏BRCA2的癌细胞无法通过HR修复DNA断裂,它们依赖这种替代途径生存。当该途径被阻断时,癌细胞就会死亡。
然而,BRCA2突变肿瘤可以规避这种策略。通常,在几个月到几年后,肿瘤会停止对化疗产生反应。研究表明,BRCA2缺陷的癌细胞有时能设法恢复HR机制。这使得它们能够修复DNA并存活下来。在此之前,这一过程如何实现一直是个谜。
意想不到的发现
Ray Chaudhuri和他的团队发现,在缺乏BRCA2的细胞中,移除蛋白质FIGNL1可以恢复HR机制。
Ray Chaudhuri和Kuthethur解释道:"这个结果完全出乎意料。我们花了相当长的时间才完全理解并接受所发生的一切。这最终演变成一项多学科、多机构的研究工作,与Petr Cejka教授(瑞士贝林佐纳IRB研究所,该研究所隶属于USI)、Shyam Sharan博士(美国NIH)以及Krishna Mohan Poluri教授(印度IIT Roorkee)的实验室进行了重要合作。"
进一步的调查研究揭示了其中的机制:FIGNL1会主动将蛋白质RAD51从受损的DNA上移除。没有RAD51,HR就无法进行。但当FIGNL1失活时,RAD51就会留在原位。这使得细胞即使在没有BRCA2的情况下也能进行HR。
BRCA2作为调节因子
这些发现为理解BRCA2在HR过程中的作用提供了新的视角。Ray Chaudhuri解释说:"近25年来,人们一直认为BRCA2是将RAD51装载到受损DNA上最关键的因素,但现在看来,这可能不是故事的全部。"
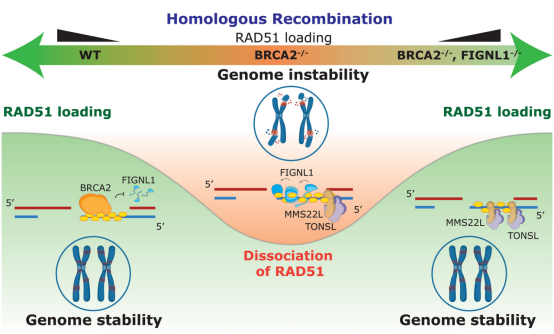
BRCA2的功能实际上更为精细。在健康细胞中,BRCA2和FIGNL1协同工作以维持平衡。BRCA2帮助RAD51与DNA结合,而FIGNL1则将其移除。两者共同微调修复DNA损伤所需的RAD51数量。
备用系统
在没有BRCA2和FIGNL1调控的情况下,RAD51需要另一个蛋白质复合物MMS22L-TONSL的帮助来执行HR。团队发现,该复合物充当了一个备用系统。在缺乏BRCA2和FIGNL1时,它会接管它们的角色,确保DNA中有足够的RAD51。
这最后一个发现对于治疗BRCA2突变肿瘤具有重要意义。那些对化疗产生耐药性的肿瘤,正是利用MMS22L-TONSL途径得以存活。
"但如果我们阻断MMS22L-TONSL,整个机制就会崩溃,"Ray Chaudhuri解释说。
通过靶向这个蛋白质复合物,可以使肿瘤重新对化疗敏感。这为治疗耐药性BRCA2肿瘤的患者开启了靶向疗法的新大门。(生物谷Bioon.com)
参考文献:
Raviprasad Kuthethur et al, FIGNL1 inhibits homologous recombination in BRCA2 deficient cells by dissociating RAD51 filaments, Science (2025). DOI: 10.1126/science.adt1210.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


