Science:靶向中介体复合物激酶模块可增强CAR-T细胞的抗肿瘤效力
来源:生物谷原创 2022-11-25 13:30
一项新的研究将中介体复合物诱导的转录共激活与T细胞分化联系起来,确定中介体复合物激酶模块是T细胞效应编程的主要调节因子,并证实MED12缺陷的T细胞在介导抗肿瘤作用方面的效力增强。
T细胞免疫疗法对某些癌症显示出令人印象深刻的疗效,但大多数患者并没有获得持久的反应。这类免疫疗法取得进展的核心障碍是T细胞效力不足,无法根除巨大的肿瘤负担,这是由多种因素造成的,包括T细胞衰竭、衰老、无能(anergy)和免疫抑制。基因编辑有潜力提高癌症免疫疗法的疗效,但目前仍不清楚哪些基因或哪组基因在编辑后能最有效地提高T细胞的效力。
在一项新的研究中,来自美国斯坦福大学的研究人员在人类T细胞中使用全基因组的CRISPR基因敲除筛选,以确定T细胞活力的调节因子。相关研究结果发表在2022年11月11日的Science期刊上,论文标题为“Enhanced T cell effector activity by targeting the Mediator kinase module”。
这些作者在人类嵌合抗原受体(CAR)T细胞(CAR-T)中进行了两次CRISPR筛选,使用的模型系统通过模拟慢性抗原暴露来诱导T细胞功能障碍。基于较高的增殖率和细胞因子产生率是最有效的抗肿瘤T细胞的特征这一假设,他们确定了在肿瘤暴露后增殖并产生白细胞介素-2(IL-2)和肿瘤坏死因子-α(TNFα)的T细胞中富含的向导RNA(gRNA)。
两次CRISPR筛选都发现了编码中介体复合物(Mediator complex)亚基的基因,这些基因包含在中介体复合物激酶模块中。中介体复合物作为增强子结合的转录因子和通用转录复合物(transcription machinery)之间的桥梁,通过协调转录网络在建立细胞身份方面起着核心作用。在人类CAR-T细胞中靶向剔除MED12(中介体复合物亚基12)或CCNC(细胞周期蛋白C)可导致增殖、细胞因子产生和肿瘤清除率增加。对于靶向多种肿瘤抗原和使用CD28或4-1BB共刺激的CAR以及在表达工程化T细胞受体(TCR)的T细胞中也观察到类似的效果。在许多模型系统中,具有干性(stemness)表型和转录组特征的T细胞显示出更高的抗肿瘤效力,然而,MED12缺失的T细胞显示出干性减弱和增强的效应细胞表型和转录组特征。与效应细胞的表型一致,MED12缺失的T细胞显示出增强的代谢活性和效力,其特点是糖酵解、氧化磷酸化和备用呼吸能力增加。MED12缺失的T细胞在长期培养和在体外和体内反复暴露于肿瘤后表现出持续的效力。小分子介导的对细胞周期蛋白依赖性激酶8和19(CDK8/19)---中介体复合物激酶模块的催化亚基---的抑制同样增加了健康的非工程化T细胞的增殖。
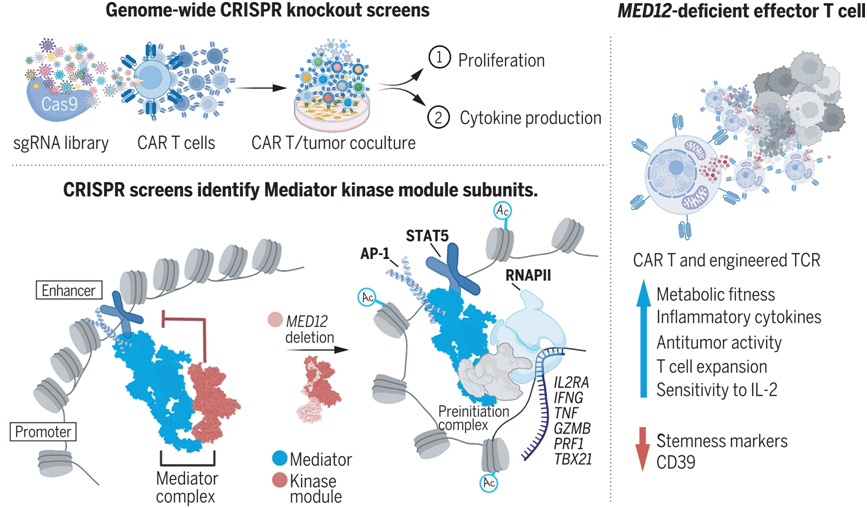
在人类T细胞中,破坏中介体复合物激酶模块会在转录上重新连接效应编程。图片来自Science, 2022, doi:10.1126/science.abn5647。
为了为理解这些观察结果提供基础,这些作者评估了MED12缺失的T细胞中染色质可及性和修饰的变化。通过使用染色质免疫沉淀测序,他们证实中介体复合物激酶模块和中介体复合物核心模块(core Mediator)在野生型CAR-T细胞中基本是共定位的,但MED12的缺失增加了中介体复合物核心模块在800多个基因组区域的染色质占用。这与已知的中介体复合物激酶模块在调节中介体复合物核心模块和RNA聚合酶II(RNAPII)之间的相互作用是一致的,并导致了这样的假设:T细胞中MED12或CCNC的缺失会选择性地减少中介体复合物核心模块和RNAPII之间的立体阻碍,从而增加转录和调节T细胞功能。与此相一致的是,在MED12缺失的CAR-T细胞中,MED1染色质占有率增加的区域表现为H3K27乙酰化增加,并且富集了在T细胞命运中起关键作用的转录因子---包括几个STAT和AP-1家族成员---所使用的增强子。在MED12缺陷的T细胞中,观察到最明显的增强是STAT5,它表现为对IL-2的敏感性增加。非工程化T细胞对IL-2的敏感性增加也可能是由于接触小分子CDK8/19抑制剂。
综上所述,这些数据将中介体复合物诱导的转录共激活与T细胞分化联系起来,确定中介体复合物激酶模块是T细胞效应编程的主要调节因子,并证实MED12缺陷的T细胞在介导抗肿瘤作用方面的效力增强。鉴于在细胞制造过程中和在体内使基因失活的技术越来越容易获得,这突显了这些发现的临床转化潜力。(生物谷 Bioon.com)
参考资料:
Katherine A. Freitas et al. Enhanced T cell effector activity by targeting the Mediator kinase module, Science, 2022, doi:10.1126/science.abn5647.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


