多肽抗氧化纳米酶治疗缺血性脑卒中的研究获进展
来源:生物物理所 2023-03-23 10:33
近日,中国科学院院士、中科院生物物理研究所研究员阎锡蕴团队针对缺血性脑卒中致死致残率高、缺乏高效低毒治疗药物的难题,发明了一种多肽抗氧化纳米酶(如图),其中的多肽能够靶向溶解血栓,MnO2纳米酶具有
纳米酶作为新兴技术之一,集天然催化与人工催化优势于一身,具有类似于天然酶的酶促反应动力学,可作为酶的替代品用于人类健康;具有稳定性高、成本低廉、易于规模化生产的特点,克服了天然酶的局限性;具有纳米材料的可设计性和多功能性,在工业、医学、生物等领域展现出广阔的应用潜力。如何利用纳米酶的独特性(如多酶活性、多功能和底物催化),创造一些新技术,解决一些天然酶或其他催化剂所不能为之的问题,是纳米酶领域当前面临的重要课题。
近日,中国科学院院士、中科院生物物理研究所研究员阎锡蕴团队针对缺血性脑卒中致死致残率高、缺乏高效低毒治疗药物的难题,发明了一种多肽抗氧化纳米酶(如图),其中的多肽能够靶向溶解血栓,MnO2纳米酶具有超氧化物歧化酶(SOD)和过氧化氢酶(CAT)催化活性,这两种酶的级联催化反应能够清除病灶区域的活性氧(reactive oxygen species,ROS)。动物实验显示,多肽抗氧化纳米酶在有效溶栓的同时,还能修复缺血再灌注损伤,有效缓解了脑组织缺血部位的氧化应激,减少了纳米酶的非特异性吸附和毒副作用,为缺血性脑卒中的治疗提供了新思路。相关研究成果在线发表在Advanced Materials上。
这种新型纳米酶的设计理念是将两种多肽链混合自组装形成直径为15 nm的纳米颗粒,其表面多肽包含靶向溶栓模块、凝血酶响应模块、血脑屏障穿越-脑缺血组织神经元靶向模块,并以内核的金属离子亲和肽为模板通过生物矿化合成MnO2纳米酶。结果表明,此多肽抗氧化纳米酶具有与天然酶相当的SOD(>2100 U/mg)和CAT(~300 U/mg)催化活性。这种多肽抗氧化纳米酶的工作原理是依次从外向内发挥靶向溶栓和清除ROS的功能。外表面的多肽能够特异结合血栓中的纤维蛋白,在凝血酶响应下释放溶栓肽,从而启动溶栓活性,进而靶向血脑屏障转铁蛋白受体,进入缺血缺氧脑组织,在此纳米酶发挥SOD和CAT双酶级联效应,即SOD将O2·-转化为H2O2和H2O,CAT将高细胞毒性的H2O2最终转化为无毒性的H2O和O2,安全有效地消除ROS。这种多肽抗氧化纳米酶在小鼠和大鼠缺血性脑卒中模型中表现出显著的神经功能恢复,梗死体积减少超过90%,治疗效果明显优于临床应用的溶栓药组织型纤溶酶原激活剂(tPA)和神经保护药伊达拉奉(Eda)。这是由于多肽具有的多功能性的优势使纳米酶精准靶向脑卒中缺血组织,保证了生物安全性,同时,纳米尺度的治疗体系使纳米酶在较长时间内发挥级联类酶活性,克服了目前小分子药物半衰期短、生物利用度低和严重毒副作用导致疗效有限的问题,为缺血性脑卒中的综合、安全、有效治疗提供了新思路。
研究工作得到国家自然科学基金、国家重点研发计划、中科院创新交叉团队、中科院青年创新促进会、中国博士后科学基金及北京市科技新星计划的支持。
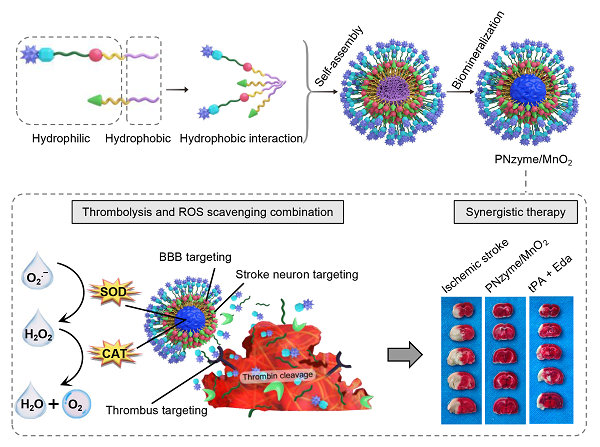
凝血酶响应型多肽抗氧化纳米酶的合成及治疗缺血性脑卒中原理示意图
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


