J Crohns Colitis:从肠上皮细胞端粒角度治疗溃疡性结肠炎的新方法
来源:本站原创 2021-07-26 15:27
溃疡性结肠炎(UC)是一种反复发作的结肠慢性炎症性疾病。在严重或长期病例中,肠上皮细胞端粒缩短已有报道。然而,其对UC发病机制的影响尚不清楚。为此,作者使用我们最初建立的长期器质性炎症模型来评估端粒缩短。本研究首次揭示了端粒缩短在UC发病机制中的作用。羟基积雪草苷(MD)可能是一种超越内镜黏膜愈合的UC治疗的新候选方法。图片来源:https://pubmed
溃疡性结肠炎(UC)是一种反复发作的结肠慢性炎症性疾病。在严重或长期病例中,肠上皮细胞端粒缩短已有报道。然而,其对UC发病机制的影响尚不清楚。为此,作者使用我们最初建立的长期器质性炎症模型来评估端粒缩短。本研究首次揭示了端粒缩短在UC发病机制中的作用。羟基积雪草苷(MD)可能是一种超越内镜黏膜愈合的UC治疗的新候选方法。
图片来源:https://pubmed.ncbi.nlm.nih.gov/34180971/
溃疡性结肠炎(UC)是常见的顽固性疾病,复发频繁。因此,UC治疗的当前目标是在临床缓解后的内镜下粘膜愈合,以防止复发。最近已经开发了许多免疫抑制生物制剂来实现粘膜愈合;然而,这些抗炎方法在某些情况下效果不够好。此外,组织学炎症最近被报道为比内镜黏膜愈合更好地预测皮质类固醇的使用和住院风险。此外,溃疡性结肠炎完全的组织学正常化,定义为没有结构改变和炎性浸润,被提倡给予比单纯消退炎症更有利的预后,尽管没有前瞻性的数据来证明实现这一组织学目标的益处。然而,在UC治疗中实现这些目标的策略和方法是有限的。由于UC的发病不仅涉及炎症,还涉及肠上皮细胞(IECS),因此有必要针对UC患者结肠粘膜IECS采取新的治疗策略。
最近,报道了一种从UC患者身上建立有机体的技术。这项技术可以将UC患者的IECS与健康人的IECS进行直接比较。此外,患者衍生的有机化合物保持了患者特有的特征,如细胞损伤[体积减小,细胞死亡增加]。然而,由于患者的多样性和异质性,这种方法仍然有局限性,因为它不能用于确定UC的新治疗靶点。作者前建立了一个使用结肠有机化合物长期炎症刺激的体外人类UC模型。作者还建立了小鼠结肠粘膜异种移植的体内模型。这些模型在体外复制了UC患者衍生的有机体(Pt-有机体),甚至复制了UC的组织学变化,如隐窝变形和杯状细胞耗竭。此外,他们还揭示了由慢性炎症引起的Schlafen家族成员11(SLFN11)与粘膜损伤密切相关。更具体地说,在UC模型的类器官中下调SLFN11 (SLFN11- KD)可以通过抑制细胞凋亡来模拟UC的再生变化,提高异种移植的移植物取片率,以及内镜下黏膜愈合的UC患者的组织学表现。然而,SLFN11-KD不能完全治疗UC,因为在组织学分析中,SLFN11-KD隐窝仍有结构变化,如隐窝变形和杯状细胞耗尽。
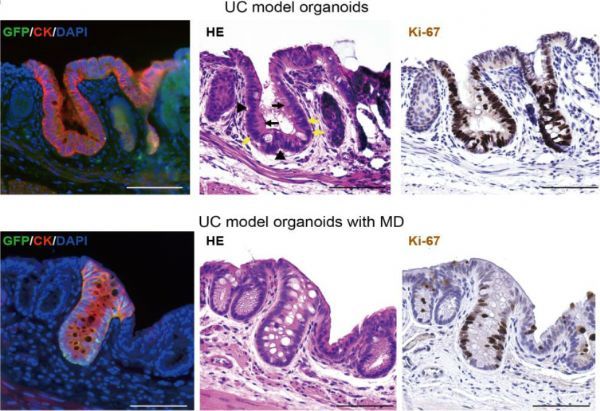
人结肠类器官移植隐窝的病理学分析
图片来源:https://pubmed.ncbi.nlm.nih.gov/34180971/
端粒是位于染色体末端保护染色体末端免受dna损伤的区域。在大多数人类体细胞中,端粒长度随着细胞分裂的每个周期而缩短。当端粒达到临界长度时,就会触发衰老或细胞死亡。几种刺激可以加速端粒缩短,包括氧化应激和炎症。虽然有报道称重度和长期UC患者的结肠黏膜端粒缩短,但关于这些端粒改变是如何发生的以及端粒缩短对结肠iec和UC发病机制的影响尚不清楚。
基于上述原因,作者使用我们的超长期炎症UC模型评估了结肠内皮细胞端粒长度的时序性变化。本研究进一步探讨端粒缩短在结肠IECS中的作用机制及其对UC发病机制的影响。此外,作者利用体外和体内模型研究了端粒酶激活剂作为一种新的UC治疗方法的潜力。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。