Cell Rep Med | 武汉大学汪晖团队揭示产前地塞米松暴露对后代肠道菌群和疾病易感性的影响机制
来源:生物探索 2024-02-08 16:01
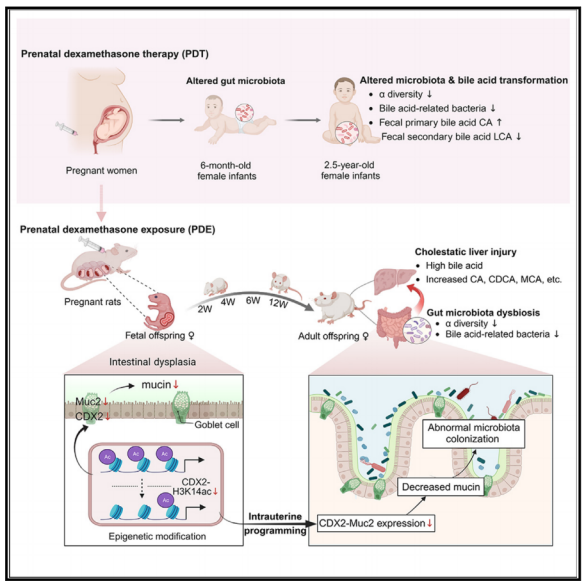
该研究揭示了产前地塞米松治疗(PDT)的人类后代和PDE的大鼠后代肠道微生物群组成的变化。
武汉大学汪晖团队在Cell Reports Medicine (IF 14.3)在线发表题为“Epigenetic programming mediates abnormal gut microbiota and disease susceptibility in offspring with prenatal dexamethasone exposure”的研究论文,该研究发现6个月大的婴儿在产前地塞米松治疗(PDT)中肠道微生物群的性别差异变化持续到2.5岁的女婴胆汁酸代谢改变。
PDE雌性后代大鼠肠道菌群定植和组成异常,对胆汁淤积性肝损伤的易感性增加。PDE子代肠道菌群定植异常可能与出生前后CDX2表达降低导致Muc2表达受到抑制有关。结合动物实验和细胞实验,进一步证实了地塞米松通过激活GR/HDAC11信号通路和调节CDX2表观遗传修饰来抑制Muc2的表达。该研究解释了宫内肠道菌群失调的PDT后代的肠道微生物群异常和疾病易感性。

肠道菌群建立于寄主童年早期,在此期间共生菌的定植对寄主的发育和长期健康至关重要孕期健康的母体环境是子代肠道菌群发育的重要保证。然而,越来越多的流行病学调查表明,怀孕期间不良的母体环境因素会干扰后代的肠道微生物群,导致他们在成年后易患多种疾病。例如,母亲在怀孕期间使用各种抗生素治疗会增加后代患免疫和代谢疾病的风险,并伴有肠道微生物群紊乱。同时,动物研究证实,孕妇肥胖或妊娠期接触三氯蔗糖可通过调节肠道菌群导致子代对肝脏疾病的易感性。然而,怀孕期间的不利环境因素如何影响后代肠道菌群定植,从而导致肠道菌群组成和功能的改变,目前尚不清楚。
产前皮质类固醇治疗是通过促进胎儿肺成熟来降低新生儿呼吸窘迫综合征(RDS)发生率和围产期死亡风险的有效措施。目前世界卫生组织(世卫组织)的建议是注射地塞米松或倍他米松,例如,每12小时注射6毫克地塞米松,共4次剂量,或每24小时注射12毫克倍他米松,共2次剂量(单疗程),以促进胎儿肺成熟。尽管产前皮质类固醇在保护新生儿呼吸系统方面有短期益处,但其对其他器官的影响尚不清楚。然而,单疗程的产前皮质类固醇治疗与不良的神经认知和/或心理结果、新生儿低血糖和胎儿发育抑制有关,而多疗程的产前皮质类固醇治疗也与低出生体重和心血管疾病风险增加有关。
之前的非靶向代谢分析显示,产前地塞米松暴露(PDE)改变了出生前后的血胆汁酸水平,并导致成年后代大鼠的肝损伤肠道菌群在胆汁酸代谢中起重要作用。进入肠道后,肝脏合成的原胆汁酸通过肠道菌群的解偶联、脱氢和去羟基作用进一步代谢生成二级胆汁酸。然而,PDE是否会影响肠道菌群定植和组成?这些肠道菌群的改变是否与PDE成年后代的疾病易感性(例如,胆汁淤积性肝损伤)有关?这些问题都不清楚。
模式图(Credit: Cell Reports Medicine)
肠道菌群的定植需要足够的粘附位点和适宜的肠道微环境Mucin-2 (Muc2)是肠黏液层的主要成分,主要由杯状细胞分泌下调肠道Muc2表达可改变肠道微环境,从而影响肠道菌群的定植和组成。“宫内编程”是指在妊娠期由于不利环境因素导致的胎儿形态和功能发育的改变,这种改变可以在出生后持续存在,甚至持续一生。表观遗传学是指在不改变DNA序列的情况下基因表达的可遗传变化。研究发现糖皮质激素治疗引起的异常表观遗传修饰可导致多器官功能障碍。因此,研究人员推测PDE通过表观遗传修饰调控子代肠道粘蛋白合成,导致肠道菌群定植和组成异常。
该研究揭示了产前地塞米松治疗(PDT)的人类后代和PDE的大鼠后代肠道微生物群组成的变化。然后,通过PDE证实了肠道Muc2表达的宫内编程,并破译了相关的表观遗传机制。最后,证实了PDE诱导的后代肠道微生物群改变使他们容易发生胆汁淤积性肝损伤。该研究确定了肠道菌群定植的影响因素,为探索与肠道菌群异常相关的胎源性疾病的潜在机制奠定了理论和实验基础。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


