Cell子刊:聂广军/赵瑞芳团队揭示新辅助化疗增强癌症疫苗效果
来源:生物世界 2024-12-28 14:30
该研究表明,纳米脂质体多柔比星新辅助化疗,增强基于肿瘤膜抗原的纳米疫苗的免疫保护作用。
国家纳米科学中心聂广军、赵瑞芳团队在 Cell 子刊 Cell Reports Medicine 上发表了题为:Neoadjuvant chemotherapy by liposomal doxorubicin boosts immune protection of tumor membrane antigens-based nanovaccine 的研究论文。
该研究表明,纳米脂质体多柔比星新辅助化疗,增强基于肿瘤膜抗原的纳米疫苗的免疫保护作用。

在临床实践中,许多癌症患者在接受个性化肿瘤疫苗之前可能已经接受了各种治疗。例如,部分患者可能会在术前进行全身系统性化疗,即新辅助化疗,以降低肿瘤的临床分期,改善术前状态,为后续手术创造有利条件。研究表明,化疗可以潜在地增强肿瘤微环境的免疫格局,使其转向免疫激活状态。但同时,化疗引起的全身不良反应也会对免疫系统产生有害的影响。
肿瘤细胞膜对化疗刺激的动态变化可能直接影响肿瘤膜疫苗的效果。因此,在实施上述条件下的自体肿瘤疫苗时,需要考虑化疗引起的变化,无论是患者整体免疫状态的变化,还是肿瘤本身的修饰。但目前尚未报道这些改变是否会影响疫苗的效力。
在这项最新研究中,研究团队探索了术前化疗对自体肿瘤细胞膜抗原疫苗(tumor cell membrane antigen-based vaccine,TMV)疗效的影响。
化疗药物多柔比星(Dox)可在肿瘤中诱导免疫原性细胞死亡(ICD),释放肿瘤抗原和免疫相关信号,进一步触发免疫应答。但考虑到游离态多柔比星具有严重毒性作用,可能会影响免疫系统,研究团队选择更安全、更有效的纳米脂质体多柔比星(NP-Dox),同时以游离态多柔比星作为对照。
研究团队以肿瘤膜为抗原制备肿瘤细胞膜抗原疫苗(TMV),并以高效的双重TLR7/8激动剂瑞喹莫特(R848)为佐剂。但值得注意的是,R848在体内代谢迅速,容易发生严重的免疫相关不良事件。因此,研究团队将其包裹在聚乳酸-羟基乙酸共聚物(PLGA)纳米颗粒中,从而实现抗原和佐剂的共递送。
研究团队首先分析了暴露于不同治疗的肿瘤的膜蛋白的变化,然后通过实施上述程序研究了小鼠的免疫反应,进而评估TMV在术后小鼠模型中预防复发和转移的作用,以解释术前化疗对TMV疗效的影响。
结果显示,纳米脂质体多柔比星改善了免疫抑制性的肿瘤微环境(TME),增强了肿瘤膜上免疫分子的表达。这促使肿瘤细胞膜抗原疫苗(TMV)产生了比单独的多柔比星治疗更强的免疫应答,从而产生了更有效的免疫保护作用。纳米脂质体多柔比星治疗的肿瘤制备的TMV诱导的树突状细胞成熟和T细胞活化优于多柔比星,从而在小鼠术后模型中显示出更好的预防复发和转移的效果。
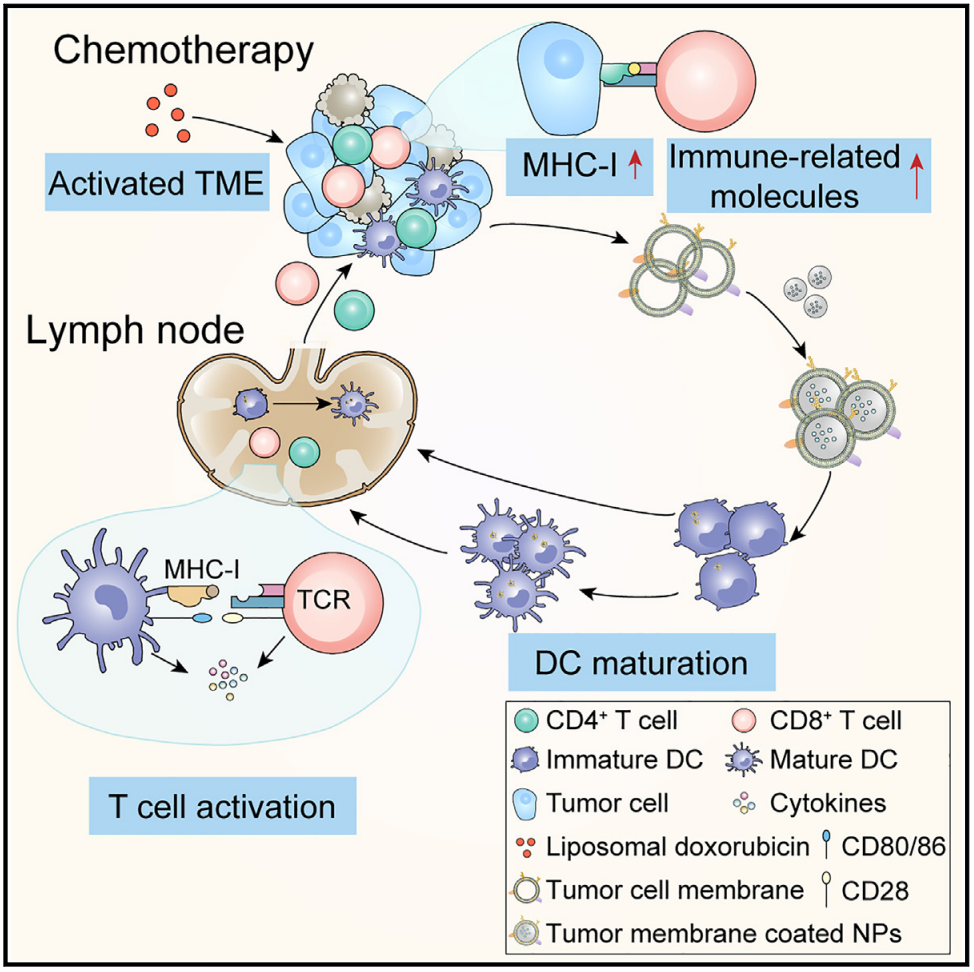
该研究的核心发现:
-
新辅助化疗有助于提高肿瘤细胞膜抗原疫苗(TMV)的疗效;
-
纳米脂质体多柔比星(NP-Dox)化疗可改善免疫抑制性肿瘤微环境;
-
NP-Dox化疗可增强肿瘤膜的免疫相关分子;
-
来源于NP-Dox治疗后的肿瘤的TMV,表现出强大的抗肿瘤作用。
总的来说,这项研究表明,化疗可以诱导免疫调节变化,从而增强免疫治疗的潜力,并为肿瘤细胞膜抗原疫苗(TMV)的临床应用提供了有价值的新见解。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


