Nat Commun | 马小彤/程涛/肖志坚/张磊团队首次揭示GADD45g是新的骨髓增殖性肿瘤致病因子
来源:生物探索 2024-04-16 09:24
本研究首次证明了GADD45g不足是MPN的一个新的致病因子,通过激活RAC2-PAK1-PI3K-AKT级联发挥作用。
中国医学科学院/北京协和医学院马小彤、程涛、肖志坚及张磊共同通讯在Nature Communications发表题为“Gadd45g insufficiency drives the pathogenesis of myeloproliferative neoplasms”的研究论文,该研究证明生长停滞和DNA损伤诱导的γ(GADD45g)在MPN患者中的表达水平显著降低,并且JAK2V617F突变和组蛋白去乙酰化导致其表达降低。
GADD45g的下调在人MPN细胞中起肿瘤促进作用。仅鼠造血系统中的Gadd45g功能不全就导致偏向髓样造血干细胞的生长和自我更新能力显着增强,以及类似于MPN的表型的发展。在机制上,GADD45g不足的致病作用是通过激活RAC2, PAK1和PI3K-AKT信号通路介导的。这些数据表明GADD45g缺乏是MPN的一种新的致病因素。

骨髓增生性肿瘤(MPN)是影响骨髓系细胞的造血干细胞(HSC)疾病。经典费城阴性 MPN PhMPN)的特征是一个或多个成熟髓系血细胞谱系的输出过多,包括真性红细胞增多症(PV)、原发性血小板增多症(ET)和原发性骨髓纤维化(PMF)。JAK2、CALR和MPL的突变,称为“驱动突变”,发生在超过95%的MPN患者中,导致JAK-STAT信号通路的组成型激活,然后引发疾病。此外,在MPN患者中,已发现与表观遗传调控、转录控制和剪接机相关的基因中同时发生的体细胞突变,先于驱动突变获得并导致疾病进展。其中,ASXL1、DNMT3A和TET2在整个MPNs频谱中超过5%的患者样本中处于相对较高的频率。
目前的治疗已显示出减少脾肿大和改善MPN患者症状的益处。然而,它们不能有效地根除MPNs干细胞,并且分子反应是可变的和不可预测的。更好地了解MPN的发病机制可能为开发有效的治疗方法提供新的靶点。编码小(18 kDa)核/细胞质蛋白的GADD45基因家族(GADD45a、GADD45b 和GADD45g)是应激传感器。之前的研究表明,GADD45g在急性髓系白血病(AML)患者中优先沉默,其上调发挥选择性和有效的抗白血病作用。然而,GADD45g是否在MPN的发展中发挥作用仍然未知。
该研究发现GADD45g表达在MPN患者中显著降低,并且与较高的克隆生成潜力和炎症细胞因子产生呈负相关。仅缺乏Gadd45g就足以引起小鼠的MPN。GADD45g不足通过激活RAC2-PAK1-PI3K-AKT信号通路发挥肿瘤促进活性。最常见的驱动突变JAK2V617F和组蛋白去乙酰化与 MPN 中的GADD45g 沉默有关。该研究首次证明了GADD45g不足在MPNs中的致病作用。
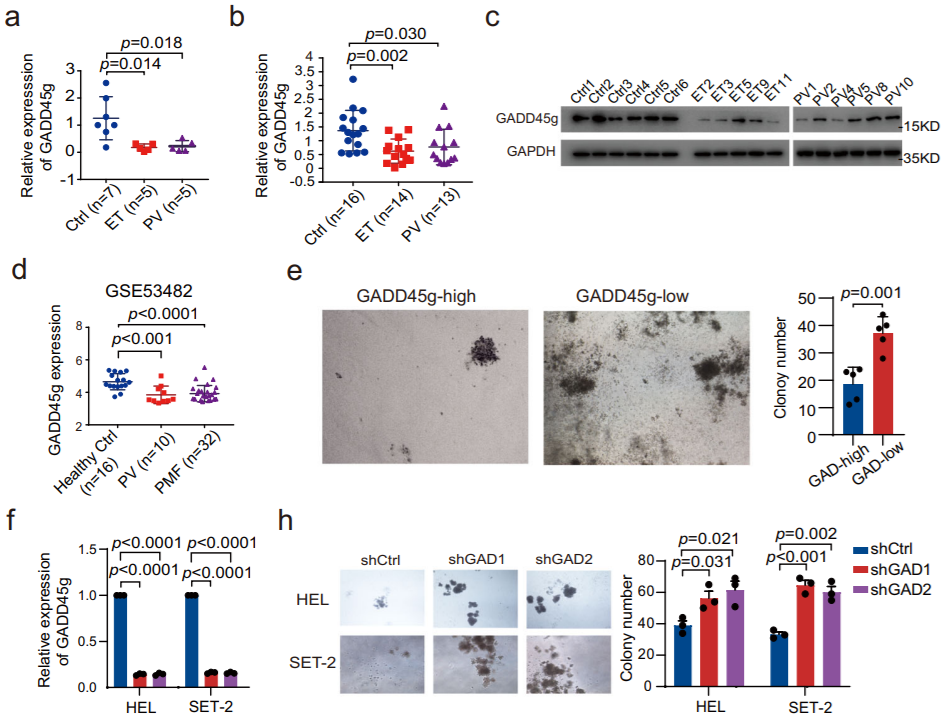
降低人MPNs细胞中GADD45g的表达具有促进肿瘤的功能(Credit: Nature Communications)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


