JAMA Oncology权威综述:对决致命的小细胞肺癌,现代医学何时能够“道高一丈”?
来源:奇点糕 2023-02-01 14:36
SCLC整体仍是一种治疗难度极大的肿瘤,现有治疗手段带来的生存获益十分有限,因此其防治一方面仍然要从预防出发,通过加强戒烟等方式降低发病率,另一方面就是推动创新治疗药物的研发,在机制层面的深入研究
小细胞肺癌(SCLC)约占全部肺癌的15%,素来以恶性程度高、进展速度快、极易远处转移和治疗后复发著称,因此患者的预后也极差,如果确诊时病情已处于广泛期(ES-SCLC),既往接受化疗患者的中位总生存期(OS)就不足一年。
可想而知,临床对SCLC治疗手段的需求是极其迫切的。近年来虽然有多种PD-1/L1抑制剂+化疗方案,取得了ES-SCLC一线治疗临床研究的成功,但生存获益还都相当有限,多数患者仍难以获得长期生存,也缺少指导治疗的生物标志物。
那么SCLC到底有多难缠,在研的创新治疗药物和方案又有哪些呢?近期在JAMA Oncology上,来自美国和西班牙的两位专家就共同撰文,全面盘点了SCLC的病理生理机制、分期、诊断,以及现有和在研的治疗策略[1],一起来看吧!

论文首页截图
SCLC的肿瘤生物学行为特点和病理生理机制
SCLC是一种神经内分泌肿瘤,常伴有副肿瘤综合征(paraneoplastic syndromes),且以增殖和生长速度快、发生远处转移较早为特点,有研究基于基因、转录组和免疫特征,对SCLC进行了亚型上的划分,但相关研究还处于早期阶段。
1)基因特征
已有研究揭示,几乎所有SCLC中均存在两大抑癌基因,即TP53(75-90%)、RB1(60-90%)功能完全失活,它们可能是SCLC发生发展的必要条件;编码组蛋白乙酰转移酶CREBBP和EP300的基因突变可能也参与了疾病进程[2]。
不过上述研究分析的大多是可经手术切除的肿瘤样本,结论或不能完全适用于ES-SCLC,此外还有研究提示SCLC中存在Notch信号通路基因的序列变异,TP73融合转录,以及MYC家族基因、FGFR1及SOX2的扩增等等[3]。
2)转录组学及分型
2019年发表在Nature Reviews Cancer的一篇专家意见性文章,建议基于SCLC中ASCL1、NEUROD1等关键转录因子的表达情况,划分出四种SCLC亚型,以更好地区分神经内分泌/非神经内分泌型SCLC,不同亚型的特征具体如下图所示。
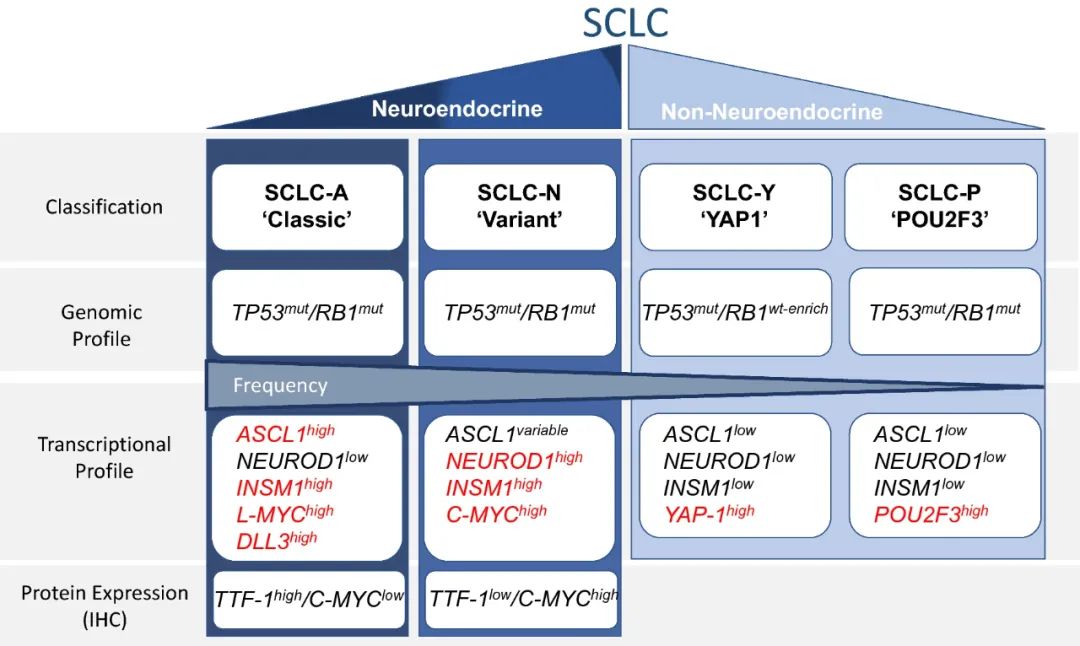
2019年国际专家基于转录因子表达提出的SCLC亚型划分
3)免疫学特征和免疫病理机制
虽然SCLC存在肿瘤突变负荷高、副肿瘤综合征等可能提示免疫原性的特点,但它却是名副其实的冷肿瘤,肿瘤浸润淋巴细胞(TILs)、CD8/CD3比值及癌细胞上的MHC-I/II类分子表达都相当低,而且免疫抑制性微环境可能是SCLC发生发展的关键,肿瘤相关巨噬细胞(TAMs)也可能参与了抑制性微环境的形成。
而在免疫检查点方面,SCLC微环境中的TILs上可能存在PD-L1、TIM3和LAG3等检查点表达,对预后有一定提示价值,但从免疫一线治疗的CASPIAN研究分析结果来看,患者PD-L1表达水平普遍偏低,也不能指导免疫治疗的使用[4]。
不过2021年发表在Cancer Cell上的一项研究,将上文提到的SCLC转录亚型与免疫通路激活情况进行结合,划分出了新的亚型——炎症型SCLC(SCLC-I),基于免疫一线治疗的IMpower133研究数据,此类患者从免疫治疗中获益更多[5]。
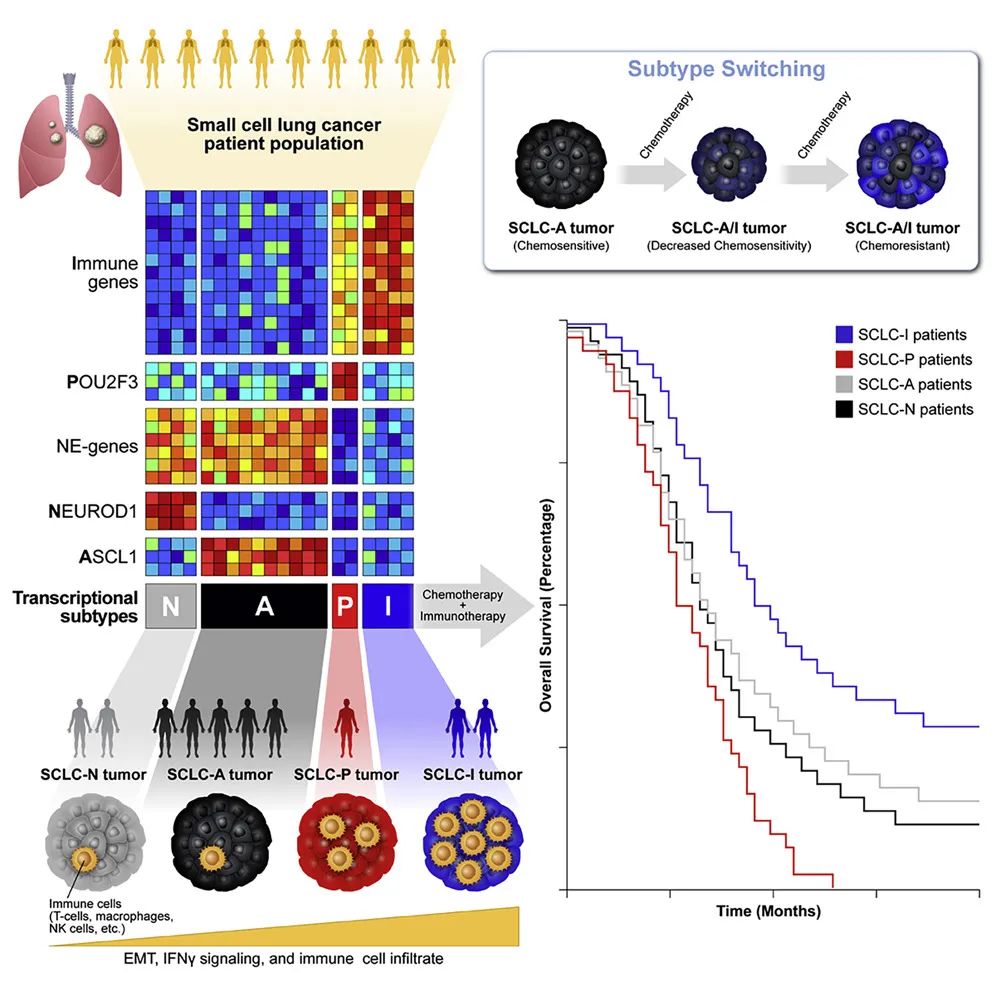
SCLC-I亚型患者从免疫治疗中的获益
SCLC的分期和预后
被普遍使用的SCLC分期方式是美国退伍军人医院分期法,即区分局限期(LS-SCLC)和广泛期,分别大致对应TNM分期的I-III期和IV期,两类患者分别占全部SCLC的30%和40%,另有30%分期不确切,该分期也是选择治疗的主要依据。
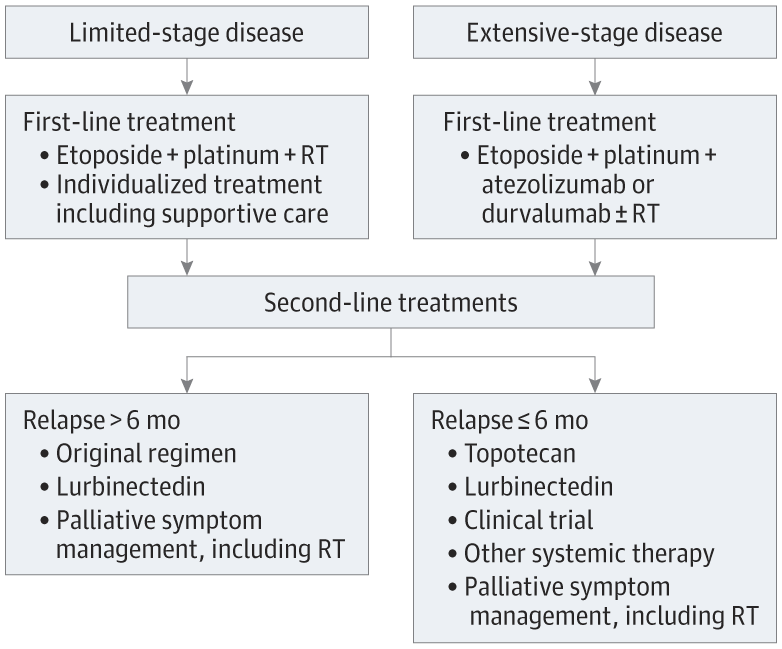
SCLC治疗流程图
LS-SCLC的一线治疗
除少数可手术患者外,LS-SCLC的治疗主要包括系统性药物治疗和放疗(含预防性脑照射),药物治疗最常用的是依托泊苷+铂类化疗(可选卡铂或顺铂,效果并无差异),而放疗对提高局部控制率和改善生存率均有明确作用。目前免疫治疗的使用尚未前移到LS-SCLC阶段,但众多临床研究正在紧锣密鼓地开展之中。
ES-SCLC的一线治疗
与LS-SCLC治疗类似,依托泊苷+铂类化疗曾长期是ES-SCLC一线治疗标准方案,放疗作用则不明显。而进入免疫治疗时代,IMpower133、CASPIAN两项关键临床III期研究奠定了PD-1/L1抑制剂+化疗方案的地位,2022年又有两种国产免疫治疗药物(斯鲁利单抗、Adebrelimab)在设计相似的研究中取得成功[6-7]。
在上述几项临床研究中,免疫+化疗方案均“显著降低了患者死亡风险”,但从目前公布的长期随访数据来看,能通过治疗实现长期生存的患者仍是少数,如CASPIAN研究的2年OS率为22.9%,3年OS率为15.3%[8];国产PD-L1抑制剂Adebrelimab的CAPSTONE-1研究中,免疫治疗组患者的2年OS率则为31.3%。
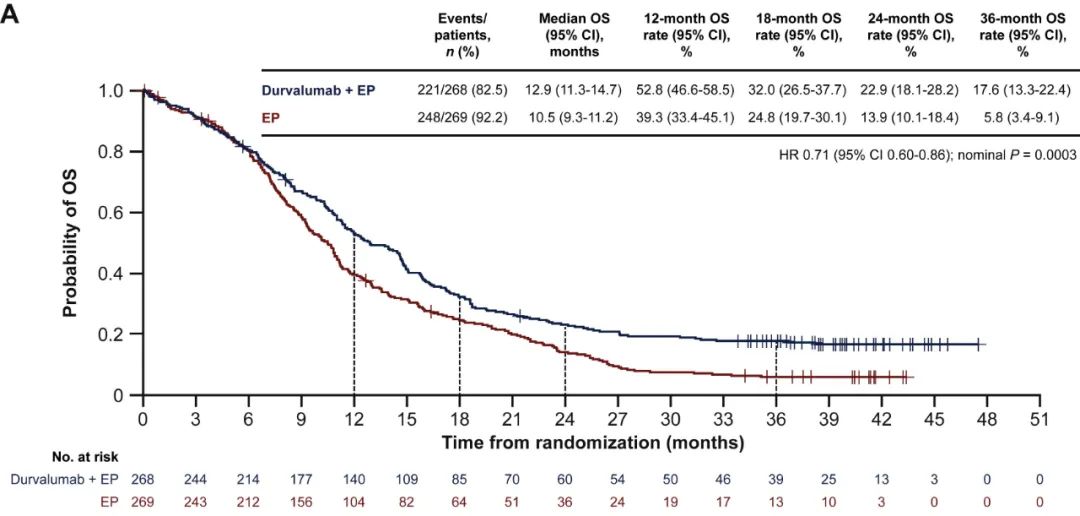
CASPIAN研究的3年OS随访结果
除PD-1/L1抑制剂外,也有临床III期研究尝试使用CTLA-4抑制剂,但无论是单独联合化疗(CA184-156研究),或是采用双免疫+化疗(CASPIAN研究双免疫组),CTLA-4抑制剂的探索均以失败告终,这可能与不同免疫治疗药物的作用机制差异有关,还有研究正在探索放疗、抗血管生成类靶向药与免疫治疗联合是否有效。
SCLC后线治疗
由于SCLC极易复发,绝大多数患者均需要接受后线治疗。一般认为如从初治到复发的时间<3个月,则患者属于难治性疾病,一般不能重复使用此前的治疗方案(时间>6个月则可复用),Meta分析显示此类患者后线治疗的客观缓解率(ORR)偏低(14.8%,非难治性患者为27.7%[9]),中位OS仅为6.7个月,预后极差。
因此临床亟需对难治性SCLC患者有效的治疗方案,但既往获批的药物寥寥,如在美国仅有拓扑替康获FDA正式批准;直到2020年FDA才基于临床II期研究中35.2%的ORR数据,经加速审批通过致癌基因转录抑制剂类新药Lurbinectedin上市,用于含铂化疗后疾病进展的SCLC患者(含难治/非难治性患者)。
但在后续的关键临床III期ATLANTIS研究中,Lurbinectedin联合多柔比星的方案,较对照组(医师选择的化疗)未能显著延长患者中位OS,其它疗效终点也未体现优势[10]。不过FDA认为该研究设计与既往II期研究并不完全相同,且Lurbinectedin治疗剂量偏低可能影响了结果,并未撤回该适应证批准。
而Lurbinectedin的研发方则启动了另外两项关键的临床III期验证性研究,其中二线治疗研究采用Lurbinectedin+伊立替康方案,该方案在临床Ib/II期研究中报告的ORR达到62%,另一项则是Lurbinectedin+阿替利珠单抗用于一线化疗后维持治疗的研究,这两项研究将决定Lurbinectedin在SCLC治疗领域的未来。
目前获国内外肺癌诊疗指南推荐的SCLC后线治疗方案,还有伊立替康、紫杉醇等药物单独化疗、联合化疗【如环磷酰胺/多柔比星/长春新碱(CAV)方案】及抗血管生成药物单药治疗(如我国指南推荐的安罗替尼)等,而由于III期研究未能证实临床获益,多种PD-1抑制剂的单药后线治疗适应证纷纷被撤回。

最新版美国NCCN指南(2023.V3版)对SCLC后线治疗的推荐
值得高度关注的SCLC在研疗法
SCLC创新疗法的开发难度相当之大,比如被寄予厚望的新型免疫检查点抑制剂Tiragolumab(TIGIT抑制剂),近期就在关键临床III期研究中失利。但高风险往往伴随着高收获,因此SCLC的临床研究一直热度很高,已进入临床III期研究阶段的有新剂型化疗药物(伊立替康脂质体)、PARP抑制剂(如Niraparib)等。
此外基于临床前研究结果,还有多种创新靶向和免疫治疗药物开展了治疗SCLC的早期研究,如靶向细胞内感知复制应激的ATR激酶抑制剂、CDK7抑制剂、极光激酶A抑制剂,通过调节免疫应答起效的DLL3抑制剂,靶向SCLC表面肿瘤相关抗原FucGM1的单抗药物、抗CD47单抗等等。
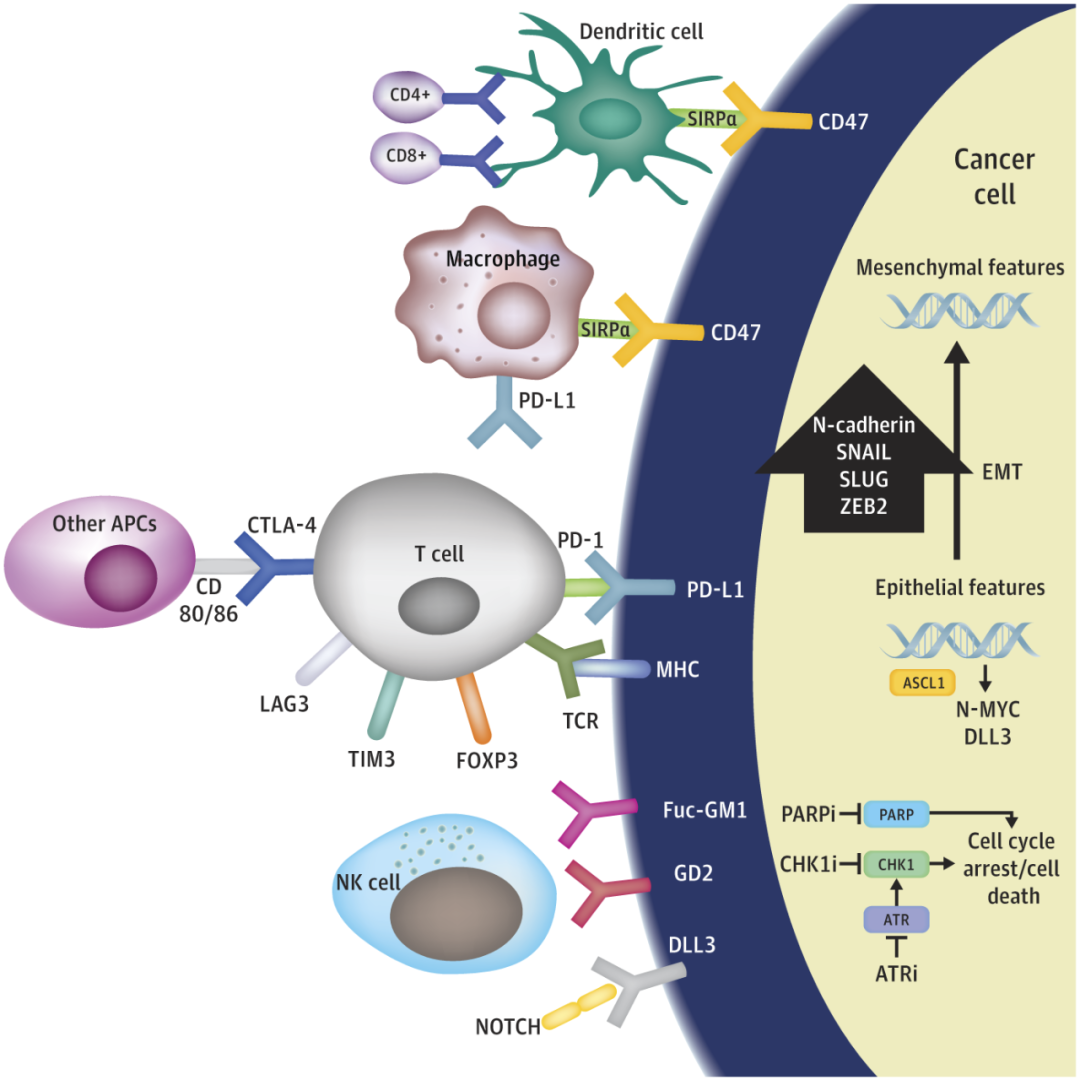
SCLC的病理生理机制及部分潜在治疗靶点
总结
SCLC整体仍是一种治疗难度极大的肿瘤,现有治疗手段带来的生存获益十分有限,因此其防治一方面仍然要从预防出发,通过加强戒烟等方式降低发病率,另一方面就是推动创新治疗药物的研发,在机制层面的深入研究,有望发掘更多潜在治疗靶点和指导治疗的生物标志物,逐渐改变SCLC的治疗格局和患者预后。
参考文献:
[1]Petty W J, Paz-Ares L. Emerging Strategies for the Treatment of Small Cell Lung Cancer: A Review[J]. JAMA Oncology, 2022.
[2]George J, Lim J S, Jang S J, et al. Comprehensive genomic profiles of small cell lung cancer[J]. Nature, 2015, 524(7563): 47-53.
[3]齐静, 徐波. 小细胞肺癌多基因组学研究进展[J]. 肿瘤研究与临床, 2021, 33(7): 549-552.
[4]Paz-Ares L, Goldman J W, Garassino M C, et al. PD-L1 expression, patterns of progression and patient-reported outcomes (PROs) with durvalumab plus platinum-etoposide in ES-SCLC: Results from CASPIAN[J]. Annals of Oncology, 2019, 30(Supplement 5): v928-v929.
[5]Gay C M, Stewart C A, Park E M, et al. Patterns of transcription factor programs and immune pathway activation define four major subtypes of SCLC with distinct therapeutic vulnerabilities[J]. Cancer Cell, 2021, 39(3): 346-360. e7.
[6]Wang J, Zhou C, Yao W, et al. Adebrelimab or placebo plus carboplatin and etoposide as first-line treatment for extensive-stage small-cell lung cancer (CAPSTONE-1): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial[J]. The Lancet Oncology, 2022, 23(6): 739-747.
[7]Cheng Y, Han L, Wu L, et al. Effect of first-line serplulimab vs placebo added to chemotherapy on survival in patients with extensive-stage small cell lung cancer: the ASTRUM-005 randomized clinical trial[J]. JAMA, 2022, 328(12): 1223-1232.
[8]Paz-Ares L, Chen Y, Reinmuth N, et al. Durvalumab, with or without tremelimumab, plus platinum-etoposide in first-line treatment of extensive-stage small-cell lung cancer: 3-year overall survival update from CASPIAN[J]. ESMO Open, 2022, 7(2): 100408.
[9]Owonikoko T K, Behera M, Chen Z, et al. A systematic analysis of efficacy of second-line chemotherapy in sensitive and refractory small-cell lung cancer[J]. Journal of Thoracic Oncology, 2012, 7(5): 866-872.
[10]Aix S P, Ciuleanu T E, Navarro A, et al. Combination lurbinectedin and doxorubicin versus physician's choice of chemotherapy in patients with relapsed small-cell lung cancer (ATLANTIS): a multicentre, randomised, open-label, phase 3 trial[J]. The Lancet Respiratory Medicine, 2023, 11(1): 74-86.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


