LncRNA HIF1A-AS1通过调节AKT/YB1/HIF-1α通路增强糖酵解,促进胰腺癌吉西他滨耐药
来源:本站原创 2021-10-15 21:53
吉西他滨(GEM)耐药是胰腺癌(PC)化疗面临的主要挑战。既往研究报道了lncRNA在PC肿瘤发生中的作用,但lncRNA是否参与PC GEM耐药的发展尚不清楚。
吉西他滨(GEM)耐药是胰腺癌(PC)化疗面临的主要挑战。既往研究报道了lncRNA在PC肿瘤发生中的作用,但lncRNA是否参与PC GEM耐药的发展尚不清楚。在本研究中,作者证明了在gem耐药的PC细胞中HIF-1α的反义RNA1 (HIF1A-AS1)显著升高。功能增益和功能缺失实验证实HIF1A-AS1在体外和体内均能促进PC细胞对GEM的抗性。作者进一步发现,HIF1A-AS1上调HIF-1α的表达,从而促进糖酵解,增强PC细胞对GEM的抗性。
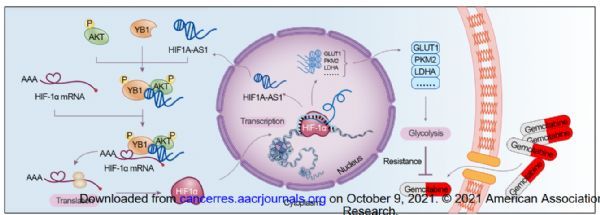
在机制上,HIF1A-AS1促进了丝氨酸/苏氨酸激酶AKT和Y-box结合蛋白1 (YB1)的相互作用,从而促进了YB1 (pYB1)的磷酸化。同时,HIF1A-AS1将pYB1募集到HIF-1α
mRNA中,从而促进HIF-1α的翻译。此外,HIF-1α通过直接结合HIF1A-AS1启动子区域的HIF-1α响应元件而促进HIF1A-AS1转录,形成正反馈。一贯地,HIF1A-AS1和HIF-1α在PC组织中均上调,并与较差的总生存率相关。
图片来源:https://pubmed.ncbi.nlm.nih.gov/34593522/
胰腺癌(PC)是发达国家最致命的疾病之一,5年生存率低于6%,预计到2030年将成为癌症死亡的第二大原因。大多数PC患者直到疾病发展到晚期才意识到身体状况的恶化。低生存率主要是由于早期局部浸润和远处转移。更重要的是,由于PC耐药的发展导致的治疗反应差仍然是一个重要的临床挑战,并导致患者的整体预后差。吉西他滨(GEM)单独或联合其他药物是目前晚期转移性PC的标准,如GEM/nab-紫杉醇、GEM/卡培他滨、GEM/厄洛替尼等。
然而,许多PC患者对GEM治疗最初表现出敏感性,随后迅速发展为耐药,导致患者生存期急剧下降。研究人员从药物转运、药物代谢、信号通路等多个角度探索GEM耐药机制。脱氧胞苷激酶(dCK)是GEM胞内激活和代谢的主要限速酶,其失活是GEM抗性的关键机制之一。同时,一些选择性抑制剂已经证实PI3K/AKT通路过度激活与GEM耐药有关。然而,阐明PC耐药的潜在机制仍是当务之急,这可能为治疗提供有前景的靶点。
长链非编码rna (long noncoding RNAs, lncRNAs)是一种长度超过200个核苷酸的非编码rna,通常失去蛋白质编码潜能。多项研究表明,lncrna已成为肿瘤细胞启动、生长、转移和化疗耐药能力几乎各个方面的重要调控因子。特别是研究发现,lncrna在GEM抗性PC细胞系中表达异常,说明lncrna是GEM敏感性的新型调控因子。例如,lncRNA生长抑制特异性转录本5 (GAS5)通过靶向miR-221/SOCS3在PC中逆转肿瘤干细胞介导的GEM耐药。
(GSTM3TV2)作为一种关键的内源性RNA,通过上调l型氨基酸转运体2
(LAT2)和氧化低密度脂蛋白受体1 (OLR1)增强PC的耐药能力。另一项研究报道lncRNA LINC00346可促进PC的GEM抗性,部分是通过拮抗miR-188-3p和诱导BRD4介导的。虽然这些结果提示lncrna可能在PC耐药过程中起到重要的调节作用,但lncrna在PC耐药GEM过程中的作用和机制尚不清楚,需要进一步阐明。
HIF1A-AS1/HIF-1α信号通路参与PC耐药的示意图
图片来源:https://pubmed.ncbi.nlm.nih.gov/34593522/
在本研究中,作者通过增加GEM处理培养基,建立了GEM抗性(GEM- r) PC细胞系(BxPC-3GEM-R/
pan - 1gem - r)。LncRNA-seq显示,与亲本BxPC-3细胞相比,BxPC-3GEM-R细胞中HIF-1α反义RNA HIF1A-AS1明显升高。因此,作者推测HIF1A-AS1可能是PC细胞对GEM耐药的重要的onco-lncRNA。巧合的是,该研究发现,HIF1A-AS1通过调节HIF-1α的表达,以糖酵解依赖的方式促进PC细胞的GEM抗性。进一步探讨了HIF1A-AS1调控HIF-1α表达的可能机制。进一步探讨了抗GEM PC细胞中HIF1A-AS1上调的调控机制。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。