Sci Adv:组合性表观遗传学癌症疗法或能有效治疗人类结直肠癌和其它肿瘤
来源:生物谷原创 2024-04-05 12:08
本文研究结果表明,补偿性的EZH2活性或能限制DNMTi在人类结肠癌中的疗效,同时研究人员还将NFAT:AP-1信号与表观遗传学治疗所诱导的病毒模仿联系了起来。
DNA甲基转移酶抑制剂(DNMTi,DNA methyltransferase inhibitor)在实体瘤中的疗效有限,暴露于DNMTi中的结肠癌细胞会在组蛋白H3上积累赖氨酸-27三甲基化(H3K27me3)。近日,一篇发表在国际杂志Science Advances上题为“Select EZH2 inhibitors enhance viral mimicry effects of DNMT inhibition through a mechanism involving NFAT:AP-1 signaling”的研究报告中,来自美国Van Andel研究所等机构的科学家们通过研究发现,能促使恶性细胞表现地像病毒一样的两种药物或有望帮助治疗人类结直肠癌和其它实体瘤。
在临床前研究中,研究人员揭示了低剂量的DNMT抑制剂如何促使癌细胞对EZH2抑制剂变得敏感,从而就会产生比单独使用任何一种药物更好的对抗癌细胞的双重打击;相关研究发现或为即将进行的I期临床试验奠定一定的基础,该临床试验评估了这种药物组合在治疗结直肠癌或其它实体瘤患者中的作用。研究者Scott Rothbart教授说道,DNMT抑制剂获批用于治疗人类血液癌症,同时EZH2抑制剂也被批准治疗血液癌症和一种罕见的肉瘤;截止到目前为止,其在诸如结直肠癌等人类实体瘤中取得的治疗成果非常有限。
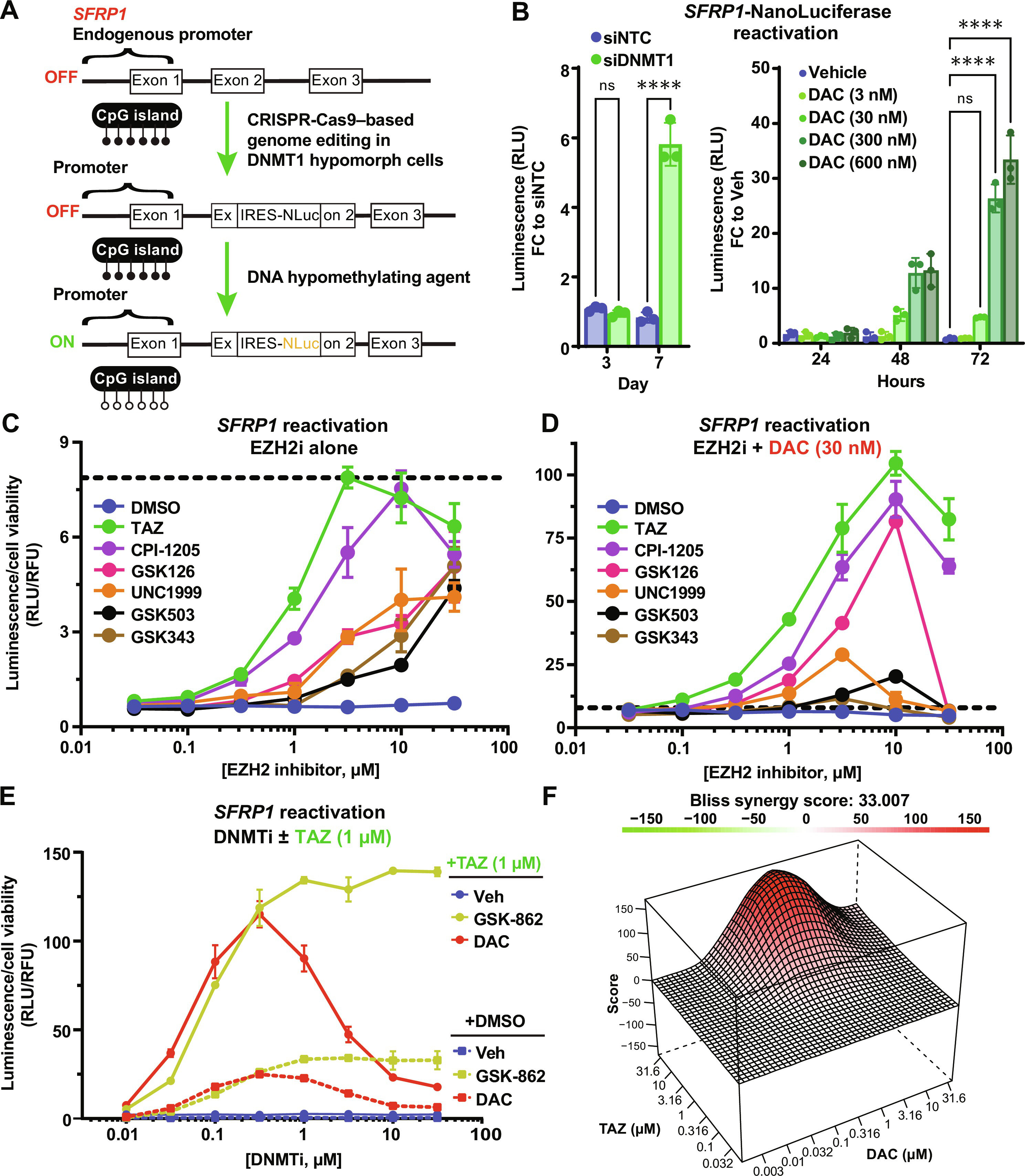
组合性表观遗传学癌症疗法或能有效治疗人类结直肠癌和其它肿瘤
图片来源:Science Advances (2024). DOI:10.1126/sciadv.adk4423
本文研究结果通过揭示这两种药物是如何相互作用,强调了组合性癌症疗法的治疗前景,DNMT抑制剂能以一种促使EZH2抑制剂更加有效的方式来启动癌细胞。DNMT和EZH2抑制剂能通过控制调节基因表达的表观遗传学过程来发挥作用,在癌症中,表观遗传学错误会促使恶性细胞得以生存和增殖,并为开发新型疗法提供了关键靶点。此前研究结果表明,DNMT抑制剂能促使癌细胞表现地像被病毒感染了一样,这就会使得细胞更容易被宿主机体的免疫系统所攻击。
在这项研究中,研究人员发现,将DNMT和EZH2抑制剂联合使用或许要比单独使用任何一种药物能更加有效地激活这种病毒模仿过程,即将到来的临床试验或许就是这两种类型药物的首次联合使用,其能增强这些抑制剂在治疗实体瘤中的活性。据WHO数据显示,结直肠癌如今已经成为了全球人群癌症死亡的第二大主要原因,2020年确诊病例有190多万人,预计到2040年这种癌症的发病率将会上升至320万人;尽管筛查和早期检测降低了美国老年人群的结直肠癌发病率,但年轻人的发病率却上升了。
研究者Rothbart说道,尽管目前还不清楚为何结直肠癌的发病率在年轻人中上升,但很明显的是,我们需要更为有效的疗法策略;联合用药或许就能作为一种强大的方法来同时靶向作用癌症的多种驱动因素,除了能揭示DNMT和EZH2抑制剂如何相互协同作用外,本文研究结果还表明,表观遗传学药物还能让肿瘤对免疫疗法变得敏感,这就为增强癌症治疗提供了另一种重要的机会。
综上,本文研究结果表明,补偿性的EZH2活性或能限制DNMTi在人类结肠癌中的疗效,同时研究人员还将NFAT:AP-1信号与表观遗传学治疗所诱导的病毒模仿联系了起来。(生物谷Bioon.com)
参考文献:
ALISON A. CHOMIAK,ROCHELLE L. TIEDEMANN,YANQING LIU, et al. Select EZH2 inhibitors enhance viral mimicry effects of DNMT inhibition through a mechanism involving NFAT:AP-1 signaling, Science Advances (2024). DOI:10.1126/sciadv.adk4423
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


