Nature系列综述:脂肪组织是生物衰老的关键
来源:生物世界 2024-05-27 09:55
各种新兴的实验方法为哺乳动物的衰老机制提供了新的见解。其中包括建立具有深刻特征的老年小鼠种群,并结合年龄相关特征的表型分析和遗传分析。
美国麻省大学医学院的 Silvia Corvera 教授在 Nature Metabolism 期刊发表了题为:Adipose tissue as a linchpin of organismal ageing 的综述论文。
该综述回顾了脂肪组织在衰老过程中的特征,并讨论了这些变化影响全身代谢、免疫和寿命的潜在机制。本综述还探讨了脂肪组织靶向治疗的潜力,以改善与年龄相关的疾病负担。

衰老会影响所有生物组织和器官功能,从而影响预期寿命的变化。不同物种的预期寿命各不相同,这表明衰老背后的机制是不同的。事实上,人类寿命的差异只有20-30%归因于遗传因素。衰老表现为多层次的复杂性。在细胞水平上,包括累积的DNA损伤和线粒体功能受损在内的因素决定了细胞和单细胞生物的寿命。在秀丽隐杆线虫等物种中,在发育过程中建立的细胞补体在生物体死亡前保持不变,时间并不是均匀地影响所有细胞,衰老受到细胞间信号机制的调节,该机制涉及到系统能量利用。在更复杂的物种中,干细胞和祖细胞可以通过替换受损细胞来减轻衰老的结局,从而影响寿命。衰老如何影响个体细胞功能、组织间和器官间的信号传导以及祖细胞/干细胞的维持尚不清楚。
各种新兴的实验方法为哺乳动物的衰老机制提供了新的见解。其中包括建立具有深刻特征的老年小鼠种群,并结合年龄相关特征的表型分析和遗传分析。其它的策略利用大量、单细胞和单核转录组学对衰老组织的细胞组成进行综合表型分析,并已应用于小鼠和人类。最近将异时异体共生(一种将年龄不同小鼠共享共同循环的方法)与单细胞分辨率的多种组织分析相结合 。这些研究中一个引人注目的发现是脂肪组织对年龄相关的扰动具有明显的反应性。例如,广泛的免疫细胞激活是衰老的保守标志,在白色脂肪中尤其明显,而且首先可以检测到。此外,脂肪组织祖细胞是对衰老和衰老环境最敏感的细胞之一。这些发现表明,脂肪组织在介导与衰老相关的系统性变化和调节与衰老相关的疾病风险方面发挥了关键作用。
与衰老相关的全身性衰退可能由脂肪组织通过多种机制介导:脂肪细胞是强大的内分泌细胞,分泌多种生物活性肽和细胞外囊泡。通过这些分泌产物,脂肪细胞可以对邻近组织和器官功能产生深远的影响,影响衰老和寿命。最近的研究揭示了不同类型的脂肪细胞,具有不同的分泌组和对特定储库附近细胞的潜在影响。此外,脂肪组织是支持组织发育和修复的多能祖细胞的生态位,并可能终生影响组织功能。本文回顾了最近关于不同脂肪储存库及其组成细胞如何介导衰老、衰老相关疾病和寿命的许多代谢和免疫特征的信息。本文还重点还回顾了利用脂肪组织生物学来减轻衰老相关疾病负担的潜在方法。
衰老过程中脂肪组织库的保守变化
脂肪组织在哺乳动物中起着至关重要的作用,因为缺乏脂肪会导致生物早期死亡。脂肪组织定位于特定的储存库,但也弥漫性地分布在不同组织和器官中,因此脂肪细胞直接接近多种细胞类型。下文回顾了脂肪库的功能和细胞组成、随着年龄的增长而发生的变化以及这些变化是如何在不同物种中保存下来的。
皮下白色脂肪组织
皮下白色脂肪组织(sWAT)位于皮肤真皮层下方。sWAT专门用于储存和释放能量,以甘油三酯和脂肪酸的形式,这是由白色脂肪细胞中专门的大脂滴介导的。这些特殊的液滴可以占据细胞体积的90%以上,并有效地从细胞质溶胶中隔离脂质。在禁食反应中,甘油三酯被水解,脂肪酸从液滴中释放到血液循环中,提供全身能量来源。脂滴的特殊的大存储容量使sWAT成为脂肪的有效存储库。因此,sWAT功能的破坏会导致高循环水平的脂质,这些脂质在非脂肪细胞中积累,导致脂肪毒性和胰岛素抵抗。除了储存和释放脂肪酸的能力外,白色脂肪细胞还分泌脂肪因子,控制食物的摄入和利用。例如,瘦素对中枢神经系统的作用控制饱腹感,脂联素和瘦素控制外周组织的脂质利用。通过这种内分泌功能,脂肪细胞在调节全身能量平衡中起着关键作用。
衰老导致sWAT体积逐渐下降,随之脂质储存能力下降,这受到两性激素变化的不同影响。在许多物种中,包括小鼠、狗、猫和非人灵长类动物,都观察到皮下脂肪随着年龄增长而减少。即使在缺乏特化脂肪细胞的物种中,如果蝇,衰老的野生型果蝇头部和腹部脂肪体的脂肪分布质量也会逐渐减少(图1)。sWAT脂质储存能力的损害会导致全身其他细胞代谢脂质的压力增加,从而导致氧化还原和能量平衡失调,导致细胞衰老。除了在脂肪储存中发挥重要作用外,sWAT储存库的大小和功能还影响脂肪因子(如脂联素和瘦素)的循环水平。循环脂联素已被证明与人类长寿有关,并直接影响小鼠的寿命。
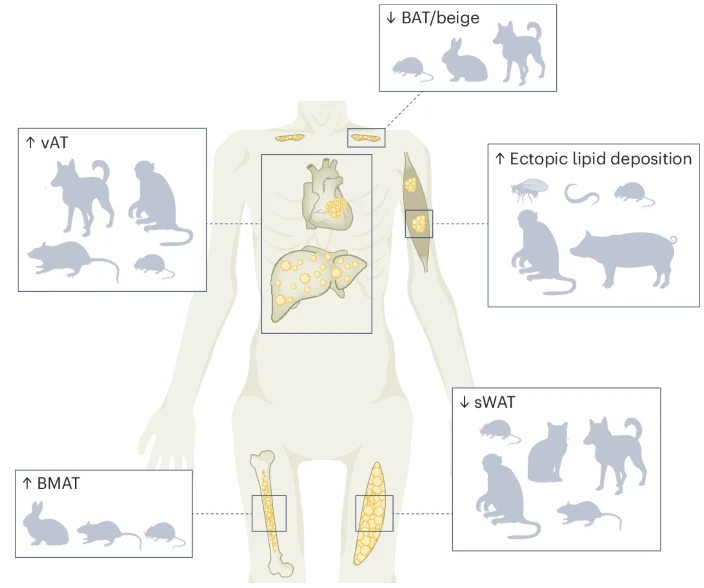
图1 衰老对人类(以及已报道出现类似变化的物种)脂肪组织的影响
内脏脂肪组织
内脏脂肪组织(vAT)存在于腹膜腔内,分布于网膜、肠系膜和性腺等区域。vAT的生理作用不同于sWAT,vAT发挥保护作用,它拥有一系列先天性和适应性免疫细胞,直接参与免疫监视。vAT的脂肪细胞与sWAT的脂肪细胞具有不同的特性,包括儿茶酚胺激活的脂肪分解率更高,对胰岛素的抑制具有抵抗力 ,以及明显不同的蛋白质组,富含参与能量代谢的蛋白质。
肥胖和衰老对vAT有类似的影响,其特征是浸润和常驻免疫细胞的定量和定性变化,向促炎表型转变。vAT中的脂肪细胞肥大和免疫细胞积累与胰岛素抵抗的关系比sWAT中的密切得多,vAT的扩张是Ⅱ型糖尿病、心血管疾病、中风和代谢综合征等年龄相关疾病的主要危险因素。对来自幼龄和老年小鼠vAT的脂肪细胞、基质祖细胞和免疫细胞的分析表明,促进年龄相关脂肪组织炎症的介质的主要来源不是脂肪细胞,而是免疫细胞和基质祖细胞。然而,衰老的脂肪细胞可能是影响免疫细胞发育的Wnt配体等因素的来源,从而导致炎症。在多个物种中证实了与衰老相关的vAT库大小变化和炎症状态的产生相关(图1)。
棕色和米色脂肪组织
脂肪组织的第二个众所周知的作用是体温调节,它在通过非颤抖性产热来维持体温方面起着关键作用。非颤抖产热主要由棕色或米色脂肪细胞介导,由线粒体解偶联蛋白1 (UCP1)的表达决定。UCP1的激活加速了电子传递,从而产生热量。脂肪库主要由棕色脂肪组织(BAT)组成,存在于小鼠和人类新生儿的肩胛间区域。米色脂肪细胞表现出棕色脂肪细胞的主要特征,包括UCP1的表达、多房脂滴和丰富的线粒体,但它们散布在人类锁骨上、肾上和主动脉旁间隙等处的白色脂肪细胞中,在小鼠中主要出现在腹股沟皮下脂肪库中。
人类在冷暴露期间通过18 F-氟脱氧葡萄糖正电子发射断层扫描(FDG-PET)测量产热脂肪组织的数量,这是一种功能性读数,可以反映产热脂肪细胞数量、现有脂肪细胞活性或两者的变化。FDG-PET研究表明老年人的活性下降。在热中性条件下的分析揭示了性别依赖性和肥胖依赖性效应,其中老年男性的产热脂肪组织减少速度比女性更快。在一项对52487名患者进行FDG-PET扫描的大型回顾性研究中,棕色脂肪的分布随着年龄的增长而下降,其丰度与较低的心脏代谢疾病患病率和较低的Ⅱ型糖尿病发病率相关。在小鼠、大鼠、狗和家兔中,衰老与棕色和米色脂肪细胞丰度减少以及产热脂肪组织减少有关。在非人类灵长类动物中已经检测到产热脂肪组织,并且在患有糖尿病的动物中显示出减少,但是在非人灵长类动物中,衰老对产热脂肪组织的影响尚未得到系统的研究。因此,产热脂肪组织的减少或退化似乎在物种中高度保守,并与衰老相关病理的出现有关(图1)。
骨髓脂肪组织
出生后,造血发生在骨髓中,位于由骨小梁支撑的血管丰富的正弦区域内。脂肪细胞在出生后早期就开始出现在这些区域内,并随着年龄的增长占据骨髓体积越来越大的比例。据报道,与衰老相关的骨髓脂肪组织(BMAT)扩张发生在多个物种中,包括人类、兔子、小鼠和大鼠(图1)。
骨髓脂肪细胞在形态学和转录组学景观上与其他部位的白色脂肪细胞不同,并且骨髓脂肪细胞的亚型可以通过脂质组成来区分。调节性BMAT代表对全身代谢变化更敏感的脂肪细胞,富含不饱和脂质,主要位于骨骺附近。组成性BMAT对全身代谢变化的反应较小,富含饱和脂质,主要位于远端骨骼中骨髓的骨。从骨髓中分离和培养脂肪细胞存在技术困难,因此很难具体探索BMAT扩增在衰老过程中的作用。针对骨髓脂肪细胞的几种转基因小鼠模型表明,它们在介导与衰老相关的骨稳态、造血和免疫变化方面具有潜在作用。这些模型中的特异性是由谱系启动子赋予的,这些启动子可能并不完全局限于BMAT,需要实施进一步的互补研究方法。BMAT扩增与年龄相关的骨髓功能变化之间的高度物种保守关联使其成为继续研究的重要领域。
其他脂肪组织库
脂肪组织除存在于皮下、内脏和骨髓库中外,还广泛分布于其他器官和组织中,包括神经鞘、血管周围、以及心脏等器官的直接邻近区域。人类、非人类灵长类动物、小鼠和猪的横纹肌和心肌中都会随着衰老出现脂肪细胞(图1 ) 。在骨骼肌、心肌和受伤后的其他部位 中也发现了脂肪细胞。衰老和受伤导致非脂肪库内形成脂肪细胞的机制,以及脂肪组织在这些部位的作用,目前在很大程度上仍不清楚。这种反应可能构成一种保护机制,例如,确保局部能量供应,也可能是一种损害组织功能的适应不良过程。要回答这些问题,需要进一步探索脂肪细胞在大型脂肪库外的作用。除了异位脂肪细胞的形成外,衰老还会导致非脂肪细胞中的脂质积累,甚至在将脂肪储存在非脂肪细胞中的物种中也会发生这种情况。
衰老脂肪组织的细胞特征
虽然脂肪细胞由于体积大而构成了脂肪组织的大部分体积,但必须强调的是,它们只占组织内细胞的一半以下。事实上,免疫细胞、血管和淋巴管内皮细胞以及多能间充质干细胞/祖细胞占脂肪组织内细胞的 50% 以上。脂肪组织间充质祖细胞不仅能够替代脂肪细胞,还能分化成多种途径,包括成骨和软骨形成途径。因此,随着年龄增长,脂肪组织祖细胞功能受损可能导致组织修复受损。脂肪组织内浸润的免疫细胞和内皮细胞可能是与衰老相关的全身性、轻度促炎表型的基础,这反过来也可能影响组织修复和免疫稳态。下文将回顾最近关于衰老对脂肪组织细胞类型的影响的研究(图2)。
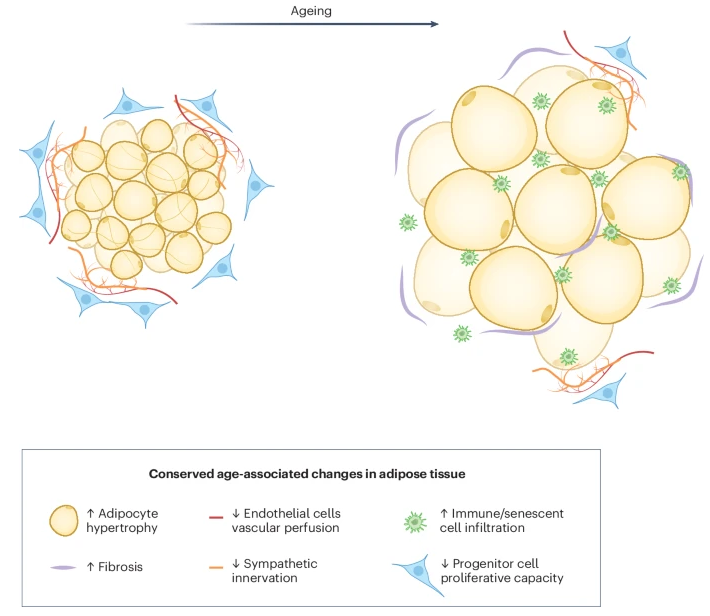
图2 脂肪组织细胞组成随年龄的变化
脂肪细胞
脂肪库可以通过调节脂肪细胞数量或增加每个脂肪细胞的尺寸来收缩或扩张。后一种特性非常显著,因为脂肪细胞直径范围从不到20µm到300μm,这表明不同细胞的脂质储存能力相差数倍。一般情况下,脂肪细胞的尺寸会随着年龄的增长而不断增加。在人类中,脂肪细胞的周转速度异常缓慢,这表明长寿细胞会随着年龄的增长而不断增加其储存能力。在多个物种中,包括大鼠、鱼、小鼠和猴,白色脂肪组织(WAT)和BAT中的脂肪细胞尺寸都会随着年龄的增长而增加。在小鼠中,肥大性BAT脂肪细胞也会失去其多房特征,在衰老过程中变得更像单房白色脂肪细胞。脂肪细胞大小与胰岛素抵抗受损相关,无论大型脂肪细胞是由肥胖饮食还是衰老产生。
祖细胞
在发育过程中,新脂肪细胞的形成取决于脂肪组织中间充质祖细胞(也称为脂肪组织干细胞或基质祖细胞)的存在,以及它们进行脂肪形成轨迹的能力。据推测,增生所必需的祖细胞增殖和/或分化下降是导致衰老相关脂肪细胞肥大的原因。研究衰老对脂肪组织祖细胞的影响的研究得出了不同的结果。测量祖细胞增殖能力的不一致结果可能归因于物种和库特异性差异。然而,即使在增殖潜力没有改变的研究中,衰老也会影响脂肪组织来源的祖细胞进行成骨分化的能力 ,这反映了生理相关的改变。
最近,通过应用单细胞和单核RNA测序,对脂肪组织内细胞的转录组进行了全面分析。这些研究为衰老对脂肪组织祖细胞的影响提供了重要的新见解,但这些结果并不一致。尽管如此,在小鼠中研究衰老的影响和异时共生的影响后发现,来自脂肪组织的祖细胞在差异表达基因数量上随年龄的变化差异最大。此外,基质祖细胞对衰老环境的反应比来自其他组织的基质祖细胞更强烈:与老年小鼠共生的年轻小鼠脂肪组织的基质祖细胞与其他组织相比显示出最多数量的差异表达基因(加速衰老表型 ),而来自老年小鼠脂肪组织的基质祖细胞对与年轻小鼠的共生表现出强烈的反应(恢复活力表型)。虽然老年小鼠和年轻小鼠之间的共生关系很复杂,细胞反应可能不仅反映衰老的影响,但这些结果表明脂肪组织的祖细胞对环境干扰高度敏感。
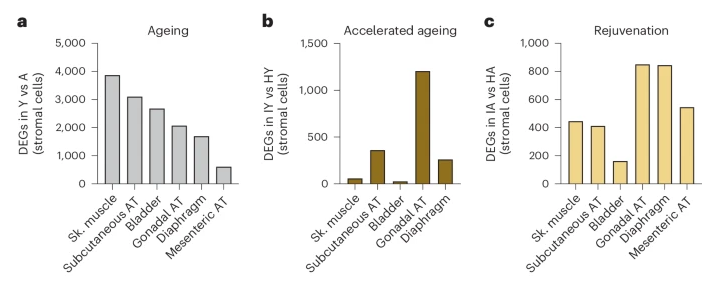
图3 基质祖细胞的基因表达随年龄变化
免疫细胞
小鼠肥胖后,脂肪组织中会出现巨噬细胞浸润,不过这种反应在人类脂肪组织中不太明显。无论是小鼠还是人类,免疫细胞浸润在 vAT 中都比在 SAT 中更明显,并且与脂肪细胞增大、脂肪分解和脂肪组织纤维化有关。在衰老过程中,脂肪细胞增大,与肥胖类似,免疫细胞也会积聚。然而,在衰老过程中,免疫细胞在其他多种组织中也变得可检测到,这表明衰老相关的免疫浸润机制不同。有趣的是,免疫细胞在衰老过程中首次在脂肪组织中检测到,这表明脂肪组织功能和免疫细胞动态与年龄之间存在密切的相互作用。浸润衰老脂肪组织的免疫细胞不仅包括巨噬细胞,还包括 B 细胞和 T 细胞以及嗜酸性粒细胞,所有这些细胞都可能影响组织稳态和代谢。
在衰老过程中,介导免疫细胞浸润脂肪组织的机制尚不清楚,但与年龄相关的脂肪细胞肥大可能起着关键作用。巨噬细胞的募集可能是由脂肪细胞增大引起的脂肪分解增加引起的,而脂肪细胞增大又源于胰岛素抵抗 。募集到肥大、缺氧环境的巨噬细胞可能会向更具炎症性的表型极化,并在介导肥胖所见的全身胰岛素抵抗方面发挥主导作用。最近的一项研究支持了这一观点,该研究将老年小鼠的 vAT 移植到幼鼠的颈动脉中,可增加移植部位附近颈动脉以及远端血管床的动脉粥样硬化斑块大小。移植前清除内脏脂肪中的巨噬细胞可大大减轻这些影响,表明脂肪组织巨噬细胞在介导与年龄相关的组织损伤方面起主导作用。
综上所述,上述研究支持了以下观点:在小鼠和人类中,免疫细胞浸润会损害 WAT 功能,对组织完整性和全身能量稳态产生负面影响。然而,巨噬细胞浸润也在脂质稳态中发挥积极作用,并介导脂肪组织的修复和维持。免疫细胞浸润在产热脂肪组织中也发挥着矛盾的作用,其中衰老免疫细胞的浸润导致产热功能受损,至少部分原因是通过损害儿茶酚胺激活产热,但巨噬细胞也与褐变增强呈正相关。
巨噬细胞对白色脂肪组织和产热脂肪组织的矛盾作用表明,浸润的免疫细胞可能引发适应性或适应不良的功能反应。这种矛盾的一个可能解释是,浸润免疫细胞的表型可能影响脂肪细胞或组织中其他细胞的反应。衰老的免疫细胞可能偏向于更具炎症性的表型,它们与肥大性脂肪细胞的相互作用会引发适应不良的反应。为了支持这种可能性,最近的几项研究表明,老年小鼠脂肪组织中浸润的巨噬细胞显示出衰老标志物,因此在功能上可能与能够介导上述健康、适应性反应的年轻巨噬细胞不同。
内皮细胞和神经支配
衰老的脂肪组织表现出血管减少和缺氧增加,表明内皮细胞功能障碍。单细胞衰老研究和异时共生表明,脂肪组织的内皮细胞对衰老和加速衰老敏感,尽管程度低于祖细胞或巨噬细胞。内皮细胞对衰老的敏感性是细胞自主的还是继发于内皮细胞和脂肪细胞之间的相互作用尚不清楚,但脂肪组织以外组织的内皮细胞对衰老不太敏感这一发现表明存在组织依赖性效应。随着年龄的增长,脂肪细胞表达的关键血管生成因子VEGF水平会降低,抗VEGF治疗会产生年龄依赖性的代谢效应,支持衰老脂肪细胞对脂肪组织血管的直接影响。老年小鼠脂肪组织中周围神经丰度降低,且与老年性周围神经病变有关。神经支配与血管生成密切相关,值得进一步研究衰老过程中脂肪组织中内皮细胞和神经元细胞功能之间的关系。
衰老细胞
细胞衰老最初被描述为原代成纤维细胞体外复制能力的逐渐下降,导致不可逆的细胞周期停滞状态。复制性衰老是由端粒缩短引起的DNA损伤以及其他形式的持续性DNA损伤引发的,例如由氧化应激、放疗、化疗和致癌有丝分裂信号引起的DNA损伤。体DNA损伤引起的有丝分裂停滞伴有分泌反应,包括许多细胞因子,统称为衰老相关分泌表型(SASP)。
复制性衰老和DNA损伤相关衰老已在培养细胞中得到明确定义和广泛表征,类似事件也被认为会导致衰老和与年龄相关的疾病。在早衰小鼠、DNA修复缺陷小鼠以及正常衰老大鼠和小鼠的脂肪组织中检测到了显示衰老标志物的细胞。
很少有研究同时对衰老标志物和细胞标志物进行成像,因此老年动物完整脂肪组织内衰老细胞的身份尚不清楚。在一个例子中,衰老脂肪组织中与衰老相关的β-半乳糖苷酶染色呈阳性的细胞对巨噬细胞标志物也呈阳性染色。这些结果表明,脂肪组织中至少有一些衰老细胞可能对应于浸润性巨噬细胞,巨噬细胞会随着衰老在脂肪组织中积聚。由于衰老标志物的表达水平低 ,脂肪组织中全部衰老细胞可能难以识别,这可能会妨碍在单细胞和单核研究中对其进行识别。此外,最近在单细胞水平上检查衰老细胞的研究揭示,在组织内和不同组织之间,公认的衰老标志物的表达存在显著的异质性 。这些新发现强调需要结合完整脂肪库内的细胞身份标志物来识别多种衰老标志物,以更好地定义衰老过程。尽管如此,体外研究已推断出衰老脂肪组织中存在衰老祖细胞,在这些研究中,从衰老小鼠的脂肪组织培养的细胞与来自年轻动物的细胞相比在形态学、增殖和转录组学上存在差异。类似地,来自具有肥大性脂肪细胞的人类脂肪组织的祖细胞(随着肥胖和衰老而发展)在体外培养后显示出衰老标志物。
在非人灵长类动物中,已从老年个体的脂肪组织培养的细胞中发现了对衰老相关的β-半乳糖苷酶呈阳性的基质细胞,但在体内未检测到。在组织中检测衰老细胞通常很困难,这促使人们最近采取举措来提供进一步的方法来可靠地识别它们。采用这些策略可能会提高识别脂肪组织中衰老细胞的能力,并且如下所述,提高针对衰老细胞的治疗方法。值得注意的是,在衰老标志物出现之前,老年小鼠的祖细胞在体外表现出增殖能力下降,这表明衰老机制可能尚未完全确定。
潜在的改善措施
衰老带来的衰弱影响和疾病负担迫使人们研究如何减轻甚至逆转这些不利影响。任何潜在方法的成功都取决于与年龄相关的细胞功能缺陷(例如由氧化还原应激产生的缺陷)是否可逆。秀丽隐杆线虫的肠道是脂肪储存的主要部位,作用于胰岛素受体信号传导的等位基因可以大大延长寿命,胰岛素受体信号传导是控制全身能量代谢的中心途径。特异性的阻断老年秀丽隐杆线虫肠道中的胰岛素信号传导可使寿命翻倍,这提供了遗传证据表明可以通过特定干预来延长寿命。这些在秀丽隐杆线虫中的发现指出了脂质代谢和整体能量调节在衰老中的作用,与下文讨论的其他研究一致,这些研究表明,延长寿命最有效的方法与脂肪组织的重要功能直接相关。
热量限制和间歇性禁食
缓解衰老带来的代谢影响并延长寿命的研究最为广泛的方法是热量限制。热量限制是指将总热量消耗降低到避免营养不良的程度,并可延长从酵母到灵长类动物等众多物种的寿命。间歇性禁食包括几种定期限制食物的方式,而不一定降低净热量消耗,已证明对人类和非人类灵长类动物的多种代谢参数具有有益作用。间歇性禁食已被证明可以延长小鼠的寿命,但需要前瞻性临床试验结果来确定它是否会导致人类寿命延长。
热量限制和间歇性禁食改善代谢参数和寿命的机制尚不完全清楚,因为这些干预措施与多种与衰老相关的信号通路有关。热量限制和间歇性禁食都会促进脂肪组织中的脂肪分解,从而导致外周组织中的β氧化和氧化还原应激。因此,对氧化还原状态作出反应的信号通路可能是这些干预措施产生有益效果的基础。Sirtuins是一个对氧化还原状态变化反应灵敏的蛋白质家族,在抗氧化防御中发挥着重要作用。周期性的β氧化介导的应激可能会增强外周组织中的Sirtuin活性,增强抗氧化防御并保护细胞免于衰老相关的功能衰退。为什么这些机制无法应对肥胖和衰老过程中脂肪细胞储存受损导致的脂肪酸循环增加,或者为什么转基因过度表达Sirtuins 无法产生代谢益处尚不清楚,但伴随的激素状态可能是一个重要因素,在热量限制期间,儿茶酚胺信号增强,胰岛素分泌减少,而营养过剩则相反。此外,脂肪细胞对脂肪分解信号的反应除了脂肪分解之外,还会产生其他作用,包括诱导血管生成和神经生成因子。这些机制在介导热量限制的有益作用中的机制仍有待探索。
二甲双胍是治疗Ⅱ型糖尿病患者的一线药物。人类纵向研究表明,使用二甲双胍治疗的糖尿病患者的生存率高于年龄匹配的非糖尿病对照组。虽然二甲双胍的作用并不局限于脂肪组织,但其全身作用会转化为脂肪组织功能的变化,包括促进线粒体脂肪酸代谢、不饱和脂肪酸生物合成、PPAR和SREBP信号传导、LXR/RXR活化、胶原链三聚化和脂肪组织细胞外基质重塑。体外研究还发现二甲双胍可以减缓脂肪来源的祖细胞衰老,如果在体内重现这些作用,可能会克服与祖细胞分化丧失有关的脂肪细胞肥大。
噻唑烷二酮类
噻唑烷二酮(TZD)激活PPARγ已被证明可以延长小鼠的寿命,回顾性研究表明其临床应用与死亡率降低有关。这种效果似乎是可以保留的,因为鱼类中PPARγ的激活可增强对压力的适应性。TZD促进脂肪组织重塑,包括出现更小的脂肪细胞、增加毛细血管密度和增加祖细胞增殖。从系统上讲,TZD可减少肝脏和外周甘油三酯的积累,减少内脏脂肪并增加循环脂联素 , 逆转与年龄相关的脂肪组织功能障碍。然而,尽管TZD在临床前模型中显示出有希望的抗衰老作用,但它在人体临床上的应用却受到与TZD相关的并发症的限制,包括女性骨密度降低导致骨折风险增加。推测骨髓密度降低是由于骨细胞功能受损,可能继发于骨髓间充质祖细胞的影响。这些数据强调了针对特定脂肪库以最大化治疗选择的重要性。
恢复脂肪细胞祖细胞库
维持脂肪组织祖细胞的功能可能对于脂肪组织在整个生命周期中的功能至关重要。如上所述,这些细胞对衰老和加速衰老高度敏感,并且它们的增殖潜力会随着年龄的增长而降低。因此,维持功能性祖细胞库的干预措施可以恢复脂肪组织与年龄相关的功能障碍。人们抑制探索决定人类脂肪组织祖细胞命运的机制 。研究发现,罗格列酮可增强脂肪组织祖细胞的增殖,并降低其处于静止状态的比例。这些研究表明,PPARγ激活不仅可以增强成熟脂肪细胞的功能,还可以刺激祖细胞增殖和自我更新,促进脂肪细胞分化,从而导致增生和脂质储存改善。
脂肪因子模拟物
衰老脂肪细胞功能障碍的特征之一是脂联素失调,如上所述,这与人类的长寿有关。基于与年龄相关的脂联素生成下降,人们研究了用合成小分子AdipoR激动剂(脂联素受体激动剂:AdipoRon)治疗。结果发现,AdipoRon可激活AMPK和PPARα,加速脂肪酸氧化,并改善肝脏、骨骼肌和脂肪组织的胰岛素敏感性。这些有益作用与糖尿病小鼠模型的长寿有关。
抗衰老产品
细胞衰老伴有分泌表型,包括多种与衰老不同程度相关的炎性细胞因子。近年来,关于消除衰老细胞以延长寿命和改善健康的研究如雨后春笋。这种方法得到了遗传模型的支持,在该模型中,表达衰老标志物p16和p21的细胞通过激活特定启动子驱动的促凋亡转基因而被消除。据报道,这种方法可以延缓多种与衰老相关的表型出现,并延长平均寿命。
除了遗传模型外,人们还在积极探索使用衰老细胞清除剂(senolytics,一种可以选择性消除衰老细胞的药物)。衰老细胞清除剂包括激酶抑制剂、Bcl-2家族蛋白抑制剂、天然多酚、热休克蛋白抑制剂、BET家族蛋白抑制剂、P53稳定剂、PPARα激动剂和抗生素等。据报道,达沙替尼和槲皮素可以减少脂肪炎症并延长老年小鼠的寿命。
在一项开放标签 I 期试点研究中,使用达沙替尼和槲皮素治疗3天可减少患有糖尿病肾病的老年人的脂肪组织衰老细胞负担和衰老相关的分泌表型因子。在小鼠模型中,衰老细胞清除剂可减轻脂肪组织炎症并改善老年人的全身代谢功能。有趣的是,在同一项研究中,肝脏或骨骼肌中并未观察到衰老细胞清除剂的作用,强调了脂肪组织在与年龄相关的代谢功能障碍中的关键作用。在非人类灵长类动物中,达沙替尼和槲皮素在多种免疫细胞类型中产生显著的抗炎表型,并降低脂肪组织中的衰老标志物基因表达。确定脂肪组织中在达沙替尼和槲皮素作用下衰老细胞负担减少的细胞身份非常重要。据报道,免疫细胞耗竭可增强脂肪组织功能并预防与衰老相关的全身胰岛素抵抗。达沙替尼和槲皮素导致性腺脂肪组织中浸润 T 细胞和巨噬细胞数量减少,这表明它们对全身代谢的影响可能至少部分归因于脂肪组织免疫细胞负担的改善。在斑马鱼模型中,已观察到衰老细胞清除剂可直接减轻慢性炎症,这表明免疫细胞的产生或功能可能对这些药物有反应。阐明达沙替尼和槲皮素对脂肪组织中特定细胞的有益代谢作用将是临床研究中令人兴奋的挑战。
总结
从单细胞真核生物到人类,都观察到能量稳态与衰老之间的关系。脂质代谢是细胞能量的基本来源,但其通过线粒体β氧化的代谢会导致氧化还原应激增强,β氧化受损会导致有毒副产物的积累,从而导致细胞衰老。脂肪组织在控制脂质分布中起着关键的、物种保守的作用,因此,它的功能对全身能量代谢、细胞应激和细胞衰老至关重要。正如单细胞转录组学分析所确定的那样,脂肪组织可能是最早对衰老做出反应的器官之一,这使得它可能随后推动整个生物体的衰老。
脂肪组织的变化,如sWAT的下降、产热功能的下降和骨髓脂肪的积累,在许多物种中都是保守的,这一事实支持了脂肪组织在生物体衰老中的保守作用。其中,BMAT的积累令人感兴趣,因为它在出生后发育早期开始并持续到成年期,在此之前脂肪组织中其他与衰老相关的变化尚未显现。骨髓脂肪细胞的这种发育程序化形成可能在确定新生免疫细胞的表型以及它们在衰老过程中与组织和器官相互作用的适应或不适应后果方面发挥关键作用。脂肪组织是机体衰老的驱动力这一假设也与年龄相关疾病具有与衰老无关的脂肪组织功能障碍直接相关的代谢性疾病(如肥胖)的特征相一致。
需要进一步研究探究脂肪细胞如何直接接近多个器官和组织的细胞,如血管周围、神经周围和骨髓中的细胞,影响细胞功能和影响衰老表型,以及物种保守的衰老程序是否通过脂肪组织起作用来指导衰老。这些信息将有助于为减轻与衰老有关的疾病负担和延长寿命的方法提供有价值信息。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


